Fe2O3 + HCl → FeCl3 + H2O | Fe2O3 ra FeCl3
Fe2O3 + HCl → FeCl3 + H2O là phản ứng trao đổi. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng Fe2O3 + HCl → FeCl3 + H2O
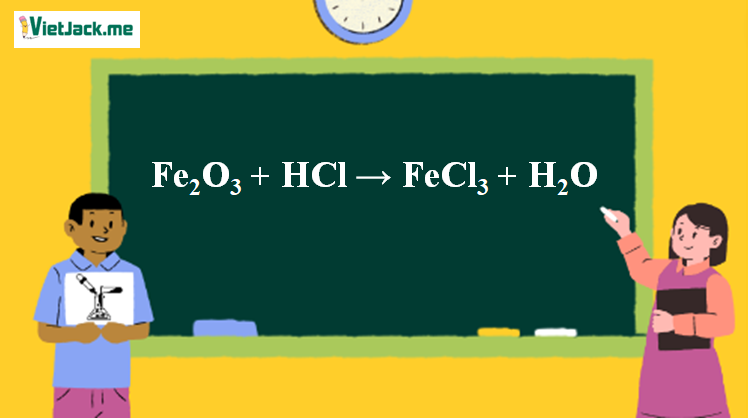
1. Phương trình phản ứng Fe2O3 tác dụng HCl
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
2. Điều kiện phản ứng Fe2O3 tác dụng với dung dịch axit HCl
Không có
3. Cách thực hiện phản ứng Fe2O3 tác dụng với dung dịch axit HCl
Cho vào đáy ống nghiệm một ít oxit bazơ Fe2O3 thêm 1-2 ml dung dịch axit, sau đó lắc nhẹ.
4. Hiện tượng phản ứng
Chất rắn màu đen Sắt III Oxit (Fe2O3) tan dần, tạo ra dung dịch có màu vàng nâu.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của Fe2O3 (Sắt (III) oxit)
Fe2O3 mang tính chất của một oxit bazơ tác dụng với dung dịch axit tạo ra dung dịch bazơ tạo ra dung dịch muối và nước.
5.2. Bản chất của HCl (Axit clohidric)
HCl có tính oxi hóa nên tác dụng oxit kim loại tạo thành muối clorua (kim loại không thay đổi hóa trị) + nước.
6. Thông tin kiến thức về Fe2O3
6.1. Tính chất hóa học của Fe2O3
Fe2O3 là một oxit của sắt, Fe2O3 là dạng phổ biến nhất của sắt oxit tự nhiên. Ngoài ra có thể lấy chất này từ đất sét màu đỏ.
Công thức phân tử: Fe2O3
Tính oxit bazơ
Fe2O3 tác dụng với dung dịch axit tạo ra dung dịch bazơ tạo ra dung dịch muối và nước.
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Fe2O3 + 6HNO3 → 2Fe(NO3)3+ 3H2O
- Tính oxi hóa
Fe2O3 là chất oxi hóa khi tác dụng với các chất khử mạnh ở nhiệt độ cao như: H2, CO, Al:
Fe2O3 + 3H2 → 2Fe + 3H2O
Fe2O3 + 3CO → 2Fe + 3CO2
Fe2O3+ 2Al → Al2O3 + 2Fe
6.2.Trạng thái tự nhiên
Fe2O3 có trong tự nhiên dưới dạng quặng hematit đỏ (Fe2O3 khan) và quặng hematit nâu (Fe2O3.nH2O).
6.3. Ứng dụng Sắt III Oxit
Fe2O3 có vai trò rất quan trọng trong việc tạo màu cho các loại men gốm sứ và giúp làm giảm rạn men; dùng để luyện gang, thép.
6.4. Điều chế Sắt III Oxit
Fe2O3 có thể điều chế bằng phản ứng phân hủy Fe(OH)3 ở nhiệt độ cao.
Nhiệt phân Fe(OH)3
2Fe(OH)3 Fe2O3 + 3H2O
7. Tính chất hoá học của HCl
Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
7.1. Tác dụng chất chỉ thị
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
7.2. Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Fe + 2HCl 
2Al + 6HCl 
Cu + HCl → không có phản ứng
7.3. Tác dụng với oxit bazo và bazo
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
CuO + 2HCl 
Fe2 O3 + 6HCl
7.4. Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
8. Bài tập vận dụng liên quan
Câu 1. Nhận xét nào sau đây không đúng?
A. Crom là kim loại cứng nhất trong tất cả các kim loại
B. Nhôm và crom đều phản ứng với HCl theo cùng tỉ lệ số mol.
C. Vật dụng làm bằng nhôm và crom đều bền trong không khí và nước vì có màng oxit bảo vệ.
D. Nhôm và crom đều bị thụ động hóa bởi HNO3 đặc, nguội
Lời giải:
B. Nhôm và crom đều phản ứng với HCl theo cùng tỉ lệ số mol.
Câu 2. Những nhận định sau về kim loại sắt:
(1) Kim loại sắt có tính khử trung bình.
(2) Ion Fe2+ bền hơn Fe3+.
(3) Fe bị thụ động trong H2SO4 đặc nguội.
(4) Quặng manhetit là quặng có hàm lượng sắt cao nhất.
(5) Trái đất tự quay và sắt là nguyên nhân làm Trái Đất có từ tính.
(6) Kim loại sắt có thể khử được ion Fe3+.
Số nhận định đúng là
A. 3
B. 4
C. 5
D. 6
Lời giải:
(1) đúng
(2) sai, Fe2+ trong không khí dễ bị oxi hóa thành Fe3+
(3) đúng
(4) đúng, quặng manhetit (Fe3O4) là quặng có hàm lượng Fe cao nhất.
(5) sai, vì từ trường Trái Đất sinh ra do sự chuyển động của các chất lỏng dẫn điện
(6) đúng, Fe + 2Fe3+ → 3Fe2+
Vậy có 4 phát biểu đúng
Câu 3. Dãy các chất và dung dịch nào sau đây khi lấy dư có thể oxi hoá Fe thành Fe (III)?
A. HCl, HNO3 đặc, nóng, H2SO4 đặc, nóng
B. Cl2, HNO3 nóng, H2SO4 đặc, nguội
C. bột lưu huỳnh, H2SO4 đặc, nóng, HCl
D. Cl2, AgNO3, HNO3 loãng
Lời giải:
Phương trình phản ứng minh họa
2Fe + 3Cl2→ 2FeCl3
3AgNO3 + Fe → Fe(NO3)3 + 3Ag
Fe + 4HNO3 loãng → Fe(NO3)3 + NO↑ + 2H2O
Câu 4. Chia bột kim loại X thành 2 phần. Phần một cho tác dụng với Cl2 tạo ra muối Y. Phần hai cho tác dụng với dung dịch HCl tạo ra muối Z. Cho kim loại X tác dụng với muối Y lại thu được muối Z. Kim loại X có thề là
A. Mg.
B. Al.
C. Zn.
D. Fe.
Lời giải:
Phương trình phản ứng liên quan
2Fe + 3Cl2→ 2FeCl3 (Y)
Fe + 2HCl → FeCl2 (Z) + H2
Fe + 2FeCl3 → 3FeCl2
Câu 5. Dung dịch FeSO4 không làm mất màu dung dịch nào sau đây?
A. Dung dịch KMnO4 trong môi trường H2SO4
B. Dung dịch K2Cr2O7 trong môi trường H2SO4
C. Dung dịch Br2
D. Dung dịch CuCl2
Lời giải:
A. Mất màu tím KMnO4
18FeSO4 + 6KMnO4 + 12H2O → 6MnO2 + 5Fe2(SO4)3 + 8Fe(OH)3 + 3K2SO4
B. Mất màu da cam K2Cr2O7
6FeSO4+ K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
C. Mất màu dung dịch Br2
6FeSO4+ 3Br2 → 2Fe2(SO4)3 + 2FeBr3
Câu 6. Hòa tan 5 gam hỗn hợp bột Fe và Fe2O3 bằng một lượng dung dịch HCl vừa đủ, thu được 0,56 lít hidro (đktc) và dung dịch X. Cho dung dịch X tác dụng với dd NaOH lấy dư. Lấy kết tủa thu được đem nung nóng trong không khí đến khối lượng không đổi thu được chất rắn Y. Khối lượng chất rắn Y là:
A. 8 gam.
B. 7 gam.
C. 6 gam.
D. 7,5 gam.
Lời giải:
nH2 (đktc) = = 0,025 (mol)
Phương trình hóa học
Fe + 2HCl → FeCl2 + H2↑ (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
Theo PTHH (1): nFe = nH2 = 0,025 (mol) → mFe = 0,025.56 = 1,4 (g)
→ mFe2O3 = mhh - mFe = 5 - 1,4 = 3,6 (g) → nFe2O3 = = 0,0225 (mol)
Theo phương trình hóa học (1): nFeCl2 = nFe = 0,025 (mol)
Theo phương trình hóa học (2): nFeCl3 = 2nFe2O3 = 2.0,025 = 0,05 (mol)
Dung dịch X thu được chứa: FeCl2: 0,025 (mol) và FeCl3: 0,05 (mol)
Phương trình phản ứng hóa học
FeCl2 + 2NaOH → Fe(OH)2 + NaCl
FeCl3 + 3NaOH → Fe(OH)3 + NaCl
Kết tủa thu được Fe(OH)2 và Fe(OH)3
Nung 2 kết tủa này thu được Fe2O3
Bảo toàn nguyên tố "Fe": 2nFe2O3 = nFeCl2 + nFeCl3 → nFe2O3 = = 0,0375 (mol)
→ mFe2O3 = 0,0375.160 = 6 (g)
Câu 7. Dung dịch muối nào sau đây sẽ có phản ứng với dung dịch HCl khi đun nóng?
A. FeBr2
B. FeSO4
C. Fe(NO3)2
D. Fe(NO3)3
Lời giải:
Câu 8. Trong phòng thí nghiệm có thể điều chế khí hidro clorua bằng cách
A. Cho NaCl tinh thể tác dụng với H2SO4 đặc, đun nóng.
B. Cho NaCl tinh thể tác dụng với HNO3 đặc, đun nóng.
C. Cho NaCl tinh thể tác dụng với H2SO4 loãng, đun nóng.
D. Cho NaCl tinh thể tác dụng với HNO3 loãng, đun nóng.
Lời giải:
Cho NaCl tinh thể tác dụng với H2SO4 đặc, đun nóng.
Phương trình phản ứng hóa học
H2SO4 + 2NaCl ⟶ 2HCl + Na2SO4
Câu 9. Phát biểu nào sau đây sai?
A. NaCl được dung làm muối ăn và bảo quản thực phẩm.
B. HCl là chất khí không màu, mùi xốc, ít tan trong nước.
C. Axit clohidric vừa có tính oxi hóa, vừa có tính khử.
D. Nhỏ dung dịch AgNO3 vào dung dịch HCl, có kết tủa trắng.
Lời giải:
Câu 10. Cho các phản ứng hóa học sau:
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
2HCl + Fe → FeCl2 + H2
3HCl + Fe(OH)3 → FeCl3 + 3H2O
6HCl + 2Al → 2AlCl3 + 3H2
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Số phản ứng trong đó HCl thể hiện tính oxi hóa là
A. 2
B. 1
C. 4
D. 3
Lời giải:
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Câu 11. Dãy gồm các chất đều tác dụng được với dung dịch HCl loãng là
A. KNO3, CaCO3, Fe(OH)3
B. NaHCO3, AgNO3, CuO
C. FeS, BaSO4, KOH
D. AgNO3, (NH4)2CO3, CuS
Lời giải:
Phương trình phản ứng hóa học
NaHCO3 + HCl → NaCl + CO2 + H2O
AgNO3 + HCl → AgCl + HNO3
CuO + 2HCl loãng → CuCl2 + H2
Câu 12. Cho 7,8 gam hỗn hợp X gồm Al, Mg tác dụng với dung dịch HCl dư, thu được 8,96 lít H2 (đktc). Thành phần phần trăm khối lượng của Al trong X là
A. 69,23%
B. 34,60%
C. 38,46%
D. 51,92%
Lời giải:
nH2 = 0,4 mol
Bảo toàn electron
3nAl + 2nMg = 2nH2 ⇒ 3nAl + 2nMg = 0,8 (1)
mhh = 27nAl + 24nMg = 7,8 (2)
Giải hệ (1) và (2) ⇒ nAl = 0,2 (mol); nMg = 0,1 mol
⇒ %mAl = .100% = 69,23%
Câu 13. Phản ứng xảy ra khi đốt cháy sắt trong không khí là
A. 3Fe + 2O2 Fe3O4.
B. 4Fe + 3O2 2Fe2O3.
C. 2Fe + O2 2FeO.
D. tạo hỗn hợp FeO, Fe2O3, Fe3O4.
Lời giải:
Câu 14. Dãy các chất và dung dịch nào dưới đây khi lấy dư có thể oxi hoá Fe thành Fe (III)?
A. HCl đặc; HNO3 đặc, nóng; H2SO4 đặc, nóng
B. Cl2; HNO3 nóng; H2SO4 đặc, nguội
C. S; H2SO4 đặc nóng; HCl loãng
D. Cl2, AgNO3, HNO3 loãng
Lời giải:
Phương trình phản ứng hóa học
2Fe + 3Cl2→ 2FeCl3
Fe + 3AgNO3 → Fe(NO3)3 + 3Ag
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Câu 15. Cho 4 kim loại A, B, C, D đứng sau Mg trong dãy hoạt động hóa học, biết rằng:
A, B tác dụng được với dung dịch H2SO4 loãng giải phóng khí Hidro
C, D không có phản ứng với dung dịch H2SO4 loãng
B tác dụng với dung dịch muối của A và giải phóng kim loại A
D tác dụng được với dung dịch muối của C là giải phóng kim loại C
Kim loại có tính khử yếu nhất trong 4 kim loại là:
A. Kim loại D
B. Kim loại B
C. Kim loại C
D. Kim loại A
Lời giải:
A, B phản ứng được với H2SO4 loãng => A, B đứng trước H trong dãy hoạt động hóa học
C, D không phản ứng với H2SO4 loãng => C, D đứng sau H trong dãy hoạt động hóa học
=> X, Y có tinh khử mạnh hơn Z, T. Giờ chỉ so sánh C và D
D đẩy được C ra khỏi muối của D => D có tính khử mạnh hơn C
=> C là có tính khử yếu nhất
Câu 16. Có thể dùng hóa chất nào sau đây để nhận biết các kim loại sau: Al, Na, Cu
A. Nước
B. dung dịch NaOH
C. dung dịch HCl
D. dung dịch H2SO4
Lời giải:
Lấy mỗi kim loại 1 ít, lần lượt cho nước vào từng kim loại
Kim loại nào không tan là Cu, Al
Kim loại nào tan có hiện tượng sủi bọt khí không màu không mùi là Na
Na + H2O → NaOH + H2
Cho dung dịch NaOH ở ống nghiệm đã nhận biết được Na vào 2 kim loại còn lại: Al, Cu
Kim loại nào có hiện tượng sủi bọt khí không màu không mùi là Al, không có hiện tượng gì là Fe
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Câu 17. Thí nghiệm nào sau đây có hiện tượng sinh ra kết tủa trắng và bọt khí thoát ra khỏi dung dịch?
A. Nhỏ từ từ dung dịch HCl vào ống nghiệm đựng dung dịch Na2CO3.
B. Nhỏ từ từ dung dịch BaCl2 vào ống nghiệm đựng dung dịch AgNO3.
C. Nhỏ từng giọt dung dịch NaOH vào ống nghiệm đựng dung dịch CuCl2.
D. Nhỏ từ từ dung dịch H2SO4 vào ống nghiệm có sẵn một mẫu BaCO3.
Lời giải:
C. 2NaOH + CuCl2 → Cu(OH)2 + 2NaCl.
Hiện tượng sau phản ứng: có kết tủa màu xanh tạo thành.
D. H2SO4 + BaCO3→ BaSO4+ CO2 + H2O.
Hiện tượng sau phản ứng: có kết tủa trắng và bọt khí thoát ra khỏi dung dịch.
B. BaCl2+ AgNO3 → Ba(NO3)2 + 2AgCl.
Hiện tượng sau phản ứng: có kết tủa trắng tạo thành.
A. 2HCl + Na2CO3 → 2NaCl + CO2 + H2O.
Hiện tượng sau phản ứng: có khí thoát ra khỏi dung dịch.
Vậy thí nghiệm ứng với đề bài là: “Nhỏ từ từ dung dịch H2SO4 vào ống nghiệm có sẵn một mẫu BaCO3”.
Câu 18. Nếu cho dung dịch NaOH vào dung dịch FeCl3 thì xuất hiện
A. kết tủa màu nâu đỏ.
B. kết tủa màu trắng hơi xanh, sau đó chuyển dẩn sang màu nâu đỏ.
C. kết tủa màu trắng hơi xanh.
D. kết tủa màu xanh lam
Lời giải:
Khi ta cho dung dịch FeCl3 tác dụng với dung dịch NaOH tạo thành kết tủa có màu nâu đỏ.
Ta có phương trình phản ứng:
FeCl3 + 3NaOH → Fe(OH)3↓ nâu đỏ + 3NaCl
Câu 19. Chia bột kim loại X thành 2 phần. Phần một cho tác dụng với Cl2 tạo ra muối Y. Phần hai cho tác dụng với dung dịch HCl tạo ra muối Z. Cho kim loại X tác dụng với muối Y lạu thu được muối Z. Kim loại X có thể là?
A. Mg
B. Al
C. Zn
D. Fe
Lời giải:
Đáp án: D.
2Fe + 3Cl2 → 2Fe Cl3 (Y)
Fe + 2HCl → Fe Cl2 (Z) + H2
Fe + 2Fe Cl3 → 3Fe Cl2
Xem thêm các phương trình hóa học khác:
FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
