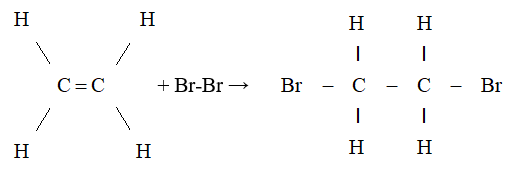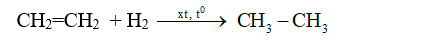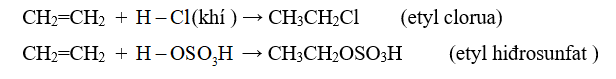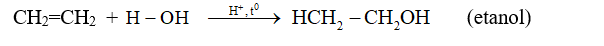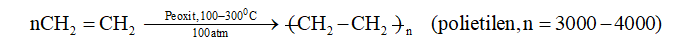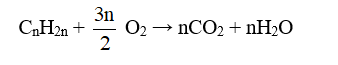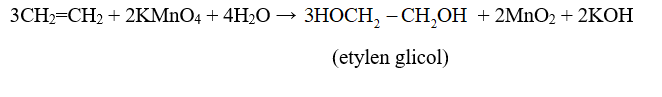CH2=CH-CH2-CH3 ra CH3-CHBr-CH2-CH3 l CH2=CH-CH2-CH3 + HBr → CH3-CHBr-CH2-CH3
CH2=CH-CH2-CH3 + HBr → CH3-CHBr-CH2-CH3 là phản ứng cộng. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng CH2=CH-CH2-CH3 + HBr → CH3-CHBr-CH2-CH3

1. Phương trình phản ứng But-1-en với HBr
CH2=CH-CH2-CH3 + HBr → CH3-CHBr-CH2-CH3
2. Bản chất của CH2=CH-CH2-CH3 (But-1-en) trong phản ứng
CH2=CH-CH2-CH3 là anken nên tham gia vào phản ứng cộng với nước, hidro halogen (HBr, HCl, HI) và với các axit mạnh.
3. Áp dụng Quy tắc Maccopnhicop
Quy tắc Maccopnhicop: Trong phản ứng cộng HX vào liên kết đôi, nguyên tử H (hay phần mang điện dương) chủ yếu cộng vào nguyên tử cacbon bậc thấp hơn (có nhiều H hơn), còn nguyên tử hay nhóm nguyên tử X (phần mang điện âm) cộng vào nguyên tử cacbon bậc cao hơn (có ít H hơn).
Khi đó, H sẽ cộng vào nguyên tử cacbon bậc thấp hơn (CH2) và Br sẽ cộng vào CH.
4. Tính chất hóa học của anken
Liên kết π ở nối đôi của anken kém bền vững, nên trong phản ứng dễ bị đứt ra để tạo liên kết σ với các nguyên tử khác. Vì thế, liên kết đôi là trung tâm phản ứng gây ra những phản ứng hóa học đặc trưng cho anken như phản ứng cộng, phản ứng trùng hợp và phản ứng oxis hóa.
4.1. Phản ứng cộng
- Phản ứng cộng halogen (phản ứng halogen hóa)
Cộng brom
- Dẫn khí etilen qua dung dịch brom màu da cam
- Hiện tượng: Dung dịch brom bị mất màu.
- Nhận xét: Etilen đã phản ứng với brom trong dung dịch.
- Liên kết kém bền trong liên kết đôi bị đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom. Phản ứng trên được gọi là phản ứng cộng.
- Ngoài brom, trong những điều kiện thích hợp, etilen còn có phản ứng cộng với một số chất khác. Ví dụ hiđro, clo.
- Nhìn chung, các chất có liên kết đôi (tương tự như etilen) dễ tham gia phản ứng cộng.
Cộng clo
- Phản ứng cộng hiđro (phản ứng hiđro hóa)
- Phản ứng cộng axit
+ Hiđro halogenua (HCl, HBr, HI), axit sunfuric đậm đặc ,... có thể cộng vào etilen.
- Phản ứng cộng nước (phản ứng hiđrat hóa)Ở nhiệt độ thích hợp và có xúc tác axit, etilen có thể cộng nước.
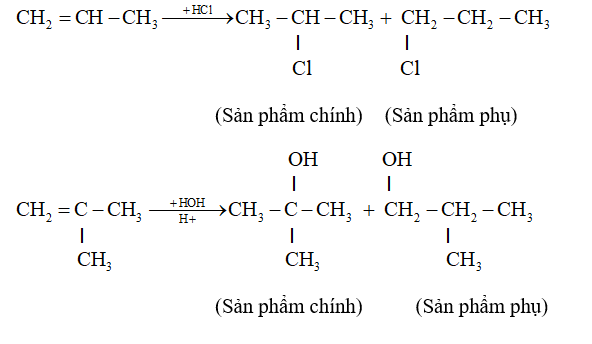
=> Hướng của phản ứng cộng axit và nước vào anken
- Phản ứng cộng axit hoặc nước vào anken bất đối xứng thường tạo ra hỗn hợp hai đồng phân, trong đó có một đồng phân là sản phẩm chính. Thí dụ:
4.2. Phản ứng trùng hợp
- Các anken ở đầu dãy như etilen, propilen, butilen trong những điều kiện nhiệt độ, áp suất, xúc tác thích hợp thì tham gia phản ứng cộng nhiều phân tử với nhau thành những phân tử mạch rất dài và có khối lượng phân tử rất lớn.
- Phản ứng trên được gọi là phản ứng trùng hợp.
- Polietilen là chất rắn, không tan trong nước, không độc. Nó là nguyên liệu quan trọng trong công nghiệp chất dẻo.
4.3. Phản ứng oxi hóa
- Giống với ankan, anken cháy hoàn toàn tạo ra CO2, H2O và tỏa nhiều nhiệt:
- Khác với ankan, anken làm mất màu dung dịch KMnO4:
- Phản ứng làm mất màu dung dịch thuốc tím kali pemanganat được dùng để nhận ra sự có mặt của liên kết đôi của anken.
5. Tính chất vật lí của Anken
Trong điều kiện thường, các anken từ C2H4 đến C4H8 là chất khí; từ C5H10 trở đi là chất rắn hoặc lỏng. Nhiệt độ nóng chảy, nhiệt độ sôi, khối lượng riêng của anken tăng dần theo chiều tăng của phân tử khối. Tất cả các anken đều nhẹ hơn nước (D <1g/cm3). Anken không tan trong nước.
6. Câu hỏi vận dụng
Câu 1. Khi cho but-1-en tác dụng với dung dịch HBr, theo quy tắc Maccopnhicop sản phẩm nào sau đây là sản phẩm chính ?
A. CH3-CH2-CHBr-CH3
B. CH3-CH2-CH2-CH2Br
C. CH3-CH2-CHBr-CH2Br
D. CH2Br-CH2-CH2-CH2Br
Lời giải:
Đáp án: A
Câu 2. Khi cho CH3-CH2-CH=CH2 tác dụng với dung dịch HBr theo quy tắc Maccopnhicop sản phẩm nào sau đây là sản phẩm chính?
A. CH3-CH2-CHBr-CH2Br
B. CH2Br-CH2-CH2-CH2Br
C. CH3-CH2-CHBr-CH3
D. CH3-CH2-CH2-CH2Br
Lời giải:
Đáp án: C
Câu 3. Sản phẩm chính khi cho cho but-1-en tác dụng với dung dịch HBr là
A. CH2Br-CH2-CH2-CH2Br
B. CH3-CH2-CH2-CH2Br
C. CH3-CH2-CHBr-CH2Br
D. CH3-CH2-CHBr-CH3.
Lời giải:
Đáp án: D
Câu 4. Chất nào dưới đây khi phản ứng với HCl thu được sản phẩm chính là 2-clobutan?
A. But-1-en
B. Buta-1,3-đien
C. But-2-in
D. But-1-in
Lời giải:
Đáp án: A
Xem thêm các phương trình phản ứng hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2025)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
- Tổng hợp thông tin, kiến thức chung
- Tiền tiểu học