CaC2 ra C2H2 l CaC2 + H2O → C2H2 + Ca(OH)2 | Canxi cacbua ra Axetilen
CaC2 + H2O → C2H2 + Ca(OH)2 là phản ứng trao đổi. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng CaC2 + H2O → C2H2 + Ca(OH)2
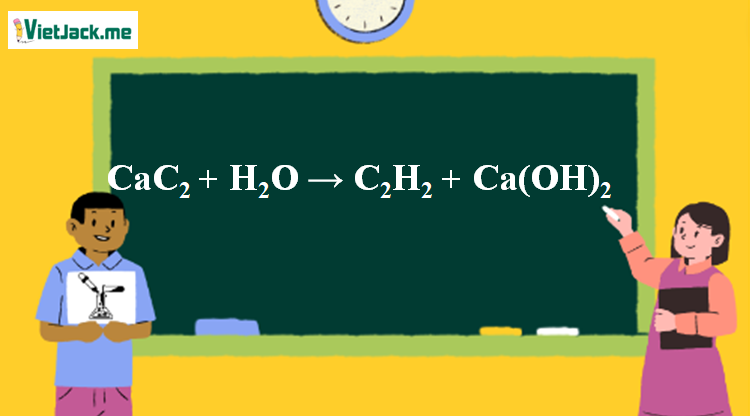
1. Điều chế C2H2 từ CaC2
CaC2 + 2H2O → C2H2 + Ca(OH)2
2. Điều kiện phản ứng điều chế C2H2
Không có
3. Hiện tượng phản ứng điều chế C2H2
Hiện tượng: Chất rắn màu đen canxi cacbua (CaC2) bị hòa tan và sinh ra khí axetilen (C2H2) làm sủi bọt dung dịch.
4. Bản chất của CaC2 (Canxi cacbua) trong phản ứng
Phản ứng là cơ sở của việc sản xuất axetilen công nghiệp và cũng là công dụng chính của CaC2.
5. Điều chế axetilen
5.1. Điều chế axetilen trong phòng thí nghiệm
Cách tiến hành
Cho vài mẩu nhỏ canxi cacbua vào ống nghiệm đã đựng 1ml nước và đậy nhanh bằng nút có ống dẫn khí đầu vuốt nhọn.
Đốt khí sinh ra ở đầu ống vuốt nhọn.
Phương trình phản ứng
CaC2 + 2H2O → C2H2 + Ca(OH)2
Tuy nhiên, phương pháp điều chế này sinh ra nhiều nhiệt, hàm lượng Canxi Cacbua cũng chứa nhiều tạp chất nên phương pháp này mang lại Axetilen không tinh khiết lắm.
5.2. Điều chế axetilen trong công nghiệp
Trong công nghiệp người ta điều chế axetilen bằng cách cho canxi cacbua tác dụng với nước
CaC2 + 2H2O → C2H2 + Ca(OH)2
Điều chế axetilen từ (Ag2C2)
2HCl + Ag2C2 → 2AgCl + C2H2
Điều chế axetilen từ etilen
Sử dụng dẫn xuất halogen của C2H4để điều chế C2H2:
CH2=CH2 + Cl2→ Cl-CH2-CH2-Cl
Cl-CH2-CH2-Cl + 2NaOH → CH = CH + 2NaCl + H2O
6. Ứng dụng của axetilen
Axetilen được dùng làm nguyên liệu sản xuất các monome, rồi từ đó chế tạo nên các polime khác, sợi tổng hợp, cao su, muội than,…
Axetilen dùng làm nhiên liệu trong đèn xì oxi-axetilen (khi được tác dụng với oxy) để hàn hay cắt kim loại.
Axetilen dùng để sản xuất axit axetic, rượu etylic…
7. Bài tập vận dụng
Câu 1. Cho chất axetilen (C2H2) và benzen (C6H6), hãy chọn nhận xét đúng trong các nhận xét sau:
A. Hai chất đó giống nhau về công thức phân tử và khác nhau về công thức đơn giản nhất
B. Hai chất đó khác nhau về công thức phân tử và giống nhau về công thức đơn giản nhất.
C. Hai chất đó khác nhau về công thức phân tử và khác nhau về công thức đơn giản nhất.
D. Hai chất đó có cùng công thức phân tử và cùng công thức đơn giản nhất
Lời giải:
Đáp án: B
Giải thích:
Công thức đơn giản nhất của axetilen: CH
Công thức đơn giản nhất của benzen: CH
=> 2 chất khác nhau về công thức phân tử và giống nhau về công thức đơn giản nhất
Câu 2. Phát biểu nào sau được dùng để định nghĩa công thức đơn giản nhất của hợp chất hữu cơ?
A. Công thức đơn giản nhất là công thức biểu thị số nguyên tử của mỗi nguyên tố trong phân tử.
B. Công thức đơn giản nhất là công thức biểu thị tỉ lệ tối giản về số nguyên tử của các nguyên tố trong phân tử.
C. Công thức đơn giản nhất là công thức biểu thị tỉ lệ phần trăm số mol của mỗi nguyên tố trong phân tử.
D. Công thức đơn giản nhất là công thức biểu thị tỉ lệ số nguyên tử C và H có trong phân tử.
Lời giải:
Đáp án: B
Câu 3. Dãy các chất nào sau đây có cùng công thức đơn giản nhất?
A. CH4, C2H6, C3H8.
B. C2H4O2, C6H12O6, C3H6O3.
C. C6H12O6, C4H8O2, C3H6O.
D. CH4, C2H4, C3H4.
Lời giải:
Đáp án: B
Giải thích:
Dãy các công thức phân tử C2H4O2, C6H12O6, C3H6O3 đều có thể viết thành (CH2O)n
⟹ Dãy B gồm các chất có cùng công thức đơn giản nhất là CH2O.
Câu 4. Nhận định nào sau đây là sai?
A. Các hiđrocacbon thơm đều là chất lỏng hoặc chất rắn ở điều kiện thường
B. Nguồn cung cấp benzen chủ yếu từ nhựa than đá.
C. Oxi hóa không hoàn toàn ancol bậc I được anđehit.
D. Phenol tan tốt trong nước lạnh.
Lời giải:
Đáp án: D
Câu 5. Tính chất vật lý của axetilen là
A. chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
B. chất khí không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. chất khí không màu, không mùi, tan tốt trong nước, nhẹ hơn không khí .
D. chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Lời giải:
Đáp án: B
Câu 6: Phản ứng nào trong các phản ứng sau không tạo ra axetilen?
A. Ag2C2 + HCl →
B. CH4
C. Al4C3 + H2O→
D. CaC2 + H2O→
Lời giải:
Đáp án: C
Câu 7: Axetilen tham gia phản ứng cộng H2O (xúc tác HgSO4, thu được sản phẩm hữu cơ là:
A. C2H4(OH)2
B. CH3CHO
C. CH3COOH
D. C2H5OH
Lời giải:
Đáp án: B
Câu 8. Trùng hợp eten, sản phẩm thu được có cấu tạo là:
A. (-CH2=CH2-)n
B. (-CH2-CH2-)n
C. (-CH=CH-)n.
D. (-CH3-CH3-)n
Lời giải:
Đáp án: B
Giải thích:
Trùng hợp etilen CH2=CH2 thu được poli etilen (-CH2-CH2-)n
Câu 9. Oxi hóa etilen bằng dung dịch KMnO4 thu được sản phẩm là:
A. MnO2, C2H4(OH)2, KOH.
B. C2H5OH, MnO2, KOH.
C. C2H4(OH)2, K2CO3, MnO2.
D. K2CO3, H2O, MnO2.
Lời giải:
Đáp án: A
Giải thích:
Phương trình hóa học:
3CH2=CH2 + 2KMnO4 + 4H2O → 3CH2OH-CH2OH + 2MnO2 + 2KOH.
Câu 10: Khí axetilen không có tính chất hóa học nào sau đây?
A. Phản ứng cộng với dung dịch brom.
B. Phản ứng cháy với oxi.
C. Phản ứng cộng với hiđro.
D. Phản ứng thế với clo ngoài ánh sáng.
Lời giải:
Đáp án: D
Giải thích:
Khí axetilen không có phản ứng thế với clo ngoài ánh sáng.
Câu 11. Etilen có các tính chất hóa học sau:
A. Tham gia phản ứng cộng, phản ứng trùng hợp, phản ứng với thuốc tí và phản ứng cháy.
B. Chỉ tham gia phản ứng thế và phản ứng với dung dịch thuốc tím.
C. Chỉ tham gia phản ứng cháy.
D. Chỉ tham gia phản ứng cộng, phản ứng trùng hợp, không tham gia phản ứng cháy.
Lời giải:
Đáp án: A
Câu 12. Đốt cháy V lít etilen thu được 3,6 g hơi nước. Biết rằng oxi chiếm 20% thể tích không khí. Vậy thể tích không khí ở đktc cần dùng là:
A. 336 lít
B. 3,36 lít.
C. 33,6 lít
D. 0,336 lít.
Lời giải:
Đáp án: C
Giải thích:
Số mol nước là: nH2O = 3,6/18 = 0,2 mol
Phương trình phản ứng hóa học
C2H4 + 3O2 2CO2 + 2H2O
0,3 mol ← 0,2 mol
=> VO2 = 0,3.22,4 = 6,72 lít
Vì O2 chiếm 20% thể tích không khí => Vkhông khí = VO2/20% = 33,6 lít
Câu 13. Dẫn m gam hỗn hợp gồm metan và etilen đi qua dung dịch nước brom thì thấy lượng brom tham gia phản ứng là 8 gam. Khí bay ra được đốt cháy hoàn toàn và dẫn sản phẩm cháy đi qua dung dịch Ba(OH)2 dư thì thu được 29,55 gam kết tủa. Giá trị của m là:
A. 4 gam
B. 5 gam
C. 3,8 gam
D. 2,2 gam
Lời giải:
Đáp án: D
Giải thích:
nCO2 = nBaCO3 = 29,55/197 = 0,15 (mol)
Phương trình hóa học
C2H4 + Br2 → C2H4Br2
0,05 → 0,05
nBr2 = 8/160 = 0,05 (mol)
⇒ nCH4+ 2nC2H4 = nCO2
⇔ nCH4 + 0,05.2 = 0,15 (mol) => nCH4 = 0,05 (mol)
mkhi = mCH4 + mC2H4⇔ mkhi= 0,05.16 + 0,05.28 = 2,2 (g)
Câu 14: Phương pháp hiện đại để điều chế axetilen hiện nay là
A. nhiệt phân etilen ở nhiệt độ cao.
B. nhiệt phân benzen ở nhiệt độ cao.
C. nhiệt phân canxi cacbua ở nhiệt độ cao.
D. nhiệt phân metan ở nhiệt độ cao.
Lời giải:
Đáp án: D
Câu 15: Cho một loại đất đèn chứa 80%CaC2 nguyên chất vào một lượng nước dư, thu được 4,48 lít khí (đktc). Khối lượng đất đèn đem dùng là:
A. 12,8 gam
B. 10,24 gam
C. 16 gam
D. 17,6 gam
Lời giải:
Đáp án: C
Giải thích:
Số mol của etilen là: nC2H2 = 4,48 / 22,4 = 0,2 (mol)
Phương trình phản ứng
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 0,2
mCaC2 = 0,2 . 64 = 12,8 (gam)
mđất đèn = 12,8 / 80 .100 = 16 (gam)
Câu 16. Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là:
A. 0,05 và 0,1.
B. 0,12 và 0,03.
C. 0,1 và 0,05.
D. 0,03 và 0,12.
Lời giải:
Đáp án: A
Giải thích:
Khối lượng bình brom tăng = khối lượng etilen phản ứng
=> metilen = 2,8 gam => netilen = 2.8/28 = 0,1 mol
=> netan = 0,15 – 0,1 = 0,05 mol
Xem thêm các phương trình phản ứng hóa học khác:
C2H2 + AgNO3 + NH3 → C2Ag2 + NH4NO3
C3H4 + AgNO3 + NH3 → C3H3Ag + NH4NO3
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
