CaO + H2O → Ca(OH)2 | CaO ra Ca(OH)2
CaO + H2O → Ca(OH)2 là phản ứng hóa hợp. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng CaO + H2O → Ca(OH)2
1. Phương trình phản ứng CaO ra Ca(OH)2
CaO + H2O → Ca(OH)2
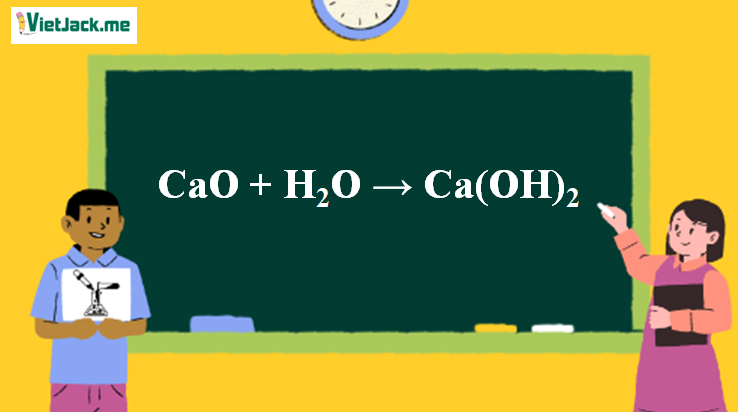
2. Điều kiện phản ứng xảy ra giữa CaO và H2O
Nhiệt độ thường.
3. Bản chất của CaO (Canxi oxit) trong phản ứng
CaO là một xit bazo tan tác dụng với nước tạo ra bazo, làm đổi màu quỳ tím thành xanh. (Chú ý: Đây cũng là 1 trong những tính chất quan trọng để nhận biết oxit bazo tan)
4. Mở rộng kiến thức về CaO
4.1. Tính chất vật lí & nhận biết
- Tính chất vật lí: CaO là chất rắn có dạng tinh thể màu trắng, là một chất ăn da và có tính kiềm.
- Nhận biết: Đem hòa tan bari oxit vào nước, tan tốt trong nước, tỏa nhiệt mạnh, sinh ra dung dịch hơi vẩn đục.
4.2. Tính chất hóa học
- Mang đầy đủ tính chất hóa học của oxit bazơ.
Tác dụng với nước:
CaO + H2O → Ca(OH)2
Tác dụng với axit:
CaO + 2HCl → CaCl2 + H2O
CaO + 2HNO3 → Ca(NO3)2 + H2O
Tác dụng với oxit axit:
CaO + CO2 → CaCO3
4.3. Điều chế
Canxi oxit thông thường được sản xuất bằng cách phân hủy bởi nhiệt (nung nóng) các loại vật liệu tự nhiên như đá vôi là khoáng chất chứa canxi cacbonat (CaCO3)
CaCO3 -to→ CaO + CO2
5. Ứng dụng của CaO
Trong nông nghiệp: Phân bón vôi làm tăng hiệu quả. Khi đất nhiễm axit, ta cần nâng cao độ pH của đất, nâng cao hàm lựơng canxi và magiê, đẩy mạnh hoạt động vi sinh, tăng tỷ lệ phát hành từ đất của vật chất hữu cơ và các yếu tố dinh dưỡng.
Ngành công nghiệp xây dựng: Vôi được sử dụng trong sản xuất gạch vôi silic, cách điện và vật liệu xây dựng. Vôi cũng được sử dụng trong vữa đặt gạch và làm cho các bức tường. Ngoài ra, vôi cũng được thêm vào bê tông và vữa để cải thiện hiệu suất của công trình xây dựng.
Công nghiệp thực phẩm: Vôi là một thành phần trong baking soda và giúp giữ trái cây và rau tươi.
Khai thác kim loại công nghiệp: Vôi còn được sử dụng vào khai thác kim lọai như đồng, thủy ngân, kẽm, niken, vàng,chì và bạc.
Sản xuất giấy: Các nhà sản xuất sử dụng vôi để phục hồi soda ăn da trong quá trình chuyển đổi của các mẩu gỗ để sản xuất bột giấy.
Kiểm soát ô nhiễm: vôi và đá vôi được sử dụng để hấp thụ lưu huỳnh đioxit từ khí thải trong smelters và các nhà máy phát điện.
Xử lý nước: bao gồm nước thải công nghiệp và nước sinh hoạt. Vôi trung hòa axit tạo ra chất thải trong ngành công nghiệp do đó cản trở sự ăn mòn và bảo vệ môi trường tự nhiên.. Vôi cũng loại bỏ silic, mangan, florua, sắt và các tạp chất khác trong nước. Nó làm mềm nước bằng cách loại bỏ độ cứng bicarbonate và tẩy uế chống lại vi khuẩn.
6. Tính chất hóa học của H2O
6.1. Nước tác dụng với kim loại
Ở điều kiện thường, nước có thể phản ứng với các kim loại mạnh như Li, Ca, Na, K, Ba,… để tạo thành dung dịch Bazo và khí Hidro.
H2O + Kim loại → Bazơ + H2↑
2M + 2nH2O → 2M(OH)n + nH2↑
2Na + 2H2O → 2NaOH + H2
2K + 2H2O → 2KOH + H2
Ca + 2H2O → Ca(OH)2 + H2
Ba + 2H2O → Ba(OH)2 + H2
Đặc biệt, một số kim loại trung bình như Mg, Zn, Al, Fe,…phản ứng được với hơi nước ở nhiệt độ cao tạo ra oxit kim loại và hidro. Bên cạnh đó, kim loại Mg tan rất chậm trong nước nóng.
6.2. Nước tác dụng với oxit bazo
Nước tác dụng với một số oxit bazo như Na2O, CaO , K2O,… tạo thành dung dịch bazo tương ứng. Dung dịch bazo làm cho quỳ tím hóa xanh.
H2O + Oxit bazơ → Bazơ
Na2O + H2O → 2NaOH
Li2O + H2O→ 2LiOH
K2O + H2O→ 2KOH
CaO + H2O → Ca(OH)2
6.3. Nước tác dụng với oxit axit
Nước tác dụng với oxit axit tạo thành axit tương ứng. Dung dịch axit làm quỳ tím hóa đỏ.
H2O + Oxit axit → Axit
CO2 + H2O → H2CO3
SO2 + H2O → H2SO3
P2O5 + 3H2O → 2H3PO4
SO3 + H2O → H2SO4
N2O5 + H2O → 2HNO3
7. Bài tập vận dụng
Câu 1. Oxit nào sau đây tan được trong nước tạo thành dung dịch làm quỳ hóa xanh.
A. CO2
B. FeO
C. CaO
D. N2O5
Lời giải:
Đáp án: C
Câu 2. Oxit bazo nào sau đây được dùng để làm khô nhiều nhất?
A. FeO
B. CuO
C. CaO
D. MgO
Lời giải:
Đáp án: C
Câu 3. Để làm sạch khí O2 từ hỗn hợp khí gồm CO2 và O2, có thể dung chất nào dưới đây?
A. H2SO4
B. Ca(NO3)2
C. Ca(OH)2
D. NaHSO3
Lời giải:
Đáp án: C
Câu 4. Canxi oxit (vôi sống) được dùng để khử chua đất trông trọt, xử lí nước thải của nhiều nhà máy hóa chất,... Đó là do tính chất nào dưới đây
A. CaO tác dụng với H2O tạo thành dung dịch bazo
B. CaO tác dụng với axit có trong đất, trong nước thải
C. CaO tác dụng với CO2
D. CaO là chất rắn dễ hút ẩm
Lời giải:
Đáp án: B
Câu 5. Để khử chua cho đất người ta thường sử dụng chất nào sau đây:
A. Muối ăn
B. thạch cao
C. phèn chua
D. vôi sống
Lời giải:
Đáp án: D
Giải thích:
Để khử chua cho đất người ta thường sử dụng vôi sống. Vì vôi có tính kiềm sẽ trung hòa axit trong đất.
Câu 6. Nội dung nào sau đây về canxi hiđroxit là không đúng ?
A. Canxi hiđroxit còn gọi là vôi tôi, là chất rắn màu trắng, tan rất nhiều trong nước.
B. Nước vôi trong là dung dịch Ca(OH)2.
C. Canxi hiđroxit được sử dụng trong 1 số ngành công nghiệp như: sản xuất amoniac, clorua vôi, vật liệu xây dựng,...
D. Canxi hiđroxit là một bazơ mạnh.
Lời giải:
Đáp án: A
Câu 7. Dẫn từ từ CO2 đến dư vào dung dịch Ca(OH)2, hiện tượng quan sát được là
A. có kết tủa, lượng kết tủa tăng dần, kết tủa không tan
B. không có hiện tượng gì trong suốt quá trình thực hiện
C. lúc đầu không thấy hiện tượng, sau đó có kết tủa xuất hiện
D. có kết tủa, lượng kết tủa tăng dần, sau đó kết tủa tan
Lời giải:
Đáp án: D
Giải thích:
Dẫn từ từ CO2 đến dư vào dung dịch Ca(OH)2 xảy ra phản ứng:
CO2+ Ca(OH)2 → CaCO3 + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
Hiện tượng quan sát được: Dung dịch xuất hiện kết tủa trắng tăng dần đến cực đại, sau đó kết tủa tan dần đến hết.
Câu 8. Dãy nào sau đây gồm các chất đều là oxit bazơ?
A. Al2O3, CaO, MgO, Na2O, CO.
B. SO2, CO2, CO, P2O5.
C. MgO, NaOH, H2O, Al2O3 .
D. FeO, CaO, MgO, Na2O.
Lời giải:
Đáp án: D
Xem thêm các phương trình phản ứng hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
