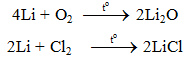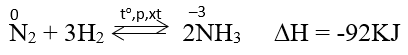Li + N2 → Li3N l Li ra Li3N
Li + N2 → Li3N là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng Li + N2 → Li3N
1. Phản ứng hoá học
6Li + N2 → 2Li3N
2. Điều kiện phản ứng
Nhiệt độ 200-250oC; áp suất
3. Cách thực hiện phản ứng
Cho Liti tác dụng với khí nitơ
4. Hiện tượng nhận biết phản ứng
Li cháy sáng mạnh trong khí nitơ.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của Li (Liti)
- Trong phản ứng trên Li là chất khử.
- Li tham gia phản ứng được với các chất khí trơ nhưng điều kiện khó khăn hơn.
5.2. Bản chất của N2 (Nito)
- Trong phản ứng trên N2 là chất oxi hóa.
- Ở nhiệt độ cao, N2 thể hiện tính oxi hóa khi tác dụng với một số kim loại hoạt động mạnh tạo thành nitrua kim loại.
6. Tính chất hóa học của Li
Liti là kim loại kiềm có tính khử rất mạnh.
Li → Li+ + 1e
6.1. Tác dụng với phi kim
6.2. Tác dụng với axit
Liti dễ dàng khử ion H+ (hay H3O+) trong dung dịch axit loãng (HCl, H2SO4 loãng...) thành hidro tự do.
2Li + 2HCl → 2LiCl + H2.
2Li + H2SO4 → Li2SO4 + H2.
6.3. Tác dụng với nước
Li tác dụng chậm với nước tạo thành dung dịch kiềm và giải phóng khí hidro.
2Li + 2H2O → 2LiOH + H2.
6.4. Tác dụng với hidro
Liti tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành Liti hidrua.
2Li (lỏng) + H2 (khí) → 2LiH (rắn)
7. Tính chất vật lý của Li
- Kim loại kiềm. Trắng – bạc. Nhẹ nhất trong các kim loại, mềm, dễ nóng chảy.
- Có khối lượng riêng là 0,534 g/cm3; có nhiệt độ nóng chảy là 180,50C và sôi ở 1336,60C
8. Tính chất hoá học của N2
- Nitơ có các số oxi hoá: -3, 0, +1, +2, +3, +4, +5.
- N2 có số oxi hoá 0 nên vừa thể hiện tính oxi hoá và tính khử.
- Nitơ có EN N = 946 kJ/mol, ở nhiệt độ thường nitơ khá trơ về mặt hóa học nhưng ở nhiệt độ cao hoạt động hơn.
- Nitơ thể hiện tính oxi hóa và tính khử, tính oxi hóa đặc trưng hơn.
8.1. Tính oxi hoá
Phân tử nitơ có liên kết ba rất bền, nên nitơ khá trơ về mặt hóa học ở nhiệt độ thường.
a. Tác dụng với hidro
Ở nhiệt độ cao, áp suất cao và có xúc tác. Nitơ phản ứng với hidro tạo amoniac.
b. Tác dụng với kim loại
- Ở nhiệt độ thường nitơ chỉ tác dụng với liti tạo liti nitrua: 6Li + N2 → 2Li3N.
- Ở nhiệt độ cao, nitơ tác dụng với nhiều kim loại: 3Mg + N2 → Mg3N2 (magie nitrua).
Lưu ý: Các nitrua dễ bị thủy phân tạo NH3.
Nitơ thể hiện tính oxi hoá khi tác dụng với nguyên tố có độ âm điện nhỏ hơn.
8.2. Tính khử
Ở nhiệt độ cao (3000 ºC) Nitơ phản ứng với oxi tạo nitơ monoxit.
9. Câu hỏi vận dụng
Câu 1. Khi cho li tác dụng với khí N2. Điều kiện để phản ứng xảy ra là
A. Nhiệt độ B. Áp suất C. Xúc tác D. A và B
Lời giải:
Đáp án: D
Câu 2. Cho m g Li tác dụng vừa đủ với 3,36 lít khí N2 (đktc). Khối lượng liti tham gia phản ứng là
A. 1,05 g B. 0,7 g C. 6,3 g D. 0,63 g
Lời giải:
Đáp án: C
6Li + N2 → 2Li3N
nLi = 6.nN2 = 0,9 mol ⇒ mLi = 0,9.7 = 6,3 g
Câu 3. Cho li tác dụng với V lít khi Nito thu được 3,5 g chất rắn màu trắng. Giá trị của V là
A. 2,24 lít B. 1,12 lít C. 3,36 lít D. 4,48 lít
Lời giải:
Đáp án: B
6Li + N2 → 2Li3N
nN2 = nLi3N/2 = 0,05 mol ⇒ VN2 = 0,05.22,4 = 1,12 lít
Xem thêm các phương trình phản ứng hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)