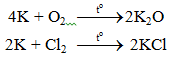K + Cu(NO3)2 + H2O → KNO3 + H2 + Cu(OH)2 l K ra KNO3
K + Cu(NO3)2 + H2O → KNO3 + H2 + Cu(OH)2 là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng K + Cu(NO3)2 + H2O → KNO3 + H2 + Cu(OH)2
1. Phản ứng hóa học
2K + Cu(NO3)2 + 2H2O → 2KNO3 + H2 + Cu(OH)2
2. Điều kiện phản ứng
Không cần điều kiện
3. Cách thực hiện phản ứng
Cho kali tác dụng với dung dịch muối đồng (II) nitrat
4. Hiện tượng nhận biết phản ứng
K tan dần trong dung dịch muối đồng (II) nitrat, có kết tủa màu xanh tạo thành và có khí thoát ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K (Kali)
- Trong phản ứng trên K là chất khử.
- K là chất khử mạnh, K tham gia phản ứng với các dung dịch muối sẽ tham gia phản ứng với nước trước tạo hidroxit.
5.2. Bản chất của Cu(NO3)2 (Đồng nitrat)
Cu(NO3)2 mang tính chất hóa học của muối nên tác dụng với dung dịch bazơ.
6. Tính chất hoá học của K
Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
6.1. Tác dụng với phi kim
6.2. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
6.3. Tác dụng với nước
K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
6.4. Tác dụng với hidro
Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
7. Mở rộng kiến thức về Cu(NO3)2
7.1. Định nghĩa
- Định nghĩa: Đồng (II) nitrat là một hợp chất vô cơ có bề ngoài là một chất rắn tinh thể màu xanh da trời.Muối khan của chất này tạo thành các tinh thể xanh lá cây-xanh da trời.
- Công thức phân tử: Cu(NO3)2
7.2. Tính chất vật lí
Là chất rắn, có màu xanh da trời. Thăng hoa trong chân không ở nhiệt độ 150-200 độC.
7.3. Tính chất hóa học
Có tính chất hóa học của muối.
Tác dụng với dung dịch bazơ:
Cu(NO3)2 + 2KOH → Cu(OH)2 + 2KCl
Cu(NO3)2 + Ba(OH)2 → Cu(OH)2 + Ba(NO3)2
7.4. Điều chế
Cho kim loại đồng tác dụng với dung dịch HNO3
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO +4H2O
7.5. Ứng dụng
Đối với màu sắc hấp dẫn của đồng nitrat, muối này được sử dụng làm phụ gia trong gốm sứ, trên bề mặt kim loại, trong một số pháo hoa và cả trong ngành dệt như một chất gắn màu.
Nó là một nguồn đồng ion tốt cho nhiều phản ứng, đặc biệt là những phản ứng xúc tác hữu cơ. Nó cũng tìm thấy việc sử dụng tương tự như các nitrat khác, như là thuốc diệt nấm, thuốc diệt cỏ hoặc làm chất bảo quản gỗ..
Một ứng dụng chính và sáng tạo nhất của nó là tổng hợp các chất xúc tác CuO, hoặc các vật liệu có phẩm chất nhạy sáng.
Nó cũng được sử dụng như một thuốc thử cổ điển trong các phòng thí nghiệm giảng dạy để hiển thị các phản ứng bên trong các tế bào bay hơi.
8. Câu hỏi vận dụng
Câu 1. Khi cho kim loại K vào dung dịch Cu(NO3)2 thu được 2,24 lít khí đktc. Khối lượng kim loại K tham gia phản ứng là:
A. 3,9 g B. 0,39 g
C. 7,8 g D. 0,78 g
Lời giải:
Đáp án C
Phương trình hóa học: 2K + Cu(NO3)2 + 2H2O → 2KNO3 + H2 + Cu(OH)2
nK = 2nH2 = 2.0,1 = 0,2 mol ⇒ mK = 39.0,2 = 7,8 g
Câu 2. Khi cho K tác dụng với dung dịch muối đồng(II)nitrat thu được khí X. Dẫn khí X qua các chất sau: ZnO; CuO; Fe; Fe2O3. X phản ứng được với bao nhiêu chất trên?
A. 1 B. 2
C. 3 D. 4
Lời giải:
Đáp án B
Phương trình hóa học: 2K + Cu(NO3)2 + 2H2O → 2KNO3 + H2 + Cu(OH)2
Khí X là khí H2; H2 phản ứng được với các oxit kim loại nung nóng đứng sau Al
Câu 3. Cho kim loại K tác dụng vừa đủ với 100 ml dung dịch Cu(NO3)2 0,1 M thu được m g kết tủa. Giá trị của m là:
A. 0,98 g B. 4,9 g
C. 2,45 g D. 0,49 g
Lời giải:
Đáp án D
Phương trình phản ứng: 2K + Cu(NO3)2 + 2H2O → 2KCl + H2 + Cu(OH)2
nCu(OH)2 = nK/2 = 0,01/2 = 0,005 mol ⇒ mCu(OH)2 = 0,005.98 = 0,49 g
Xem thêm các phương trình phản ứng hóa học khác:
K + Fe(NO3)2 + H2O → KNO3 + H2 + Fe(OH)2
K + Al(NO3)3 + H2O → KNO3 + H2 + Al(OH)3
K + Zn(NO3)2 + H2O → KNO3 + H2 + Zn(OH)2
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)