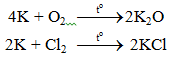K + HF → KF + H2 l K ra KF l K ra H2
K + HF → KF + H2 là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng K + HF → KF + H2
1. Phản ứng hóa học
2K + 2HF → 2KF + H2
2. Điều kiện phản ứng
Không cần điều kiện
3. Cách thực hiện phản ứng
Cho K tác dụng với axit HF tạo muối.
4. Hiện tượng nhận biết phản ứng
K tan dần trong dung dịch HF và có khí thoát ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K (Kali)
- Trong phản ứng trên K là chất khử.
- K là kim loại kiềm có tính khử rất mạnh, K tham gia phản ứng được với các axit.
5.2. Bản chất của HF (Axit flohidric)
- Trong phản ứng trên HF là chất oxi hoá,
- HF là một axit yếu nên nó có tất cả các tính chất của một axit.
6. Tính chất hoá học của K
Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
6.1. Tác dụng với phi kim
6.2. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
6.3. Tác dụng với nước
K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
6.4. Tác dụng với hidro
Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
7. Tính chất vật lí của Kali
- Kali là kim loại nhẹ thứ hai sau liti, là chất rắn rất mềm, dễ dàng cắt bằng dao và có màu trắng bạc.
- Kali bị ôxi hóa rất nhanh trong không khí và phải được bảo quản trong dầu mỏ hay dầu lửa.
- Có khối lượng riêng là 0,863 g/cm3; có nhiệt độ nóng chảy là 63,510C và sôi ở 7600C.
8. Tính chất hoá học của HF
Axit HF là axit yếu vì vậy nó có đầy đủ các tính chất của một axit.
8.1. Tác dụng với phi kim
O2 + HF → HFO2
2I2 + HF → HFI4
2Br2 + HF → HFBr4
8.2. Tác dụng với oxit
Tính chất đặc biệt của axit HF là tác dụng với SiO2 có trong thành phần thuỷ tinh.
→ Do đó không dùng chai lọ thuỷ tinh để đựng dung dịch axit HF.
SiO2 + 4HF → 2H2O + SiF4
SO3 + HF → HSO3F
8.3. Tác dụng với nước
2H2O + HF → 2H2 + HFO2
H2O + HF + AsF5 → HAsF6.H2O
8.4. Tác dụng với bazo
NaOH + HF → H2O + NaF
Ca(OH)2 + 2HF → CaF2 + 2H2O
8.5. Tác dụng với muối
NaF + HF → NaHF2
CuCl + HF → HCl + CuF
9. Câu hỏi vận dụng
Câu 1. K tác dụng lần lượt các chất dưới đây: Glucozo, HF; H3PO4; H2SO4; Fe, K. Số phản ứng xảy ra là:
A. 1 B. 2
C. 3 D. 4
Lời giải:
Đáp án D
K + C6H12O6 → C6H6(OK)6 + 3H2
6K + 2H3PO4 → 2K3PO4 + 3H2
2K + 2H2SO4 → 2K2SO4 + H2
2K + 2HF → 2KF + H2
Câu 2. Cho Na tác dụng với 100 mldung dịch axit HF 0,2 M thu được muối và V lít khi đktc. Giá trị của V là
A. 1,12 lít B. 4,48 lít
C. 0,224 lít D. 5,6 lít
Lời giải:
Đáp án C
Phương trình phản ứng: 2Na + 2HF → 2NaF + H2
nH2 = nNa/2 = 0,02/2 = 0,01 mol ⇒ VH2 = 0,01.22,4 = 0,224 lít
Câu 3. Cho m g K tác dụng với dung dịch HF dư thu được 5,8 g muối. Giá trị của m là:
A. 1,85 g B. 3,9 g
C. 7,8 g D. 0,78 g
Lời giải:
Đáp án B
Phương trình phản ứng: 2K + 2HF → 2KF + H2
nK = nKF = 0,1 mol ⇒ mKF = 0,1.39 = 3,9 g
Xem thêm các phương trình phản ứng hóa học khác:
K + CuSO4 + H2O → K2SO4 + H2 + Cu(OH)2
K + FeSO4 + H2O → K2SO4 + H2 + Fe(OH)2
K + Al2(SO4)3 + H2O → K2SO4 + H2 + Al(OH)3
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)