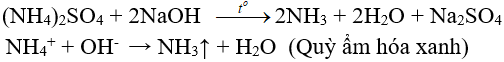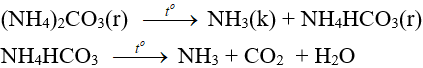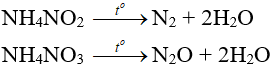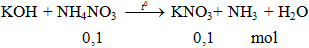KOH + NH4NO3 → KNO3 + NH3 + H2O l KOH ra KNO3
KOH + NH4NO3 → KNO3 + NH3 + H2O là phản ứng trao đổi. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng KOH + NH4NO3 KNO3+ NH3 + H2O

1. Phản ứng hóa học
KOH + NH4NO3 KNO3+ NH3 + H2O
2. Điều kiện phản ứng
Phản ứng xảy ra khi đun nóng.
3. Cách thực hiện phản ứng
Đun nóng muối NH4NO3 với KOH.
4. Hiện tượng nhận biết phản ứng
Có khí không màu, mùi khai bay ra.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của KOH (Kali hidroxit)
KOH là một bazo mạnh tác dụng được với NH4NO3.
5.2. Bản chất của NH4NO3 (Amoni nitrat)
NH4NO3 có thể tác dụng với các bazo như KOH, NaOH, Ba(OH)2,... giải phóng amoniac.
6. Tính chất hoá học của KOH
KOH là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
6.1. Tác dụng với oxit axit
Ở điều kiện nhiệt độ phòng, KOH tác dụng với SO2, CO2,...
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
6.2. Tác dụng với axit
-
Tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
-
Tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
6.3. Tác dụng với kim loại
KOH tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới.
KOH + Na → NaOH + K
6.4. Tác dụng với muối
KOH tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
6.5. KOH điện li mạnh
KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion K+ và OH-
6.6. KOH phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính
KOH phản ứng được với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
6.7. Phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O
7. Tính chất vật lý của KOH
- Khối lượng riêng: 2.044 g/cm3
- Độ pH: 13
- Nhiệt độ sôi: 1.327oC (1.6000 K; 2.421 oF)
- Nhiệt độ nóng chảy: 406 oC (679 K; 763 oF)
- Độ hòa tan trong nước:7 g/ml (0 oC); 121 g/ml (25 oC); 178 g/ml (100 oC)
- Khả năng hòa tan chất khác: có thể được hòa tan trong alcohol, glycerol và không tan được trong ether.
8. Tính chất hoá học của muối amoni
8.1. Phản ứng thuỷ phân
Tạo môi trường có tính axit làm quỳ tím hoá đỏ.
NH4+ + HOH → NH3 + H3O+ (Tính axit)
8.2. Tác dụng với dung dịch kiềm
(nhận biết ion amoni, điều chế amoniac trong phòng thí nghiệm)
8.3. Phản ứng nhiệt phân
- Muối amoni chứa gốc của axit không có tính oxi hóa khi nung nóng bị phân hủy thành NH3.
NH4HCO3 (bột nở) được dùng làm xốp bánh.
- Muối amoni chứa gốc của axit có tính oxi hóa khi bị nhiệt phân cho ra N2, N2O.
- Nhiệt độ lên tới 500oC, ta có phản ứng:
2NH4NO3 → 2N2 + O2 + 4H2O
9. Câu hỏi vận dụng
Câu 1. Muối nào sau đây phản ứng với KOH không thu được amoniac?
A. NH4Cl. B. NH4NO3. C. (NH4)2SO4 . D. KNO3.
Lời giải:
KNO3 không phản ứng với KOH.
Đáp án D.
Câu 2. Hiện tượng xảy ra khi đun nóng muối NH4NO3 với KOH là
A. Có khí màu nâu đỏ bay ra.
B. Có khí mùi trứng thối thoát ra.
C. Có khí màu vàng lục, mùi xốc thoát ra.
D. Có khí mùi khai thoát ra.
Lời giải:
KOH + NH4NO3 
NH3 là khí có mùi khai.
Đáp án D.
Câu 3. Cho dung dịch KOH dư vào 100 ml NH4NO3 1 ml đun nóng nhẹ. Thể tích khí ở đktc thu được là
A. 1,12 lít. B. 2,24 lít. C. 3,36 lít. D. 4,48 lít
Lời giải:
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Xem thêm các phương trình hóa học khác:
KOH + (NH4)2SO4 → K2SO4 + NH3 + H2O
CH3COOCH3 + KOH → CH3COOK + CH3OH
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)