NaOH ⟶ H2O + Na + O2 | NaOH ra Na
NaOH ⟶ H2O + Na + O2 là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng: NaOH ⟶ H2O + Na + O2
1. Phương trình điện phân nóng chảy
4NaOH ⟶ 2H2O + 4Na + O2
2. Điều kiện xảy ra phản ứng
Nhiệt độ điện phân nóng chảy
3. Hiện tượng xảy ra sau phản ứng
Xuất hiện chất rắn màu trắng Natri (Na) và khí Oxi (O2) làm sủi bọt khí.
4. Tính chất hóa học của NaOH
NaOH Là một bazơ mạnh nó sẽ làm quỳ tím chuyển màu xanh, còn dung dịch phenolphtalein thành màu hồng. Một số phản ứng đặc trưng của Natri Hidroxit được liệt kê ngay dưới đây.
Phản ứng với axit tạo thành muối + nước:
NaOHdd + HCldd→ NaCldd + H2O
Phản ứng với oxit axit: SO2, CO2…
2 NaOH + SO2→ Na2SO3 + H2O
NaOH + SO2→ NaHSO3
Phản ứng với axit hữu cơ tạo thành muối và thủy phân este, peptit:
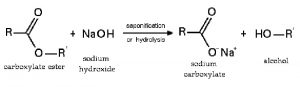
Phản ứng với muối tạo bazo mới + muối mới (điều kiện: sau phản ứng phải tạo thành chất kết tủa hoặc bay hơi):
2 NaOH + CuCl2→ 2NaCl + Cu(OH)2↓
Tác dụng với kim loại lưỡng tính:
2 NaOH + 2Al + 2H2O→ 2NaAlO2 + 3H2↑
2NaOH + Zn → Na2ZnO2 + H2↑
Tác dụng với hợp chất lưỡng tính:
NaOH + Al(OH)3 → NaAl(OH)4
2NaOH + Al2O3 → 2NaAlO2 + H2O
5. Tính chất vật lí của NaOH
Natri hydroxide là chất rắn không màu, hút ẩm mạnh, tan nhiều trong nước và tỏa nhiệt. Dung dịch natri hydroxide có tính nhờn, làm bục vải, giấy và ăn mòn da.
6. Bài tập vận dụng liên quan
Bài 1: NaOH có tính chất vật lý nào sau đây ?
A. Natri hiđroxit là chất rắn không màu, ít tan trong nước.
B. Natri hiđroxit là chất rắn không màu, hút ẩm mạnh, tan nhiều trong nước và tỏa nhiệt.
C. Natri hiđroxit là chất rắn không màu, hút ẩm mạnh và không tỏa nhiệt.
D. Natri hiđroxit là chất rắn không màu, không tan trong nước, không tỏa nhiệt.
Lời giải
NaOH có tính chất vật lí là: NaOH là chất rắn không màu, hút ẩm mạnh, tan nhiều trong nước và tỏa nhiệt.
Đáp án: B
Bài 2: Nếu rót 200 ml dung dịch NaOH 1M vào ống nghiệm đựng 100 ml dung dịch H2SO4 1M thì dung dịch tạo thành sau phản ứng sẽ:
A. Làm quỳ tím chuyển đỏ
B. Làm quỳ tím chuyển xanh
C. Làm dung dịch phenolphtalein không màu chuyển đỏ.
D. Không làm thay đổi màu quỳ tím.
Lời giải
Phương trình hóa học:
2NaOH + H2SO4 → Na2SO4 + 2H2O
Xét tỉ lệ:
=> NaOH và H2SO4 phản ứng vừa đủ với nhau
=> dung dịch thu được có môi trường trung tính => không làm thay đổi màu quỳ tím.
Đáp án: D
Bài 3: Có 2 dung dịch không màu là Ca(OH)2 và NaOH. Để phân biệt 2 dung dịch này bằng phương pháp hoá học dùng
A. HCl
B. CO2
C. phenolphtalein
D. nhiệt phân
Lời giải
Cho 2 dung dịch qua CO2, dd nào xuất hiện kết tủa trắng là Ca(OH)2, còn lại không có hiện tượng là NaOH
CO2 + Ca(OH)2→ CaCO3↓ + H2O
CO2 + NaOH → NaOH + H2O (xảy ra phản ứng nhưng không quan sát được hiện tượng, vì không có gì đặc trưng của phản ứng)
Đáp án: B
Bài 4: Để phân biệt hai dung dịch NaOH và Ba(OH)2 đựng trong hai lọ mất nhãn ta dùng thuốc thử:
A. Quỳ tím
B. HCl
C. NaCl
D. H2SO4
Lời giải
Để phân biệt NaOH và Ba(OH)2 ta dùng dung dịch H2SO4
NaOH không có hiện tượng gì còn Ba(OH)2 tạo kết tủa màu trắng
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
Đáp án: D
Bài 5: Dung dịch NaOH và dung dịch KOH không có tính chất nào sau đây?
A. Làm đổi màu quỳ tím và phenophtalein
B. Bị nhiệt phân hủy khi đun nóng tạo thành oxit bazơ và nước
C. Tác dụng với oxit axit tạo thành muối và nước
D. Tác dụng với axit tạo thành muối và nước
Lời giải
Dung dịch NaOH và dung dịch KOH không có tính chất : bị nhiệt phân hủy khi đun nóng tạo thành oxit bazơ và nước.
Vì NaOH và KOH đều là bazơ tan.
Đáp án: B
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
