C2H4 ra C2H5OH l C2H4 + H2O → C2H5OH l Etilen ra Ancol etylic
C2H4 + H2O → C2H5OH là phản ứng cộng. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng C2H4 + H2O → C2H5OH
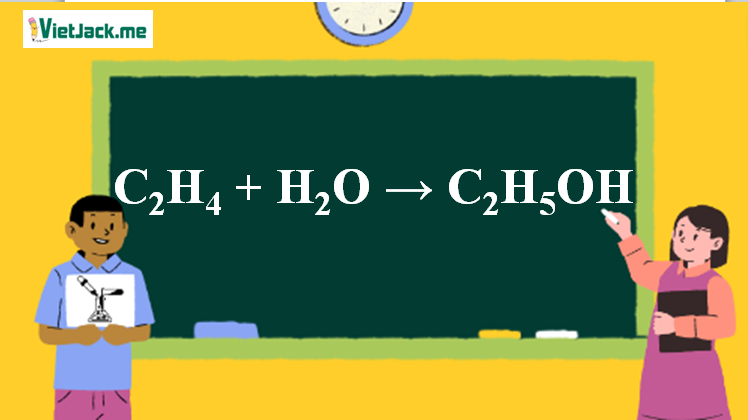
1. Phương trình hóa học C2H4 tác dụng với H2O
C2H4 + H2O C2H5OH
2. Điều kiện phản ứng xảy ra C2H4 ra C2H5OH
Xúc tác: H2SO4
Điều kiện khác: nhiệt độ cao.
3. Cách tiến hành thí nghiệm khi điều chế C2H4 ra C2H5OH
Sục khí C2H4 qua nước.
4. Bản chất của C2H4 (Etilen) trong phản ứng
Do có liên kết đôi nên ở nhiệt độ thích hợp và có xúc tác axit, etilen có thể cộng nước tạo thành etanol (C2H5OH).
5. Mở rộng điều chế etanol
Trong điều kiện không có oxy thì một số loại men rượu sẽ chuyển hóa đường tạo ra Ethanol và Cacbon dioxit CO2.
Phương trình điều chế như sau:
C6H12O6→ 2CH3CH2OH + 2CO2
Quá trình nuôi cấy men rượu theo các điều kiện để sản xuất rượu được gọi là ủ rượu. Men rượu có thể phát triển trong sự hiện diện của khoảng 20% rượu, nhưng nồng độ của rượu trong các sản phẩm cuối cùng có thể tăng lên nhờ chưng cất.
6. Tính chất hóa học của Etilen
Etilen tác dụng được với rất nhiều chất ở nhiều dạng khác nhau như: khí oxy, dung dịch brom, phản ứng trùng hợp của etilen C2H4, vân vân… C2H4 là một chất khí hoàn toàn không thể trơ về mặt hóa học.
Etilen có công thức cấu tạo: Viết gọn là: CH2=CH2
Trong phân tử etilen C2H4, có một liên kết đôi giữa hai nguyên tử cacbon, bao gồm 1 liên kết kém bền, dễ dàng đứt khi tiến hành phản ứng hóa học.
6.1. Etilen tác dụng với oxi
Khi đốt trong oxi, etilen cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
-
Etilen cháy hoàn toàn tạo ra CO2, H2O và tỏa nhiều nhiệt:
Phương trình hóa học
C2H4 + 3O2 → 2CO2+ 2H2O + Q
-
Etilen làm mất màu dung dịch KMnO4:
CH2=CH2+ 4H2O + 2KMnO4 → 3HO-CH2-CH2-OH + 2MnO2 + 2KOH
6.2. Etilen tác dụng brom dạng dung dịch
Phương trình hóa học:
CH2= CH2 + Br2 → Br – CH2 – CH2 – Br
6.3. Etilen tác dụn với H2O
Ở nhiệt độ thích hợp và có xúc tác axit, etilen có thể cộng nước
C2H4 + H2O C2H5OH
Với đặc điểm các chất liên kết đôi (tương tự etilen) dễ tham gia phản ứng cộng. Phân tử etilen kết hợp với nhau (còn gọi là phản ứng trùng hợp).
6.4. Phản ứng trùng ngưng
Các phân tử etilen kết hợp với nhau tạo ra chất có phân tử lượng rất lớn gọi là PolyEtiten hay còn gọi là PE
Phương trình phản ứng:
….+ CH2= CH2 + CH2= CH2 +….→ ….- CH2– CH2 – CH2– CH2-….
7. Tính chất vật lí của etilen
- Nhìn vào công thức cấu tạo của Etilen, có thể thấy đây là chất khí, không màu, không mùi, nhẹ hơn không khí (d= 28/29), ít tan trong nước. Etilen cũng rất dễ bắt cháy và có mùi ngọt nhẹ của xạ hương.
- Etilen tan ít trong nước nhưng tan nhiều trong ete và một số dung môi hữu cơ.
- Để nhận biết khí etilen, người ta dùng các phương pháp:
Dẫn khí etilen qua dung dịch brom (dung dịch có màu cam), quan sát thấy dung dịch brom bị mất màu.
Dẫn khí etilen qua dung dịch kali pemanganat, quan sát thấy dung dịch kali pemanganat bị mất màu.
8. Câu hỏi vận dụng
Câu 1. Công thức cấu tạo của rượu etylic là
A. CH2 – CH3 – OH.
B. CH3 – O – CH3.
C. CH2 – CH2 – OH2.
D. CH3 – CH2 – OH.
Lời giải:
Đáp án: D
Câu 2. Đốt cháy hoàn toàn m gam hỗn hợp 3 ancol đơn chức, thuộc cùng dãy đồng đẳng, thu được 7,612 lít khí CO2 (đktc) và 10,8 gam H2O. Giá trị của m là
A. 5,42.
B. 7,42.
C. 9,44.
D. 4,72.
Lời giải:
Đáp án: C
Giải thích:
Ta có: nCO2 = 0,34 mol; nH2O= 0,6 mol
Ta thấy: nH2O > nCO2 => 3 ancol là no, đơn chức, mạch hở
=> nancol= nH2O- nCO2= 0,6 – 0,34 = 0,26 mol
Đặt công thức chung của 3 ancol là CnH2n+2O
Ta có: nO(ancol)= nancol= 0,26 mol; nC(ancol) = nCO2= 0,34 mol;
nH(ancol)= 2.nH2O = 2.0,6 = 1,2 mol
Ta có: m= mO(ancol)+ mC(ancol) + mH(ancol )
= 0,26.16 + 0,34.12 + 1,2.1 = 9,44 gam
Câu 3. Cho 9,2 gam C2H5OH tác dụng với lượng dư Na sau phàn ứng hoàn toàn thu được V lít khí H2(đktc). Giá trị của m là
A. 2,24.
B. 3,36.
C. 4,48.
D. 6,72.
Lời giải:
Đáp án: C
Giải thích:
Ta có
nC2H5OH = 9,2 : 46 = 0,2 mol
Phương trình hóa học: 2C2H5OH + 2Na → 2C2H5ONa + H2
Theo phản ứng: 0,2 → 0,1 (mol)
=> n = 0,1 mol
Thể tích khí H2sinh ra là: VH2 = 0,1.22,4 = 2,24 lít
Câu 4. Hòa tan m gam ancol etylic (D= 0,8 gam/ml) vào 216 ml nước (D= 1 gam/ml) tạo thành dung dịch A. Cho A tác dụng với Na dư thu được 170,24 lit (đktc) khí H2. Dung dịch A có độ rượu bằng bao nhiêu?
A. 40o
B. 46o
C. 36o
D. 30o
Lời giải:
Đáp án: B
Giải thích:
Ta có phương trình hóa học
Na + C2H5OH → C2H5ONa + 1/2H2
x-------------x-----------x/2
Na + H2O → NaOH + 1/2H2
y---------y---------y/2
Theo bài ta có DH2O = 1 gam/ml
⇒ mH2O = 216 gam ⇒ nH2O = 216/18 = 12 mol = y
Mà nH2 = x/2 + y/2 = 170,24/22,4 = 7,6 mol
⇒ nC2H5OH = x = 3,2 mol
⇒ mC2H5OH = 3,2.46 = 147,2 gam
⇒ VC2H5OH = m/D = 147,2/0,8 = 184 ml
⇒ Vdd = 184 + 216 = 400 ml
⇒ D = 184.100/400 = 46o
Câu 5. Nhận xét nào sau đây là sai
A. Rượu etylic là chất lỏng, không màu
B. Rượu etylic tan vô hạn trong nước
C. Rượu etylic có thể hòa tan được iot
D. Rượu etylic nặng hơn nước
Lời giải:
Đáp án: D
Câu 6. Nhận định nào sau đây sai?
A. Có thể dùng glucoszơ để sản xuất rượu etylic.
B. Có thể dùng xenlulozơ đê sản xuất thuốc súng.
C. Phân biệt tinh bột và xenlulozơ bằng phản ứng tráng gương.
D. Phân biệt mantozơ và saccarozơ bằng phản ứng tráng gương.
Lời giải:
Đáp án: C
Câu 7. Có 4 dung dịch: Natri clorua, rượu etylic (C2H5OH), axit axetic (CH3COOH), kali sunfat đều có nồng độ 0,1 mol/l. Khả năng dẫn điện của các dung dịch đó tăng dần theo thứ tự nào trong các thứ tự sau:
A. NaCl < C2H5OH < CH3COOH < K2SO4
B. C2H5OH < CH3COOH < NaCl < K2SO4
C. C2H5OH < CH3COOH < K2SO4 < NaCl
D. CH3COOH < NaCl < C2H5OH < K2SO4
Lời giải:
Đáp án: B
Câu 8. Nhận xét đúng về khí etilen
A. Là chất khí không màu, có mùi hắc
B. Là chất khí không mùi, ít tan trong nước
C. Là chất khí nặng hơn không khí
D. Là chất khí không màu, ít tan trong nước
Lời giải:
Đáp án: D
Giải thích:
Cách giải nhanh bài tập này
Etilen là chất khí không màu , không mùi , ít tan trong nước , nhẹ hơn không khí.
Câu 9. Hãy chọn phát biểu đúng nhất về hoá học hữu cơ trong số các phát biểu sau:
A. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon.
B. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon, trừ cacbon (II) oxit, cacbon (IV) oxit, muối cacbonat, xianua, cacbua.
C.Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon, trừ cacbon (II) oxit, cacbon (IV) oxit.
D. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon trừ muối cacbonat.
Lời giải:
Đáp án: B
Giải thích:
Hợp chất hữu cơ là hợp chất của cacbon (trừ CO, CO2, HCN, muối cacbonat, muối xianua, muối cacbua…). Do đó hóa học hữu cơ là hóa học chuyên nghiên cứu các hợp chất của cacbon, trừ cacbon (II) oxit, cacbon (IV) oxit, muối cacbonat, xianua, cacbua.
Câu 10. Cho hỗn hợp các ankan sau: pentan (sôi ở 36oC), heptan (sôi ở 98oC), octan (sôi ở 126oC), nonan (sôi ở 151oC). Có thể tách riêng các chất đó bằng cách nào sau đây?
A. Kết tinh.
B. Chưng cất
C. Thăng hoa.
D. Chiết.
Lời giải:
Đáp án: B
Giải thích:
Vì nhiệt độ sôi của các chất chênh lệch nhau đáng kể và cao dần nên ta có thể dùng phương pháp chưng cất để tách các chất.
Câu 11. Ancol etylic có thể phản ứng được với các chất trong dãy nào dưới đây:
A. K, HBr, Fe.
B. Na, CuO, NaOH.
C. Na, CuO, HCl.
D. Na, MgCO3, HCl.
Lời giải:
Đáp án: C
Giải thích:
Ancol etylic phản ứng được với Na, CuO, HCl.
Phương trình hóa học xảy ra là:
CH3-CH2-OH + Na → CH3-CH2-ONa + ½ H2
CH3-CH2-OH + CuO → CH3-CHO + Cu + H2O
CH3-CH2-OH + HCl → CH3-CH2-Cl + H2O
Câu 12. Trong phân tử etilen giữa hai nguyên tử cacbon có
A. hai liên kết đôi.
B. một liên kết đôi.
C. một liên kết đơn.
D. một liên kết ba.
Lời giải:
Đáp án: B
Câu 13. Etilen có tính chất vật lý nào sau đây?
A. là chất khí không màu, không mùi, tan nhiều trong nước, nhẹ hơn không khí.
B. là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí màu vàng lục, mùi xốc, ít tan trong nước, nặng hơn không khí.
D. là chất khí không màu, mùi hắc, tan trong nước, nặng hơn không khí.
Lời giải:
Đáp án: B
Giải thích:
Etilen có tính chất vật lý là
B. là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
Câu 14. Khi đốt cháy khí etilen thì số mol CO2 và H2O được tạo thành theo tỉ lệ
A. 2 : 1.
B. 1 : 2.
C. 1 : 3.
D. 1 : 1.
Lời giải:
Đáp án: D
Câu 15. Cho rượu etylic nguyên chất tác dụng với kali dư. Số phản ứng hóa học xảy ra là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án: A
Câu 16. Cho rượu etylic 80o tác dụng với natri dư. Số phản ứng hóa học xảy ra là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án: B
Câu 17. Nhận xét nào sau đây là sai?
A. Rượu etylic là chất lỏng, không màu.
B. Rượu etylic tan vô hạn trong nước.
C. Rượu etylic có thể hòa tan được iot.
D. Rượu etylic nặng hơn nước.
Lời giải:
Đáp án: D
Câu 18. Độ rượu là
A. số ml rượu etylic có trong 100 ml hỗn hợp rượu với nước.
B. số ml nước có trong 100 ml hỗn hợp rượu với nước.
C. số gam rượu etylic có trong 100 ml hỗn hợp rượu với nước.
D. số gam nước có trong 100 gam hỗn hợp rượu với nước.
Lời giải:
Đáp án: A
Câu 19. Rượu etylic tác dụng được với dãy hóa chất là
A. NaOH; Na; CH3COOH; O2.
B. Na; K; CH3COOH; O2.
C. C2H4; K; CH3COOH; Fe.
D. Ca(OH)2; K; CH3COOH; O2.
Lời giải:
Đáp án: B
Giải thích:
C2H5OH + Na → C2H5ONa +1/2H2
C2H5OH + K → C2H5OK + 1/2H2
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
C2H5OH + 3O2 → 2CO2 + 3H2O
Câu 20. Trong 100 ml rượu 40° có chứa
A. 40 ml nước và 60 ml rượu nguyên chất.
B. 40 ml rượu nguyên chất và 60 ml nước.
C. 40 gam rượu nguyên chất và 60 gam nước.
D. 40 gam nước và 60 gam rượu nguyên chất.
Lời giải:
Đáp án: B
Giải thích:
Trong 100 ml rượu 40° có chứa 40 ml rượu nguyên chất và 60 ml nước.
Xem thêm các phương trình phản ứng hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
