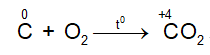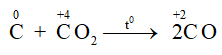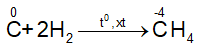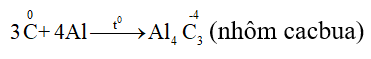C + CO2 → CO | C ra CO
C + CO2 → CO là phản ứng oxi hoá khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng C + CO2 → CO
1. Phản ứng tạo thành khí CO
C + CO2 2CO
2. Điều kiện phản ứng C ra CO
Nhiệt độ cao trong lò.
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của C (Cacbon)
- Trong phản ứng trên C là chất khử.
- C chủ yếu thể hiện tính khử khi tác dụng với CO2, O2,...
3.2. Bản chất của CO2 (Cacbon dioxit)
- Trong phản ứng trên CO2 là chất oxi hoá.
- CO2 là oxit axit bền, ở nhiệt độ cao thể hiện tính oxi hóa khi tác dụng với các chất khử mạnh.
4. Tính chất hóa học của C
- Trong các dạng tồn tại của C, C vô định hình hoạt động hơn cả về mặt hóa học.
- Trong các phản ứng hóa học C thể hiện hai tính chất: Tính oxi hóa và tính khử. Tuy nhiên tính khử vẫn là chủ yếu của C.
4.1. Tính khử
- Tác dụng với oxi
Ở nhiệt độ cao C lại khử CO2 theo phản ứng:
- Tác dụng với oxit kim loại:
+ C khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học của kim loại:
CuO + C → Cu + CO (tº)
Fe2O3 + 3C → 2Fe + 3CO (tº)
+ Với CaO và Al2O3:
CaO + 3C → CaC2 + CO (trong lò điện)
2Al2O3 + 9C → Al4C3 + 6CO (2000ºC)
- Tác dụng với các chất oxi hóa mạnh thường gặp H2SO4 đặc, HNO3, KNO3, KClO3, K2Cr2O7, ... trong các phản ứng này, C bị oxi hóa đến mức +4 (CO2).
C + 2H2SO4 đặc → CO2 + 2SO2 + 2H2O (tº)
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O (tº)
C + 4KNO3 → 2K2O + CO2 + 4NO2 (tº)
- Khi nhiệt độ cao, C tác dụng được với hơi nước:
C + H2O → CO + H2 (1000ºC)
C + 2H2O → CO2 + 2H2
4.2. Tính oxi hóa
- Tác dụng với hidro
- Tác dụng với kim loại
5. Ứng dụng của Cacbon
- Than chì được dùng làm điện cực, chất bôi trơn, ruột bút chì; …
- Kim cương được dùng làm đồ trang sức quý hiếm, mũi khoan, dao cắt kính...
- Cacbon vô định hình cũng có nhiều ứng dụng:
+ Than hoạt tính làm mặt nạ phòng độc. khử mùi,…
+ Than gỗ dùng làm chất đốt, chất khử,…
6. Tính chất hóa học của CO2
CO2 là oxit axit
- CO2 tan trong nước tạo thành axit cacbonic (là một điaxit rất yếu)
CO2 + H2O ↔ H2CO3
- CO2 tác dụng với oxit bazơ → muối.
CaO + CO2 → CaCO3 (t0)
- CO2 tác dụng với dung dịch bazơ → muối + H2O
NaOH + CO2 → NaHCO3
2NaOH + CO2 → Na2CO3 + H2O
- CO2 bền, ở nhiệt độ cao thể hiện tính oxi hóa khi tác dụng với các chất khử mạnh
CO2 + 2Mg → 2MgO + C
CO2 + C → 2CO
Lưu ý: Được dùng để giải thích CO2 không dùng để dập tắt các đám cháy kim loại.
7. Bài tập vận dụng
Câu 1: Thành phần chính của quặng hemantit là:
A. Fe3O4
B. Fe2O3
C. FeO
D. Fe
Lời giải:
Đáp án: B
Câu 2: Trong công nghiệp đời sống, gang và thép được sử dụng nhiều vì có ưu điểm là
A. Cứng, dẻo, ít bị ăn mòn
B. Cứng, đàn hồi và nhẹ
C. Mềm, dễ nóng chảy và nhẹ
D. Dễ nóng chảy, nhẹ và ít bị ăn mòn
Lời giải:
Đáp án: A
Câu 3: Phát biểu nào sau đây đúng?
A. Thép là hợp kim của nhôm với cacbon và một số nguyên tố khác, trong hàm lượng cacbon nhỏ hơn 2%
B. Thép là hợp kim của nhôm với cacbon và một số nguyên tố khác, trong hàm lượng cacbon chiếm từ 2% - 5%
C. Thép là hợp kim của sắt với cacbon và một số nguyên tố khác, trong hàm lượng cacbon nhỏ hơn 2%
D. Thép là hợp kim của sắt với cacbon và một số nguyên tố khác, trong hàm lượng cacbon lớn hơn 2%
Lời giải:
Đáp án: C
Câu 4. Trong quá trình sản xuất gang, thép, khí nào bị thải ra gây ảnh hưởng đến môi trường?
A. SO2
B. H2
C. N2O
D. O2
Lời giải:
Đáp án: A
Câu 5. Thổi khí CO vào lò luyện thép phản ứng hóa học không xảy ra là:
A. O2 + Fe → 2FeO
B. C + O2 → CO2
C. FeO + CO→ Fe + CO2
D. 2FeO + 2Mn → Fe + MnO2
Lời giải:
Đáp án: A
Xem thêm các phương trình phản ứng hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)