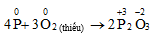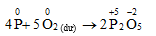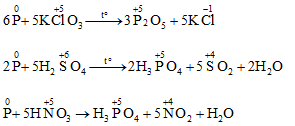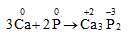P + H2SO4 → H3PO4 + SO2 + H2O | P ra H3PO4
P + H2SO4 → H3PO4 + SO2 + H2O là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng P + H2SO4 → H3PO4 + SO2 + H2O
1. Phương trình phản ứng P tác dụng H2SO4 đặc
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
2. Điều kiện để phản ứng P ra H3PO4
Nhiệt độ, H2SO4 đặc.
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của P (Photpho)
- Trong phản ứng trên P là chất khử.
- P vừa có tính khử vừa có tính oxi hoá nên P khử được một số hợp chất có tính oxi hoá mạnh.
3.2. Bản chất của H2SO4 (Axit sunfuric)
- Trong phản ứng trên H2SO4 là chất oxi hoá.
- Trong H2SO4 thì S có mức oxi hoá +6 cao nhất nên H2SO4 đặc có tính axit mạnh, oxi hoá mạnh và háo nước.
4. Tính chất hoá học của P
P vừa có tính khử vừa có tính oxi hóa
4.1. Tính khử
a. Khử phi kim mạnh hơn:O2, Cl2, S...
- Khử O2 :
Photpho trắng tác dụng với oxi ở điều kiện thường, phản ứng tỏa năng lượng ở dạng ánh sáng → gây ra hiện tượng phát quang hóa học
Photpho đỏ chỉ tác dụng với oxi ở nhiệt độ cao
- Khử : 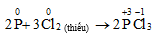
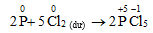
b. Khử một số hợp chất có tính oxi hóa mạnh
4.2. Tính oxi hóa
* P oxi hóa các kim loại hoạt động tạo ra photphua kim loại
5. Ứng dụng của P
+ P đỏ được dùng trong sản xuất diêm.
+ Điều chế axit photphoric, thuốc trừ sâu chứa photpho…
+ Dùng trong quân sự: sản xuất bom, đạn cháy, đạn khói…
+ Photpo còn là một nguyên tố rất cần cho con người nhất là trí thông minh, sáng tạo, phát triển xương. Cần cho cây nhất là cấy ăn quả.
6. Tính chất hoá học của H2SO4
6.1. H2SO4 loãng
Axit sunfuric là một axit mạnh, hóa chất này có đầy đủ các tính chất hóa học chung của axit như:
- Axit sunfuric H2SO4 làm chuyển màu quỳ tím thành đỏ.
- Tác dụng với kim loại đứng trước H (trừ Pb) tạo thành muối sunfat.
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazo tạo thành muối mới (trong đó kim loại giữ nguyên hóa trị) và nước .
FeO + H2SO4 → FeSO4 + H2O
- Axit sunfuric tác dụng với bazo tạo thành muối mới và nước.
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
- H2SO4 tác dụng với muối tạo thành muối mới (trong đó kim loại vẫn giữ nguyên hóa trị) và axit mới.
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
6.2. H2SO4 đặc
Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh với tính chất hóa học nổi bật như:
- Tác dụng với kim loại: Khi cho mảnh Cu vào trong H2SO4 tạo ra dung dịch có màu xanh và có khí bay ra với mùi sốc.
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
- Tác dụng với phi kim tạo thành oxit phi kim + H2O + SO2.
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
- Tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- H2SO4 còn có tính háo nước đặc trưng như đưa H2SO4 vào cốc đựng đường, sau phản ứng đường sẽ bị chuyển sang màu đen và phun trào với phương trình hóa học như sau.
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
7. Câu hỏi vận dụng
Câu 1. Phát biểu nào sau đây không đúng?
A. Dùng KMnO4 oxi hoá dung dịch HCl đặc tạo ra khí Cl2.
B. Nhiệt phân KMnO4 tạo ra khí O2.
C. Cho dung dịch HCl dư vào CuS tạo ra khí H2S.
D. Cho dung dịch HCl dư vào dung dịch Na2SO3 tạo ra khí SO2.
Lời giải:
Đáp án: C
Giải thích:
A. Đúng:
16HCl + 2KMnO4 → 5Cl2 + 8H2O + 2KCl + 2MnCl2
B. Đúng
2KMnO4⟶ MnO2 + O2 + K2MnO4
C. Sai
Không tan trong nước và không tan trong HCl, H2SO4 loãng: CuS, PbS, Ag2S, SnS, CdS, HgS…
d. Đúng,
H2SO4 + Na2SO3 → H2O + Na2SO4 + SO2
Câu 2. Trong các thí nghiệm sau:
(1) Nhiệt phân KClO3 có xúc tác MnO2
(2) Cho khí O3 tác dụng với dung dịch KI
(3) Cho khí SO2tác dụng với khí H2S
(4) Sục khí SO2vào dung dịch nước Brom
Số thí nghiệm tạo ra đơn chất là bao nhiêu?
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án: C
Giải thích:
3KClO3 → 3KCl + 3O2
O3 + 2KI + H2O → 2KOH + I2 + O2
SO2 + 2H2S → 3S↓ + 2H2O
SO2 + Br2+ 2H2O → 2HBr + H2SO4
Câu 3. Cho phương trình hoá học: P + H2SO4 → H3PO4 + SO2 + H2O. Hệ số của chất oxi hoá và hệ số của chất khử lần lượt là (biết hệ số cân bằng của phản ứng là các số nguyên, tối giản)
A. 5 và 2.
B. 2 và 5.
C. 7 và 9.
D. 7 và 7.
Lời giải:
Đáp án: A
Giải thích:
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
Chất oxi hóa: H2SO4
Chất khử: P
Câu 4. Trong sản xuất, oxi được dùng nhiều nhất để làm gì?
A. sử dụng làm nhiên liệutên lửa.
B. sử dụng luyện thép.
C. sử dụng trong công nghiệp hoá chất.
D. sử dụng hàn, cắt kim loại.
Lời giải:
Đáp án: C
Xem thêm các phương trình phản ứng hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)