Fe + Cu(NO3)2 → Cu + Fe(NO3)2 | Fe ra Fe(NO3)2 | Fe ra Cu | Cu(NO3)2 ra Cu | Cu(NO3)2 ra Fe(NO3)2
Phản ứng hóa học: Fe + Cu(NO3)2 hay Fe ra Fe(NO3)2 hoặc Fe ra Cu hoặc Cu(NO3)2 ra Cu hoặc Cu(NO3)2 ra Fe(NO3)2 thuộc loại phản ứng oxi hóa khử, phản ứng thế đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về Fe có lời giải, mời các bạn đón xem
Phản ứng Fe + Cu(NO3)2 → Cu + Fe(NO3)2
1. Phương trình hoá học của phản ứng Fe tác dụng với Cu(NO3)2
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Cách lập phương trình hoá học:
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hoá, từ đó xác định chất oxi hoá – chất khử:
Chất khử: Fe; chất oxi hoá: Cu(NO3)2.
Bước 2: Biểu diễn quá trình oxi hoá, quá trình khử
- Quá trình oxi hoá:
- Quá trình khử:
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hoá
Bước 4: Điền hệ số của các chất có mặt trong phương trình hoá học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
2. Điều kiện để Fe tác dụng với Cu(NO3)2
Phản ứng giữa sắt và đồng (II) nitrat diễn ra ngay điều kiện thường.
3. Cách tiến hành thí nghiệm
Nhỏ từ từ dung dịch Cu(NO3)2 vào ống nghiệm đã để sẵn miếng sắt.
4. Hiện tượng phản ứng
Sắt tan dần trong dung dịch, đồng thời xuất hiện lớp đồng màu đỏ sáng
5. Tính chất hóa học của sắt
Sắt là kim loại có tính khử trung bình. Khi tác dụng với chất oxi hóa yếu, sắt bị oxi hóa đến số oxi hóa +2.
Fe → + 2e
Với chất oxi hóa mạnh, sắt bị oxi hóa đến số oxi hóa +3.
Fe → < + 3e
5.1. Tác dụng với phi kim:
Ở nhiệt độ cao, sắt khử nguyên tử phi kim thành ion âm và bị oxi hóa đến số oxi hóa +2 hoặc +3.
+ Tác dụng với lưu huỳnh:
+ Tác dụng với oxi:
+ Tác dụng với clo:
5.2. Tác dụng với axit
- Với dung dịch HCl, H2SO4 loãng, Fe bị oxi hóa đến số oxi hóa +2, giải phóng H2. Ví dụ:
Fe + H2SO4 → FeSO4 + H2
- Với dung dịch HNO3 và H2SO4 đặc nóng, Fe bị oxi hóa đến số oxi hóa +3, và không giải phóng H2. Ví dụ:
Fe + 4HNO3 loãng → Fe(NO3)3 + NO + 2H2O
Chú ý: Fe bị thụ động bởi các axit HNO3 đặc, nguội và H2SO4 đặc, nguội.
5.3. Tác dụng với dung dịch muối
Fe có thể khử được ion của các kim loại đứng sau nó trong trong dãy điện hóa của kim loại. Trong các phản ứng này, Fe thường bị oxi hóa đến số oxi hóa +2. Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
Đặc biệt:
Fe + 2Ag+ → Fe2+ + 2Ag
Nếu Ag+ dư, tiếp tục có phản ứng:
Fe2+ + Ag+ → Fe3+ + Ag
5.4. Tác dụng với nước
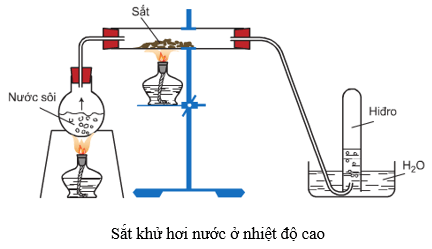
Ở nhiệt độ thường, sắt không khử được nước, nhưng ở nhiệt độ cao, sắt khử hơi nước tạo ra H2 và Fe3O4 hoặc FeO.
3Fe + 4H2O Fe3O4 + 4H2
Fe + H2O FeO + H2
6. Tính chất vật lí của Fe
- Màu xám hơi trắng, dễ ràn và dẻo cũng như có thể dát mỏng hay kéo sợi, khả năng dẫn điện và nhiệt không bằng nhôm hay đồng.
- Nhiễm từ ở nhiệt độ cao khoảng 800 độ C sẽ nhiễm từ và mất từ tính.
7. Bài tập liên quan
Câu 1: Sắt tác dụng với H2O ở nhiệt độ cao hơn 570°C thì tạo ra H2 và sản phẩm rắn là
A. FeO. B. Fe3O4. C. Fe2O3. D. Fe(OH)2.
Hướng dẫn giải
Đáp án A
3Fe + 4H2O Fe3O4 + 4H2
Fe + H2O FeO + H2
Câu 2:Tính chất vật lí nào sau đây không phải của sắt?
A. Kim loại nặng, khó nóng chảy. B. Màu vàng nâu, dẻo, dễ rèn.
C. Dẫn điện và dẫn nhiệt tốt. D. Có tính nhiễm từ.
Hướng dẫn giải
Đáp án B
Tính chất vật lý của sắt:
- Có màu trắng hơi xám.
- Dẻo, dễ rèn, nóng chảy ở nhiệt độ 1540oC
- Là kim loại nặng, có khối lượng riêng d = 7,9 g/cm3
- Dẫn điện, dẫn nhiệt tốt.
- Là kim loại có từ tính, bị nam châm hút.
→ Khẳng định sắt có màu vàng nâu là sai.
Câu 3: Phản ứng xảy ra khi đốt cháy sắt trong không khí là
A. 3Fe + 2O2 Fe3O4.
B. 4Fe + 3O2 2Fe2O3.
C. 2Fe + O2 2FeO.
D. Fe + O2 FeO2.
Hướng dẫn giải
Đáp án A
Đốt cháy sắt trong không khí tạo thành Fe3O4
Câu 4: Hợp chất nào sau đây của sắt vừa có tính khử, vừa có tính oxi hóa?
A. FeO. B. Fe2O3. C. Fe(OH)3. D. Fe2(SO4)3.
Hướng dẫn giải
Đáp án A
Trong hợp chất FeO số oxi hóa của Fe là +2 → Fe có thể tăng số oxi hóa lên +3 hoặc giảm số oxi hóa về 0. Nên FeO vừa có tính khử, vừa có tính oxi hóa.
Câu 5: Chất nào dưới đây phản ứng với Fe tạo thành hợp chất Fe(II)?
A. Cl2 B. dung dịch HNO3 loãng
C. dung dịch AgNO3 dư D. dung dịch HCl
Hướng dẫn giải
Đáp án D
A. 2Fe + 3Cl2 → 2FeCl3
B. Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
C. Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3 dư→ Fe(NO3)3 + Ag
D. Fe + 2HCl → FeCl2 + H2
Câu 6: Kim loại Fe thụ động bởi dung dịch
A. H2SO4 loãng B. HCl đặc, nguội
C. HNO3 đặc, nguội D. HCl loãng
Hướng dẫn giải
Đáp án C
Fe thụ động trong dung dịch HNO3 đặc, nguội và H2SO4 đặc, nguội.
Câu 7: Cho 2,24 gam Fe tác dụng với oxi, thu được 3,04 gam hỗn hợp X gồm 2 oxit. Để hoà tan hết X cần thể tích dung dịch HCl 2M là
A. 25 ml. B. 50 ml. C. 100 ml. D. 150 ml.
Hướng dẫn giải
Đáp án B
Áp dụng định luật bảo toàn khối lượng
mFe + mO = m oxit
→ 2,24 + mO = 3,04
→ mO = 0,8 gam
→ nO = 0,05 mol
Áp dụng bảo toàn nguyên tố
Oxit + HCl → muối clorua + H2O
nHCl = nH (axit) = 2. = 2.nO = 2.0,05 = 0,1 mol
→ Vdd HCl 2M = = 0,05 lít = 50 ml
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)