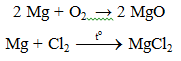Mg + HNO3 → Mg(NO3)2 + N2 + H2O | Mg ra Mg(NO3)2
Mg + HNO3 → Mg(NO3)2 + N2 + H2O là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng Mg + HNO3 → Mg(NO3)2 + N2 + H2O
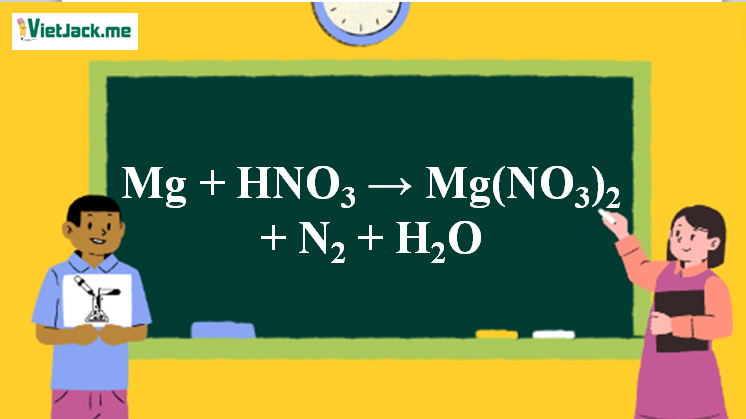
1. Phương trình phản ứng Mg tác dụng HNO3
Mg + HNO3 → Mg(NO3)2 + N2 + H2O
2. Điều kiện phản ứng giữa Mg + HNO3 ra N2
Không có
3. Cách tiến hành phản ứng giữa Mg và dung dịch HNO3
Cho kim loại magie tác dụng với dung dịch axit nitric.
4. Hiện tượng phản ứng giữa Mg và dung dịch HNO3
Chất rắn màu trắng bạc Magie (Mg) tan dần và xuất hiện khí Nito (N2) làm sủi bọt khí.
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của Mg (Magie)
- Trong phản ứng trên Mg là chất khử.
- Mg là chất khử mạnh tác dụng được với các axit.
5.2. Bản chất của HNO3 (Axit nitric)
- Trong phản ứng trên HNO3 là chất oxi hoá.
- Đây là một monoaxit mạnh, có tính oxi hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ.
6. Tính chất hoá học của Mg
Magie là chất khử mạnh:
Mg → Mg2+ + 2e
6.1. Tác dụng với phi kim
Lưu ý:
- Do Mg có ái lực lớn với oxi: 2Mg + CO2 → MgO. Vì vậy không dùng tuyết cacbonic để dập tắt đám cháy Mg.
6.2. Tác dụng với axit
- Với dung dịch HCl và H2SO4 loãng:
Mg + H2SO4 → MgSO4 + H2
- Với dung dịch HNO3:
4Mg + 10 HNO3 → 4 Mg(NO3)2 + NH4NO3 + 3 H2O
6.3. Tác dụng với nước
- Ở nhiệt độ thường, Mg hầu như không tác dụng với nước. Mg phản ứng chậm với nước nóng (do tạo thành hidroxit khó tan).
Mg + 2H2O → Mg(OH)2 + H2
6.4. Ứng dụng
Magie giúp giảm đau nửa đầu.
Magie giúp giảm huyết áp.
Magie giúp ngăn ngừa bệnh tiểu đường.
Magie giúp điều trị táo bón.
Magie được sử dụng để điều trị viêm loét dạ dày.
7. Tính chất hóa học của HNO3
- Axit nitric là một dung dịch nitrat hydro có công thức hóa học HNO3 . Đây là một axit khan, là một monoaxit mạnh, có tính oxy hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ, có hằng số cân bằng axit (pKa) = −2.
- Axit nitric là một monoproton chỉ có một sự phân ly nên trong dung dịch, nó bị điện ly hoàn toàn thành các ion nitrat NO3− và một proton hydrat, hay còn gọi là ion hiđroni.
H3O+ HNO3 + H2O → H3O+ + NO3-
- Axit nitric có tính chất của một axit bình thường nên nó làm quỳ tím chuyển sang màu đỏ.
- Tác dụng với bazo, oxit bazo, muối cacbonat tạo thành các muối nitrat
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2
- Axit nitric tác dụng với kim loại: Tác dụng với hầu hết các kim loại trừ Au và Pt tạo thành muối nitrat và nước .
Kim loại + HNO3 đặc → muối nitrat + NO + H2O ( to)
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Kim loại + HNO3 loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
- Nhôm, sắt, crom thụ động với axit nitric đặc nguội do lớp oxit kim loại được tạo ra bảo vệ chúng không bị oxy hóa tiếp.
- Tác dụng với phi kim (các nguyên tố á kim, ngoại trừ silic và halogen) tạo thành nito dioxit nếu là axit nitric đặc và oxit nito với axit loãng và nước, oxit của phi kim.
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
P + 5HNO3 đặc → 5NO2 + H2O + H3PO4
3C + 4HNO3 loãng → 3CO2 + 4NO + 2H2O
- Tác dụng với oxit bazo, bazo, muối mà kim loại trong hợp chất này chưa lên hóa trị cao nhất:
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O + CO2
- Tác dụng với hợp chất:
3H2S + 2HNO3 (>5%) → 3Skết tủa + 2NO + 4H2O
PbS + 8HNO3 đặc → PbSO4 kết tủa + 8NO2 + 4H2O
Ag3PO4 tan trong HNO3, HgS không tác dụng với HNO3.
- Tác dụng với nhiều hợp chất hữu cơ: Axit nitric có khả năng phá hủy nhiều hợp chất hữu cơ, nên sẽ rất nguy hiểm nếu để axit này tiếp xúc với cơ thể người.
8. Bài tập vận dụng liên quan
Câu 1. Nhóm các kim loại tan được trong nước gồm:
A. Na, Mg, Al
B. Ca, K, Al
C. Ba, Fe, Na
D. Na, Ba, Ca
Lời giải:
2Na + 2H2O → 2NaOH + H2
Ba + 2H2O → Ba(OH)2 + H2
Ca + 2H2O → Ca(OH)2 + H2
Câu 2. Các nguyên tố sau O, K, Al, F, Mg, P. Hãy chỉ ra thứ tự sắp xếp đúng theo chiều tính kim loại giảm dần, tính phi kim tăng dần là
A. K, Mg, Al, P, O, F.
B. Al, K, Mg, O, F, P.
C. Mg, Al, K, F, P, O.
D. K, Mg, Al, F, O, P.
Lời giải:
Câu 3. Dãy gồm các chất đều phản ứng với dung dịch HCl là
A. K2SO4, Na2CO3.
B. Na2SO3, KNO3.
C. Na2SO4, MgCO3.
D. Na2CO3, CaCO3.
Lời giải:
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Câu 4. Cho hỗn hợp CaO, MgO, Na2CO3, Fe3O4 tan vào nước ta thu được kết tủa gồm:
A. MgO, Fe3O4
B. CaO, MgO, Fe3O4
C. CaCO3, MgO, Fe3O4
D. Na2CO3, Fe3O4
Lời giải:
Câu 5. Dãy các chất nào sau đây là muối axit ?
A. KHCO3, CaCO3, Na2CO3.
B. Ba(HCO3)2, NaHCO3, Ca(HCO3)2.
C. Mg(HCO3)2, Ba(HCO3)2, CaCO3.
D. Ca(HCO3)2, Ba(HCO3)2, BaCO3.
Lời giải:
Câu 6. Cho 1,08 gam kim loại M vào dung dịch H2SO4 loãng dư. Lọc dung dịch, đem cô cạn thu được 6,84 gam một muối khan duy nhất. Vậy kim loại M là:
A. Ni
B. Ca
C. Al
D. Fe
Lời giải:
Gọi kim loại M có hóa trị n (n = 1, 2, 3, 4)
2M + nH2SO4 → M2(SO4)n + nH2
Ta có: nM = (mol);
nM2(SO4)n = mol
Theo phản ứng:
nM = 2.nR2(SO4)n=> =
=> M = 9n
Ta có bảng biện luận sau
| n | 1 | 2 | 3 | 4 |
| M | 9 loại | 18 loại | 27 (Al) | 36 loại |
Vậy M là kim loại Al
Câu 7. Cho 4 kim loại X, Y, Z, T đứng sau Mg trong dãy hoạt động hóa học, biết rằng:
X, Y tác dụng được với dung dịch HCl giải phóng khí Hidro
Z, T không có phản ứng với dung dịch HCl
Y tác dụng với dung dịch muối của X và giải phóng kim loại X
T tác dụng được với dung dịch muối của Z là giải phóng kim loại Z
Kim loại có tính khử yếu nhất trong 4 kim loại là:
A. T
B. Y
C. Z
D. X
Lời giải:
X, Y phản ứng được với HCl => X, Y đứng trước H trong dãy hoạt động hóa học
Z, T không phản ứng với HCl => Z, T đứng sau H trong dãy hoạt động hóa học
=> X, Y có tinh khử mạnh hơn Z, T. Giờ chỉ so sánh Z và T
T đẩy được Z ra khỏi muối của Z => T có tính khử mạnh hơn Z
=> Z là có tính khử yếu nhất
Câu 8. Cho hỗn hợp Al, Fe tác dụng với hỗn hợp dung dịch AgNO3, Cu(NO3)2 thu được dung dịch B và chất rắn D gồm 3 kim loại. Cho D tác dụng với HCl dư, thấy có khí bay lên. Thành phần của chất rắn D là
A. Fe, Cu, Ag
B. Al, Cu, Ag
C. Al, Fe, Cu, Ag
D. Al, Fe, Cu
Lời giải:
Thứ tự phản ứng:
Kim loại sẽ phản ứng theo thứ tự: Al, Fe
Muối sẽ phản ứng theo thứ tự: AgNO3, Cu(NO3)2
Vậy 3 kim loại là: Fe, Ag, Cu
Câu 9. Hỗn hợp bột gồm 3 kim loại Mg, Al, Zn có khối lượng 3,59 gam được chia làm hai phần đêu nhau. Phần 1 đem đốt cháy hoàn toàn trong oxi dư thu được 4,355 gam hỗn hợp oxit. Phần 2 hòa tan hoàn toàn trong HNO3 đặc nóng dư thu được V lít (đktc) khí NO2 (sản phẩm khử duy nhất). Hãy tính giá trị của V.
A. 14,336 lít
B. 6,72 lít
C. 13,36 lít
D. 7,168 ít
Lời giải:
Áp dụng định luật bảo toàn khối lượng đối với phần 1 ta có:
mO2 = 4,355 - = 2,56 (g) ⇒ nO2 = = 0,08 (mol)
Do khối lượng kim loại ở hai phần bằng nhau nên số mol do hỗn hợp kim loại nhường là như nhau ⇒ số mol eletron do O2 nhận bằng số mol eletron do N5+ nhận.
O2 + 4e → 2O2-
0,08 → 0,32
N+5 + 1e → N+4 (NO2)
0,32 → 0,32
=> nNO2 = 4nO2 = 0,32 => VNO2 = 0,32.22,4 = 7,168 lít
Xem thêm các phương trình hóa học khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)