Al2O3 + H2SO4 → Al2(SO4)3 +H2O | Al2O3 ra Al2(SO4)3
Al2O3 + H2SO4 → Al2(SO4)3 +H2O là phản ứng trao đổi. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng Al2O3 + H2SO4 → Al2(SO4)3 +H2O
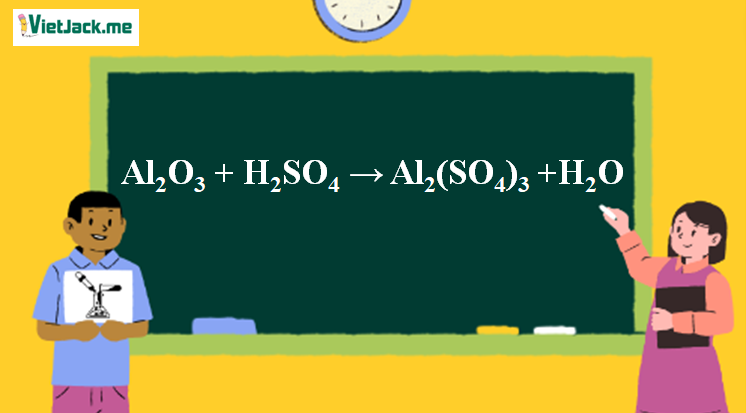
1. Phương trình phản ứng Al2O3 ra Al2(SO4)3
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
2. Điều kiện phản ứng Al2O3 tác dụng H2SO4
Nhiệt độ thường
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của Al2O3 (Nhôm oxit)
Al2O3 là oxit lưỡng tính tác dụng được với axit.
3.2. Bản chất của H2SO4 (Axit sunfuric)
H2SO4 là một axit mạnh tác dụng được với Al2O3.
4. Mở rộng về Al2O3
4.1. Nhôm oxit là gì?
Nhôm oxit hay còn gọi là a-lu-min (bắt nguồn từ từ tiếng Pháp) là một hợp chất hóa học của nhôm và oxi với công thức hóa học Al2O3. Nó còn được biết đến với tên gọi alumina trong cộng đồng các ngành khai khoáng, gốm sứ, và khoa học vật liệu.
4.2. Tính chất vật lí và nhận biết
Tính chất vật lí: Là chất rắn màu trắng, không tan trong nước, rất bền, nóng chảy ở 2050oC.
Nhận biết: Mang hòa tan Al2O3 vào dung dịch NaOH, thấy tan ra, tạo dung dịch không màu.
Al2O3 + 2NaOH → NaAlO2 + H2O
4.3. Tính chất hóa học
Al2O3 là oxit lưỡng tính
- Tác dụng với axit:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
- Tác dụng với dung dịch bazơ mạnh
Al2O3 + 2NaOH → NaAlO2 + H2O
hay
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
Al2O3 + 2OH- → 2AlO2- + H2O
- Al2O3 tác dụng với C
Al2O3 + 9C Al4C3 + 6CO
- Tính bền:
Tính bền cũng là một trong những tính chất hóa học của nhôm oxit khá quan trọng. Lí do là vì Ion Al3+ có điện tích lớn(3+) và bán kính nhỏ(0.048nm), bằng 1/2 bán kính ion Na+ nên lực hút giữa ion Al3+ và ion O2– rất mạnh, tạo ra liên kết rất bền vững.
Vì thế Al2O3 có nhiệt độ nóng chảy rất cao(2050oC) và rất khó bị khử thành kim loại Al.
Khử Al2O3 bằng C không cho Al mà thu được Al4C3
- Al2O3 không tác dụng với H2, CO ở bất kì nhiệt độ nào.
4.4. Điều chế Al2O3
Nhiệt phân Al(OH)3: 2Al(OH)3 Al2O3 + 3H2O
4.5. Ứng dụng
– Ngành công nghiệp xây dựng: Nhôm oxit thường được sử dụng để sản xuất xi măng, một trong những nguyên liệu chính trong xây dựng. Nó cung cấp tính năng chống cháy và tạo độ cứng cho vật liệu xây dựng, đồng thời giúp tăng khả năng bám dính của xi măng.
– Ngành công nghiệp điện tử: Nhôm oxit cũng là thành phần chính trong việc sản xuất các loại sơn dẫn điện và sơn chịu nhiệt. Các sản phẩm này thường được ứng dụng trong việc gia công và sản xuất các linh kiện điện tử, đảm bảo tính ổn định và an toàn của các mạch điện tử.
– Ngành công nghiệp thực phẩm và dược phẩm: Nhôm oxit thường được sử dụng như một chất chống đông trong việc sản xuất thực phẩm và dược phẩm. Điều này đảm bảo sự an toàn và vệ sinh của các sản phẩm này trước khi đến tay người tiêu dùng.
– Ngành công nghiệp gốm sứ và thủy tinh: Nhôm oxit là một trong những thành phần quan trọng trong việc sản xuất gốm sứ và thủy tinh. Nó cung cấp tính chất chống nứt và tăng độ cứng cho các sản phẩm, đồng thời cũng làm cho chất liệu trở nên bóng đẹp và dễ sơn màu.
– Ngành công nghiệp dầu khí: Nhôm oxit được sử dụng để sản xuất chất trơ đặc biệt dùng trong công nghiệp dầu khí. Chất này giúp tạo ra các sản phẩm chống ăn mòn và bảo vệ thiết bị trong môi trường dầu khí khắc nghiệt.
– Ngành công nghiệp mỹ phẩm và mỹ phẩm: Trong ngành mỹ phẩm, nhôm oxit thường được sử dụng làm thành phần chống nắng, giúp bảo vệ da khỏi tác động của tia UV.
5. Tính chất hoá học của H2SO4
5.1. H2SO4 loãng
Axit sunfuric là một axit mạnh, hóa chất này có đầy đủ các tính chất hóa học chung của axit như:
- Axit sunfuric H2SO4 làm chuyển màu quỳ tím thành đỏ.
- Tác dụng với kim loại đứng trước H (trừ Pb) tạo thành muối sunfat.
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazo tạo thành muối mới (trong đó kim loại giữ nguyên hóa trị) và nước .
FeO + H2SO4 → FeSO4 + H2O
- Axit sunfuric tác dụng với bazo tạo thành muối mới và nước.
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
- H2SO4 tác dụng với muối tạo thành muối mới (trong đó kim loại vẫn giữ nguyên hóa trị) và axit mới.
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
5.2. H2SO4 đặc
Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh với tính chất hóa học nổi bật như:
- Tác dụng với kim loại: Khi cho mảnh Cu vào trong H2SO4 tạo ra dung dịch có màu xanh và có khí bay ra với mùi sốc.
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
- Tác dụng với phi kim tạo thành oxit phi kim + H2O + SO2.
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
- Tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- H2SO4 còn có tính háo nước đặc trưng như đưa H2SO4 vào cốc đựng đường, sau phản ứng đường sẽ bị chuyển sang màu đen và phun trào với phương trình hóa học như sau.
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
6. Bài tập vận dụng liên quan
Câu 1. Thực hiện các thí nghiệm sau :
(a) Cho từ từ NaOH đến dư vào dung dịch Al2(SO4)3,
(b) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaOH,
(c) Cho từ từ NH3 đến dư vào dung dịch Al2(SO4)3,
(d) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NH3.
(e) Cho từ từ HCl đến dư vào dung dịch NaAlO2.
(f) Cho từ từ NaAlO2 đến dư vào dung dịch HCl
(g) Cho từ từ Al2(SO4)3 đến dư vào dung dịch NaAlO2
Trong các thí nghiệm trên, số thí nghiệm xuất hiện kết tủa là
A. 2.
B. 3.
C. 5.
D. 7.
Lời giải:
Câu 2. Dùng hóa chất nào sau đây để phân biệt Zn(NO3)2 và Al(NO3)3?
A. Dung dịch NaOH
B. Dung dịch Ba(OH)2
C. Dung dịch NH3
D. Dung dịch nước vôi trong
Lời giải:
Câu 3. Trong các cặp chất sau đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
A. AlCl3 và Na2CO3
B. HNO3 và NaHCO3
C. NaAlO2 và KOH
D. NaCl và AgNO3
Lời giải:
Cặp chất có thể cùng tồn tại trong một dung dịch là cặp chất đó không phản ứng với nhau
A. Không phản ứng
B. NaHCO3 + HNO3 → NaNO3 + H2O + CO2
C. NaAlO2 + KOH → KAlO2 + NaOH
D. AgNO3 + NaCl → AgCl↓ + NaNO3
Câu 4. Nung hỗn hợp X gồm Al và Fe3O4 có tỷ lệ khối lượng 1:1, sau khi các phản ứng hoàn toàn thu được chất rắn Y Thành phần của chất rắn Y
A. Al2O3, Fe, Al.
B. Al2O3, Fe, Fe3O4.
C. Al2O3, FeO, Al.
D. Al2O3, Fe.
Lời giải:
Coi nAl = nFe3O4= 1 (mol)
4Al + Fe3O4 → 2Al2O3+ 3Fe
1 → 0,25 (mol)
Al và Fe3O4 có tỉ lệ 1: 1 nên Fe3O4 sẽ dư
Vậy chất rắn sau phản ứng gồm: Al2O3; Fe và Fe3O4 dư
Câu 5. Trong các chất sau chất nào không có tính lưỡng tính
A. ZnSO4
B. Al(OH)3
C. KHCO3
D. Al2O3
Lời giải:
KHCO3 vừa tác dụng được với axit, vừa tác dụng được với dung dịch bazo nên là chất lưỡng tính
KHCO3 + HCl → KCl + CO2↑ + H2O
2KHCO3 + 2NaOH → K2CO3+ Na2CO3 + 2H2O
Al2O3 và Al(OH)2 vừa tác dụng dung dịch axit mạnh vừa tác dụng với dung dịch bazo mạnh.
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Al(OH)3+ 3HCl → AlCl3+ 3H2O
Al(OH)3+ NaOH → NaAlO2 + 2H2O
Câu 6. Nhận định nào sau đây sai?
A. Dung dịch AlCl3 và Al2(SO3)3 làm quỳ tím chuyển sang màu hồng
B. Al(OH)3, Al2O3, Al đều là các chất lưỡng tính
C. Al là kim loai nhẹ, dễ dát mỏng và có khả năng dẫn điện tốt
D. Từ Al2O3 có thế điều chế được Al.
Lời giải:
Câu 7. Khẳng định nào sau đây là đúng
A. Ba là nguyên tố có tính khử mạnh nhất trong dãy kim loại kiềm thổ
B. Tất cả các kim loại kiềm thổ đều tan trong nước ở nhiệt độ thường
C. Kim loại kiềm thổ có tính khử mạnh hơn kim loại kiềm
D. Tính khử của các kim loại kiềm thổ tăng dần từ Be đến Ba
Lời giải:
Mg và Be không phản ứng với nước ở điều kiện thường B sai.
Đi từ đầu nhóm IIA đến cuối nhóm theo chiều tăng dần điện tính hạt nhân tính kim loại (tính khử) tăng dần => Kim loại mạnh nhất là Ra; yếu nhất là Be. => A sai, D đúng.
Nhóm Kim loại kiềm có tính khử mạnh nhất => C sai.
Câu 8. Hiện tượng nào xảy ra khi cho từ từ đến dư dung dịch NaOH vào dung dịch AlCl3?
A. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện
B. Xuất hiện kết tủa keo trắng ngay lập tức, sau đó kết tủa tan dần
C. Ban đầu không thấy hiện tượng, sau đó kết tủa xuất hiện, rồi tan dần.
D. Xuất hiện kết tủa keo trắng ngay lập tức và không tan,
Lời giải:
Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3, ban đầu có kết tủa keo trắng xuất hiện.
3NaOH + AlCl3 → Al(OH)3 ↓ + 3NaCl
Sau đó kết tủa keo trắng tan trong NaOH dư tạo dung dịch trong suốt (vì Al(OH)3 có tính lưỡng tính tan được trong dung dịch axit dư, và kiềm dư)
NaOH + Al(OH)3 → NaAlO2 + 2H2O
Xem thêm các phương trình hóa học khác:
Al2(SO4)3 + NaOH→ Al(OH)3 + Na2SO4
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
