ZnO + NaOH → Na2ZnO2 + H2O | ZnO ra Na2ZnO2
ZnO + NaOH → Na2ZnO2 + H2O là phản ứng trao đổi. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng ZnO + NaOH → Na2ZnO2 + H2O
1. Phương trình phản ứng ZnO tác dụng NaOH
ZnO + 2NaOH → Na2ZnO2 + H2O
2. Điều kiện phản ứng xảy ra ZnO tác dụng NaOH
Nhiệt độ: 500 - 600oC
3. Bản chất của các chất tham gia phản ứng
3.1. Bản chất của ZnO (Kẽm oxit)
ZnO là oxit lưỡng tính tác dụng được với dung dịch bazo.
3.2. Bản chất của NaOH (Natri hidroxit)
NaOH là một bazo mạnh tác dụng được với ZnO.
4. Mở rộng kiến thức về ZnO
4.1. Tính chất vật lí & nhận biết
- Tính chất vật lí:
- Ở điều kiện thường kẽm oxit có dạng bột trắng mịn, khi nung trên 300oC chuyển sang màu vàng, sau khi làm lạnh thì trở lại màu trắng.
- Khi đưa vào mạng tinh thể một lượng nhỏ kim loại hóa trị I hoặc hóa trị III thì nó trở thành chất bán dẫn.
- Hơi của ZnO rất độc.
- Nhận biết: Hòa tan ZnO trong dung dịch NaOH, thấy chất rắn tan dần:
2NaOH + ZnO → Na2ZnO2 + H2O
4.2. Tính chất hóa học
Mang tính chất hóa học của oxit lưỡng tính
Tác dụng với axit
ZnO + 2HCl →ZnCl2 + H2O
ZnO + 2HNO3→ Zn(NO3)2 + H2O
Tác dụng với dung dịch bazơ
2NaOH + ZnO → Na2ZnO2 + H2O
Tác dụng với chất khử mạnh: Al, CO, H2
3ZnO + 2Al 
ZnO + H2 
4.3. Điều chế
Đốt cháy kẽm trong oxi
2Zn + O2 
4.4. Ứng dụng
Kẽm oxit khi được dùng chung với eugenol sẽ tạo thành eugenol kẽm oxit được ứng dụng trong nha khoa.
Kẽm Oxit ứng dụng trong ngành công nghiệp khác
Kẽm oxit có thể khử mùi và kháng khuẩn nên được thêm vào các vật liệu khác nhau bao gồm vải bông, cao su, bao bì thực phẩm.
Kẽm oxit là một thành phần của bộ lọc thuốc lá để loại bỏ các thành phần được lựa chọn từ khói thuốc lá.phụ gia thực phẩm
Oxit kẽm còn là chất phụ gia thực phẩm, được thêm vào nhiều sản phẩm thực phẩm, bao gồm ngũ cốc ăn sáng , như là một nguồn chất dinh dưỡng cần thiết.
5. Tính chất hoá học của NaOH
NaOH là một bazơ mạnh nó sẽ làm quỳ tím chuyển màu xanh, còn dung dịch phenolphtalein thành màu hồng. Một số phản ứng đặc trưng của Natri Hidroxit được liệt kê ngay dưới đây.
Phản ứng với axit tạo thành muối + nước:
NaOHdd + HCldd→ NaCldd + H2O
Phản ứng với oxit axit: SO2, CO2…
2 NaOH + SO2→ Na2SO3 + H2O
NaOH + SO2→ NaHSO3
Phản ứng với axit hữu cơ tạo thành muối và thủy phân este, peptit:
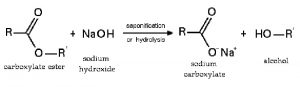
Phản ứng với muối tạo bazo mới + muối mới (điều kiện: sau phản ứng phải tạo thành chất kết tủa hoặc bay hơi):
2 NaOH + CuCl2→ 2NaCl + Cu(OH)2↓
Tác dụng với kim loại lưỡng tính:
2 NaOH + 2Al + 2H2O→ 2NaAlO2 + 3H2↑
2NaOH + Zn → Na2ZnO2 + H2↑
Tác dụng với hợp chất lưỡng tính:
NaOH + Al(OH)3 → NaAl(OH)4
2NaOH + Al2O3 → 2NaAlO2 + H2O
6. Bài tập vận dụng liên quan
Câu 1. Cho 8,1 gam ZnO phản ứng hết dung dịch HCl. Sau phản ứng thu được m gam muối. Tính giá trị m
A. 6,8 gam
B. 13,6 gam
C. 20,4 gam
D. 10,2 gam
Lời giải:
Câu 2. Thực hiện thí nghiệm sau cho ZnO tác dụng với dung dịch NaOH. Hiện tượng xảy ra của phản ứng là
A. ZnO không tan, xuất hiện bọt khí
B. Không thấy xuất hiện, hiện tượng gì
C. ZnO tan dần
D. Dung dịch có màu trong suốt
Lời giải:
Câu 3. Cho hỗn hợp Z gồm Fe(NO3)2 và ZnO vào dung dịch H2SO4 loãng (dư) thu được dd X. Cho dung dịch NaOH loãng (dư) vào X thu được kết tủa đó là
A. Fe(OH)3 và Zn(OH)2.
B. Fe(OH)2.
C. Fe(OH)2 và Zn(OH)2.
D. Fe(OH)3.
Lời giải:
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
ZnO + 2H+ → Zn2+ + H2O
Fe3+ + 3OH- → Fe(OH)3 ↓
Zn2+ + 2OH- → Zn(OH)2 ↓
Zn(OH)2 ↓ + 2OH- → ZnO22- + 2H2O
Sau phản ứng chỉ thu được kết tủa là Fe(OH)3
Xem thêm các phương trình hóa học khác:
Zn(OH)2 + NaOH → Na2ZnO2 + H2O
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)
