Công thức tính chất điện li và cách giải các dạng bài tập (2024) chi tiết nhất
Với tài liệu về Công thức tính chất điện li và cách giải các dạng bài tập (2024) chi tiết nhất bao gồm: lý thuyết và bài tập cũng như những định nghĩa, tính chất, các dạng bài sẽ giúp bạn nắm vững kiến thức và học tốt môn Vật lí hơn.
Chất điện li
1. Độ điện li (α)
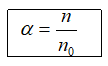
n: số phân tử hoà tan; n0: số phân tử ban đầu.
2. Chất điện li mạnh và chất điện li yếu
- Chất điện li mạnh: Là những chất khi tan trong nước, các phân tử hoà tan đều phân li ra ion (α = 1, phương trình biểu diễn →).
Axit mạnh: HCl, HNO3, HClO4, H2SO4, HBr, HI, …
Bazơ mạnh: KOH, NaOH, Ba(OH)2, …
Muối: Hầu hết các muối (trừ HgCl2, Hg(CN)2 ).
- Chất điện li yếu: Là những chất khi tan trong nước, chỉ có một phần số phân tử hoà tan phân li ra ion (0 < α < 1, phương trình biểu diễn ⇋).
Axit yếu: CH3COOH, HClO, H2S, HF, H2SO3, H2CO3, ...
Bazơ yếu: Mg(OH)2, Al(OH)3, NH3, …
- Cân bằng điện li:
Ví dụ: HF → H+ + F-
* Ảnh hưởng của sự pha trộn đến độ điện li α: Khi pha loãng → α tăng.
Xem thêm các phần Lý thuyết Hóa học lớp 11 hay khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- Phương trình hóa học | Tổng hợp PTHH của các chất hữu cơ, vô cơ chính xác nhất
- Đồng phân & Công thức cấu tạo của các chất hữu cơ
- Nhận biết các chất Hóa học
- Cấu hình electron
- So sánh bán kính nguyên tử và bán kính ion
- 1000 câu hỏi ôn tập môn Hóa có đáp án
- Wiki các chất hóa học | Định nghĩa, tính chất, nhận biết, điều chế, ứng dụng
- Cách đọc danh pháp hóa học (chương trình mới) đầy đủ nhất
- Công thức Lewis của một số chất thường gặp (chương trình mới)
- Công thức electron của một số chất thường gặp (chương trình mới)
- Công thức cấu tạo của một số chất thường gặp (chương trình mới)
- Công thức hợp chất khí với hidro của các nguyên tố (phổ biến) | Cách viết công thức hợp chất khí với hidro
- Công thức hidroxit cao nhất của các nguyên tố (phổ biến) | Cách viết công thức hidroxit cao nhất
- Công thức oxit cao nhất của các nguyên tố (phổ biến) | Cách viết công thức oxit cao nhất
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)