Lý thuyết, cách xác định và bài tập tính nồng độ mol
Tổng hợp cách xác định và bài tập các cách tính nồng độ mol giúp bạn nắm vững kiến thức và học tốt Hóa học.
Nồng độ mol
I. Định nghĩa
Nồng độ mol là đại lượng cho biết mối liên hệ giữa số mol của một chất tan và thể tích của dung dịch.
II. Công thức tính nồng độ mol
1.Công thức về nồng độ mol khi biết số mol và thể tích
CM = 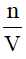
Trong đó:
n: số mol chất tan (đơn vị: mol)
V: thể tích dung dịch (đơn vị: lít)
2.Công thức về nồng độ mol khi biết nồng độ phần trăm và khối lượng riêng
CM = ![]()
Trong đó:
D: khối lượng riêng (đơn vị: g/ml)
C%: nồng độ phần trăm (đơn vị: C%)
M: khối lượng mol (đơn vị: g/mol)
III. Bài tập vận dụng
Câu 1: Tính nồng độ mol của dung dịch có chứa 0,75 mol Natri clorua (NaCl) trong 4,2 lít dung dịch?
Hướng dẫn:
Áp dụng công thức: CM = 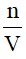
Nồng độ mol của NaCl là: CM = 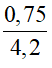 = 0,179M
= 0,179M
Câu 2: Tính nồng độ mol của dung dịch KOH 12%, biết khối lượng riêng của dung dịch là 1,1 g/ml?
Hướng dẫn :
Áp dụng công thức: CM = ![]()
Nồng độ mol của KOH là:
CM = 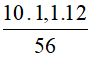 = 2,36M
= 2,36M
Câu 3: Trộn 4 lít dung dịch KCl 2M với 2 lít dung dịch KCl 5M. Tính nồng độ mol của dung dịch KCl sau trộn?
A. 2M
B. 3M
C. 4M
D. 5M
Hướng dẫn giải:
Số mol KCl có trong dung dịch sau khi trộn là: n = 2.4 + 5.2 = 18 mol
Thể tích của dung dịch sau khi trộn là: V = 4 + 2 = 6 lít
Nồng độ mol của dung dịch KCl sau khi trộn là: CM = nV = 186 = 3M
Đáp án B
Câu 4: Tính nồng độ mol của 350 ml dung dịch chứa 74,2 gam Na2CO3.
A. 5M
B. 4M
C. 3M
D. 2M
Hướng dẫn giải:
V = 350 ml = 0,35 l
Số mol của Na2CO3 là: n = 0,7 mol
Nồng độ mol của dung dịch Na2CO3 là
Áp dụng công thức: CM = nV = 0,70,35 = 2M
Đáp án D
Câu 5: Số mol của 200 ml HCl 0,15M là
A. 0,3 mol
B. 0,03 mol
C. 0,15 mol
D. 1,5 mol
Hướng dẫn giải:
V = 200 ml = 0,2 l
Áp dụng công thức: CM =nV suy ra n = CM.V
Vậy số mol của HCl là: nHCl = 0,15.0,2 = 0,03 mol
Đáp án B
Câu 6: Nồng độ mol của dung dịch cho biết:
A. Số mol chất tan có trong 1 lít dung dịch.
B. Khối lượng chất tan có trong 100 gam dung dịch.
C. Số mol chất tan có trong 100 gam dung dịch.
D. Số mol chất tan có trong 100 ml dung dịch.
Đáp án A
Câu 7: Nồng độ mol của 345 ml dung dịch chứa 27,6 gam NaOH là
A. 0,2M
B. 0,02M
C. 0,002M
D. 2M
Hướng dẫn giải:
V = 345 ml = 0,345 l
Số mol NaOH là: n = 0,69 mol
Nồng độ mol của dung dịch NaOH là:
Áp dụng công thức: CM = nV = 0,690,345 = 2M
Đáp án D
Câu 8: Trong 120 ml dung dịch có hòa tan m gam K2SO4 4M. Hãy tính giá trị của m.
A. 81,78 gam
B. 82,31 gam
C. 80,29 gam
D. 83,52 gam
Hướng dẫn giải:
V = 120 ml = 0,12 l
Áp dụng công thức: CM =nV suy ra n = CM.V
Suy ra số mol của K2SO4 là: n = 4.0,12 = 0,48 mol
Vậy khối lượng của K2SO4 là: m = 0,48.174 = 83,52 gam.
Đáp án D
Câu 9: Công thức đúng nhất của nồng độ mol là
A. CM = n.V
B. CM =nV
C. CM =Vn
D. CM = 1n.V
Đáp án B
Câu 10: Công thức liên hệ giữa nồng độ mol và nồng độ phần trăm của dung dịch là:
A. CM =C%.mddV.M.100%
B. CM = C%.100
C. CM = C%mdd.V.M.100%
D. CM = V.M.C%
Hướng dẫn giải:
Nồng độ phần trăm dung dịch là:
C% = mctmdd.100%
Suy ra mct = C%.mdd100% mà mct = n.M và CM =nV
Vậy CM =C%.mddV.M.100%
Đáp án A
Câu 11: Cho dung dịch HCl 40% có d = 1,198 g/ml. Tính nồng độ mol của dung dịch đã cho.
A. 10,13M
B. 11,13M
C. 12,13M
D. 13,13M
Hướng dẫn giải:
Đổi d = 1,198 g/ml = 1198 g/l
Áp dụng công thức liên hệ giữa nồng độ mol và nồng độ phần trăm của dung dịch ta có:
CM = C%.mddV.M.100% mà mdd = d.V
Vậy nồng độ mol của dung dịch đã cho là:
CM = C%.dM.100% = 40%.119836,5.100% = 13,13M
Đáp án D
Câu 12: Trộn 1 lít dung dịch H2SO4 2M vào 2 lít dung dịch H2SO4 0,125M. Nồng độ mol của dung dịch sau khi trộn là
A. 0,13M
B. 0,14M
C. 0,15M
D. 0,16M
Hướng dẫn giải:
Số mol H2SO4 có trong dung dịch sau khi trộn là: n = 2.0,1 + 0,125.2 = 0,45 mol
Thể tích của dung dịch sau khi trộn là: V = 1 + 2 = 3 lít
Nồng độ mol của dung dịch H2SO4 sau khi trộn là: CM = nV = 0,453 = 0,15M
Đáp án C
Xem thêm Công thức Hóa học lớp 8, 9 đầy đủ, chọn lọc chi tiết khác:
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
