C2H7N (Etylamin) là gì? Tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng của C2H7N (Etylamin)
Tổng hợp Tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng của C2H7N (Etylamin) giúp bạn nắm vững kiến thức và học tốt Hóa học.
C2H7N (Etylamin) là gì?

1. Định nghĩa Etylamin
- Định nghĩa: Etylamin là một hợp chất hữu cơ thuộc chức amin được tạo ra khi thế một nguyên tử hiđro trong phân tử amoniac bằng một gốc etyl
- Công thức phân tử: C2H7N
- Công thức cấu tạo: CH3CH2NH2
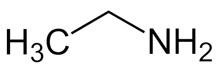
- Tên gọi
+ Tên gốc chức: Etylamin
+ Tên thay thế: Etanamin
2. Tính chất vật lí của Etylamin
Etylamin là chất khí có mùi khai khó chịu, độc, tan tốt trong nước
3. Tính chất hoá học của Etylamin
3.1. Tính bazơ
- Dung dịch Etylamin có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein do kết hợp với proton mạnh hơn amoniac
- Amin có tính bazo yếu nên có thể phản ứng với các axit vô cơ để tạo thành muối
3.2. Phản ứng với axit nitrơ
C2H5-NH2 + HONO → C2H5-OH + N2 + H2O (xúc tác HCl)
3.3. Phản ứng ankyl hóa
C2H5NH2 + CH3I → C2H5-NH-CH3 + HI
3.4. Phản ứng với dung dịch muối của các kim loại có hiđroxit kết tủa
3C2H5NH2 + FeCl3 + 3H2O → Fe(OH)3 + 3C2H5NH3Cl
4. Điều chế Etylamin
- Etylamin có thể được điều chế trong phòng thí nghiệm bằng phản ứng của etylen với amoniac với sự hiện diện của chất xúc tác là amit kim loại kiềm như amit natri
H2C=CH2 + NH3 → CH3CH2NH2
- Nó cũng có thể tổng hợp từ etanal và clorua amoni
2CH3CHO + NH4Cl → CH3CH2NH3Cl + CH3COOH
CH3CH2NH3Cl + NaOH → CH3CH2NH2 + NaCl + H2O
5. Ứng dụng Etylamin
- Etylamin được sử dụng rộng rãi trong công nghiệp hóa chất và tổng hợp hữu cơ
- Etylamin, giống như một vài amin khác, có tính chất bất thường là hòa tan liti kim loại để tạo ra ion [Li(amin)4]+ và electron sonvat hóa. Làm bay hơi dung dịch này sẽ thu lại được liti kim loại. Các dung dịch như thế được sử dụng trong khử các hợp chất hữu cơ chưa no, như naphtalen
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)
