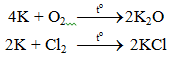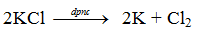Kali (K) là gì? Tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng của Kali (K)
Tổng hợp Tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng của Kali (K) giúp bạn nắm vững kiến thức và học tốt Hóa học.
Kali (K) là gì?

1. Định nghĩa
- Kali là một kim loại kiềm được phát hiện bởi Sir Humphry Davy năm 1807, ông tách nó ra từ dung dịch KOH. Kim loại kiềm này là kim loại đầu tiên được điều chế bằng điện phân.
- Kí hiệu: K
- Cấu hình electron: [Ar] 4s1
- Số hiệu nguyên tử: 19
- Khối lượng nguyên tử: 39 g/mol
- Vị trí trong bảng tuần hoàn
+ Ô: số 19
+ Nhóm: IA
+ Chu kì: 4
- Đồng vị: 39K, 40K, 41K.
- Độ âm điện: 0,82
2. Tính chất hóa học
- Kali là kim loại kiềm có tính khử rất mạnh.
K → K+ + 1e
a. Tác dụng với phi kim
b. Tác dụng với axit
2K + 2HCl → 2KCl + H2.
c. Tác dụng với nước
- K tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
d. Tác dụng với hidro
- Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
3. Tính chất vật lí
- Kali là kim loại nhẹ thứ hai sau liti, là chất rắn rất mềm, dễ dàng cắt bằng dao và có màu trắng bạc.
- Kali bị ôxi hóa rất nhanh trong không khí và phải được bảo quản trong dầu mỏ hay dầu lửa.
- Có khối lượng riêng là 0,863 g/cm3; có nhiệt độ nóng chảy là 63,510C và sôi ở 7600C.
4. Nhận biết
- Đốt cháy các hợp chất của Kali, cho ngọn lửa màu tím.
5. Trạng thái tự nhiên
- Dạng tự nhiên của K có 3 đồng vị: K39 (93,3%), K40(0,01%) và K41 (6,7%).
- Nguyên tố này chiếm khoảng 2,4% trọng lượng lớp vỏ Trái Đất và là nguyên tố phổ biến thứ bảy trong lớp này. Vì tính không hòa tan của nó, rất khó thu được kali từ các khoáng chất của nó.
6. Điều chế
- Kali có thể điều chế nhờ điện phân nóng chảy kali clorua
7. Ứng dụng
- Các loại phân hóa học chứa kali như clorua kali, sulfat kali, cacbonat kali v.v ………
+ Nitrat kali được sử dụng trong thuốc súng.
+ Cacbonat kali được sử dụng trong sản xuất thủy tinh.
+ Thủy tinh được xử lý bằng kali lỏng là có độ bền cao hơn so với thủy tinh thường.
+ NaK là hợp kim của kali với natri được sử dụng như là chất truyền nhiệt trung gian.
+ Nguyên tố này là thành phần rất cần thiết cho sự phát triển của cây cối và được tìm thấy trong nhiều loại đất
8. Các hợp chất quan trọng của Kali
- Kali hiđroxit: KOH
9. Bài tập về Kali
Bài tập 1: Chất nào sau đây không phải là đạm amoni?
A. NH4Cl.
B. NH4NO3.
C. (NH4)2SO4.
D. NaNO3.
Đáp án D: NaNO3 thuộc đạm nitrat.
Bài tập 2: Một loại phân supephotphat kép có chứa 69,62% muối canxi đihiđrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là
A. 48,52%.
B. 42,25%.
C. 39,76%.
D. 45,75%.
Đáp án B: Ca(H2PO4)2 → P2O5
100 gam phân lân có 69,62 gam Ca(H2PO4)2 (≈ 0,2975 mol)
⇒ nP2O5 = 0,2975 mol ⇒ mP2O5 = 0,2975.142 = 42,25g
Bài tập 3: Phân đạm cung cấp N cho cây dưới dạng
A. N2.
B. NHNO3.
C. NH3.
D. NH4+, NO3-.
Đáp án D: Phân đạm cung cấp nitơ cho cây dưới dạng NH4+, NO3-.
Bài tập 4: Loại phân nào thì thu được khi nung hỗn hợp quặng apatit với đá xà vân và than cốc?
A. Phân supephotphat.
B. Phân phức hợp.
C. Phân lân nung chảy.
D. Phân apatit.
Đáp án C: Phân lân nung chảy thu được khi nung hỗn hợp quặng apatit với đá xà vân và than cốc.
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)