Anken là gì? Tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng của Anken
Tổng hợp Tính chất hóa học, tính chất vật lí, nhận biết, điều chế, ứng dụng của Anken giúp bạn nắm vững kiến thức và học tốt Hóa học.
Anken là gì?

1. Định nghĩa Anken
Anken là hiđrocacbon không no, mạch hở trong phân tử có chứa các liên kết đơn và 1 liên kết đôi C=C.
2. Cấu trúc của Anken
- Hai nguyên tử C mang nối đôi ở trạng thái lai hóa sp2 (lai hóa tam giác). Liên kết đôi ở phân tử anken gồm một liên kết σ và một liên kết π. Liên kết σ được tạo thành do sự xen phủ trục (2 obitan lai hóa sp2) nên tương đối bền vững. Liên kết π được tạo thành do sự xen phủ bên (2 obitan p) nên kém bền hơn so với liên kết σ. Hai nhóm nguyên tử liên kết với nhau bởi liên kết đôi không quay tự do được quanh trục liên kết (do bị cản trở bởi liên kết π).
- Ở phân tử etilen, hai nguyên tử C và 4 nguyên tử H đều nằm cùng trên một mặt phẳng (gọi là mặt phẳng phân tử), các góc hầu như bằng nhau và gần bằng 120 độ.
3. Đồng phân Anken
3.1. Đồng phân cấu tạo
Anken từ C4 trở lên có đồng phân mạch cacbon và đồng phân vị trí liên kết đôi.
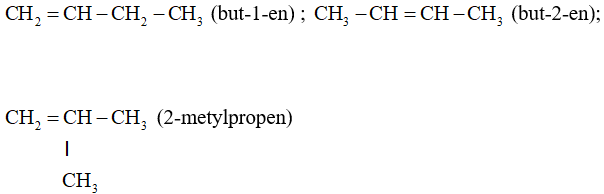
3.2. Đồng phân hình học
- Anken từ C4 trở nên nếu mỗi C mang liên kết đôi đính với 2 nhóm nguyên tử khác nhau thì sẽ có hai cách phân bố không gian khác nhau dẫn tới 2 đồng phân hình học.
- Nếu mạch chính nằm cùng một phía của liên kết thì gọi là đồng phân cis. Nếu mạch chính nằm ở hai phía khác nhau của liên kết thì gọi là đồng phân trans. Thí dụ:
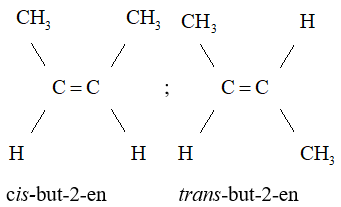
4. Đồng đẳng Anken
- Etilen (C2H4), propilen (C3H6), butilen (C4H8) ,... đều có một liên kết đôi C=C, có công thức chung là CnH2n) (n ≥ 2). Chúng hợp thành dãy đồng đẳng gọi là dãy đồng đẳng của etilen.
- Tên của một số anken đơn giản lấy từ tên của ankan tương ứng nhưng đổi đuôi an thành đuôi ilen. Thí dụ:
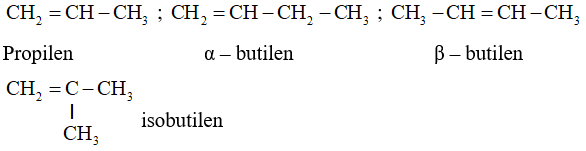
- Nhóm CH2=CH- được gọi là nhóm vinyl.
5. Danh pháp Anken
Số chỉ vị trí – Tên nhánh + Tên mạch chính – số chỉ vị trí + en
- Mạch chính là mạch chứa liên kết đôi, dài nhất và có nhiều nhánh nhất.
- Đánh số C mạch chính bắt đầu từ phía gần liên kết đôi hơn.
- Số chỉ vị trí liên kết đôi ghi ngay trước đuôi en (khi mạch chính chỉ có 2 hoặc 3 nguyên tử cacbon thì không cần ghi).
Thí dụ:
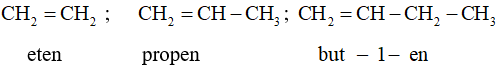
6. Tính chất hoá học của Anken
Liên kết π ở nối đôi của anken kém bền vững, nên trong phản ứng dễ bị đứt ra để tạo liên kết σ với các nguyên tử khác. Vì thế, liên kết đôi là trung tâm phản ứng gây ra những phản ứng hóa học đặc trưng cho anken như phản ứng cộng, phản ứng trùng hợp và phản ứng oxi hóa.
6.1. Phản ứng cộng
- Phản ứng cộng halogen (phản ứng halogen hóa)
Cộng brom
- Dẫn khí etilen qua dung dịch brom màu da cam
- Hiện tượng: Dung dịch brom bị mất màu.
- Nhận xét: Etilen đã phản ứng với brom trong dung dịch.
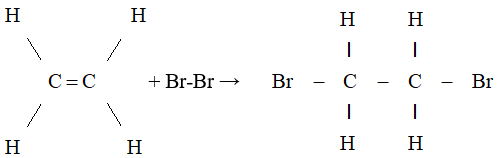
- Liên kết kém bền trong liên kết đôi bị đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom. Phản ứng trên được gọi là phản ứng cộng.
- Ngoài brom, trong những điều kiện thích hợp, etilen còn có phản ứng cộng với một số chất khác. Ví dụ hiđro, clo.
- Nhìn chung, các chất có liên kết đôi (tương tự như etilen) dễ tham gia phản ứng cộng.
Cộng clo
![]()
- Phản ứng cộng hiđro (phản ứng hiđro hóa)
![]()
- Phản ứng cộng axit
+ Hiđro halogenua (HCl, HBr, HI), axit sunfuric đậm đặc ,... có thể cộng vào etilen.
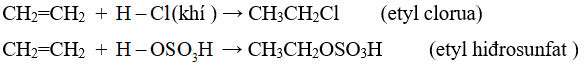
- Phản ứng cộng nước (phản ứng hiđrat hóa). Ở nhiệt độ thích hợp và có xúc tác axit, etilen có thể cộng nước.
![]()
=> Hướng của phản ứng cộng axit và nước vào anken
- Phản ứng cộng axit hoặc nước vào anken bất đối xứng thường tạo ra hỗn hợp hai đồng phân, trong đó có một đồng phân là sản phẩm chính. Thí dụ:
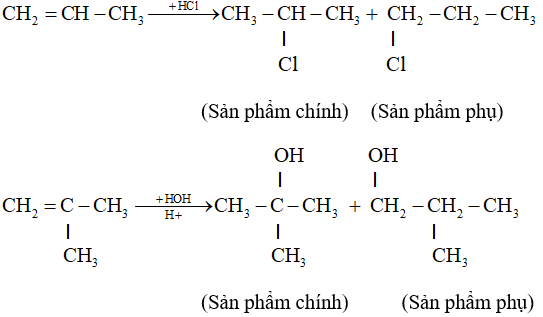
6.2. Phản ứng trùng hợp
- Các anken ở đầu dãy như etilen, propilen, butilen trong những điều kiện nhiệt độ, áp suất, xúc tác thích hợp thì tham gia phản ứng cộng nhiều phân tử với nhau thành những phân tử mạch rất dài và có khối lượng phân tử rất lớn.
![]()
- Phản ứng trên được gọi là phản ứng trùng hợp.
- Polietilen là chất rắn, không tan trong nước, không độc. Nó là nguyên liệu quan trọng trong công nghiệp chất dẻo.
6.3. Phản ứng oxi hóa
- Giống với ankan, anken cháy hoàn toàn tạo ra CO2, H2O và tỏa nhiều nhiệt:
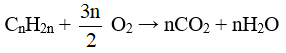
- Khác với ankan, anken làm mất màu dung dịch KMnO4:
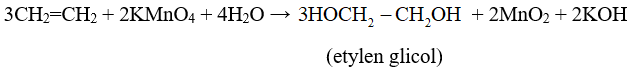
- Phản ứng làm mất màu dung dịch thuốc tím kali pemanganat được dùng để nhận ra sự có mặt của liên kết đôi của anken.
7. Tính chất vật lí của Anken
- Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng của anken không khác nhiều so với ankan tương ứng và thường nhỏ hơn so với xicloankan có cùng có nguyên tử cacbon.
- Ở điều kiện thường, anken từ C2 đến C4 là chất khí. Nhiệt độ sôi, nhiệt độ nóng chảy tăng theo khối lượng mol phân tử. Các anken đều nhẹ hơn nước.
- Anken hòa tan tốt trong dầu mỡ. Anken hầu như không tan trong nước và là những chất không màu.
8. Điều chế Anken
- Trong công nghiệp, etilen, propilen và butilen được điều chế bằng phản ứng tách hiđro từ ankan tương ứng hoặc bằng phản ứng crackinh.
- Trong phòng thí nghiệm, etilen được điều chế bằng cách đun etanol với axit sunfuric đậm đặc:
![]()
9. Ứng dụng Anken
- Trong các hợp chất hữu cơ do con người sản xuất thì etilen đứng hàng đầu về sản lượng. Sở dĩ như vậy vì etilen cũng là nguyên liệu quan trọng của công nghiệp tổng hợp polime và các hợp chất hữu cơ khác.
- Tổng hợp polime
+ Trùng hợp etilen người ta thu được các polime để chế tạo màng mỏng.... dùng cho nhiều mục đích khác nhau.
+ Chuyển hóa etilen thành các monome khác để tổng hợp ra hàng loạt polime đáp ứng nhu cầu phong phú của đời sống và kĩ thuật.
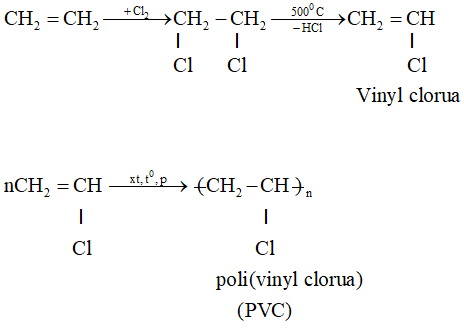
- Tổng hợp các hóa chất khác: Từ etilen tổng hợp ra những hóa chất hữu cơ thiết yếu như etanol, etilen oxit, etylen glicol, anđehit axetic,....
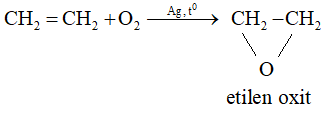
- Etilen dùng để kích thích quả mau chín.
10. Bài tập về Anken
Ví dụ 1: 2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Hiđrat hóa X chỉ thu được một ancol duy nhất. X có tên là
A. etilen.
B. but-2-en.
C. hex-2-en.
D. 2,3-đimetylbut-2-en.
Hướng dẫn giải
Vì hiđrat hóa A chỉ thu được 1 ancol duy nhất A là CH3-CH=CH-CH3 (but-2-en)
Đáp án B
Ví dụ 2: Hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với He là 3,75. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với He là 5. Tính hiệu suất của phản ứng hiđro hoá?
A. 20%
B. 25%
C. 50%
D. 40%
Hướng dẫn giải
C2H4 (M = 28) 13
H2 (M = 2) 13
Hiệu suất tính theo anken hoặc H2 đều được
Giả sử:
Mà
Đáp án C
Ví dụ 3: Dẫn 3,36 lít hỗn hợp X gồm 2 anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7 gam. Tìm CTPT của 2 anken?
A. C3H6 và C4H8
B. C4H8 và C5H10
C. C5H10 và C6H12
D. C3H6 và C5H10
Hướng dẫn giải
CnH2n + Br2 → CnH2nBr2
Khối lượng bình brom tăng bằng khối lượng của 2 anken:
CTPT của 2 anken kế tiếp là: C3H6 và C4H8
Đáp án A
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2024) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2024)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2024)
