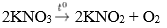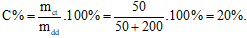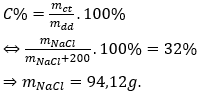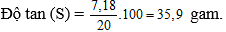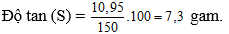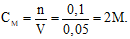TOP 40 câu Trắc nghiệm Một số muối quan trọng (có đáp án 2024) – Hóa học 9
Bộ 40 bài tập trắc nghiệm Hóa học lớp 9 Bài 10: Một số muối quan trọng có đáp án đầy đủ các mức độ giúp các em ôn trắc nghiệm Hóa học 9.
Trắc nghiệm Hóa học 9 Bài 10: Một số muối quan trọng
Bài giảng Hóa học 9 Bài 10: Một số muối quan trọng
Câu 1: Trong tự nhiên muối natri clorua có nhiều trong
A. Nước mưa
B. Nước sông
C. Nước giếng
D. Nước biển
Đáp án: D
Giải thích: NaCl có nhiều trong tự nhiên, dưới dạng hòa tan trong nước biển.
Câu 2: Nung kali nitrat ở nhiệt độ cao, sau phản ứng thu được chất khí là
A. N2O
B. NO2
C. O2
D. NO
Đáp án: C
Giải thích:
Phương trình phản ứng:
2KNO3 2KNO2 + O2
Câu 3: Hòa tan 14,625 gam NaCl vào nước thu được 200 ml dung dịch. Dung dịch tạo thành có nồng độ mol là
A. 0,75M
B. 1,12M
C. 0,50M
D. 1,25M
Đáp án: D
Giải thích:
200 ml = 0,2 lít
Số mol của NaCl là:
nNaCl = = 0,25 mol
Nồng độ mol dung dịch tạo thành là:
CM = = 1,25M
Câu 4: Cách khai thác natri clorua là
A. Ở những nơi có biển hoặc hồ nước mặn, người ta khai thác NaCl từ nước mặn trên. Cho nước mặn bay hơi từ từ, thu được muối kết tinh
B. Ở những nơi có mỏ muối, người ta đào hầm hoặc giếng sâu đến mỏ muối để lấy muối lên
C. Muối mỏ sau khi khai thác, được nghiền nhỏ và tinh chế để có muối sạch
D. A, B đều đúng
Đáp án: D
Giải thích:
Cách khai thác natri clorua là
+ Ở những nơi có biển hoặc hồ nước mặn, người ta khai thác NaCl từ nước mặn trên. Cho nước mặn bay hơi từ từ, thu được muối kết tinh
+ Ở những nơi có mỏ muối, người ta đào hầm hoặc giếng sâu đến mỏ muối để lấy muối lên.
Ý C loại vì minh họa cho cách chế biến muối.
Câu 5: Hòa tan 15 gam KNO3 vào 110 gam nước, thu được dung dịch A có nồng độ phần trăm là
A. 12%
B. 13%
C. 14%
D. 15%
Đáp án: A
Giải thích:
Nồng độ phần trăm của dung dịch A là:
Câu 6: Ứng dụng của muối kali nitrat là
A. Chế tạo thuốc nổ đen
B. Làm phân bón (cung cấp nguyên tố nitơ và kali cho cây trồng)
C. Bảo quản thực phẩm trong công nghiệp
D. A, B, C đều đúng
Đáp án: D
Giải thích:
Ứng dụng của muối kali nitrat là
+ Chế tạo thuốc nổ đen
+ Làm phân bón (cung cấp nguyên tố nitơ và kali cho cây trồng)
+ Bảo quản thực phẩm trong công nghiệp
Câu 7: Muối kali nitrat (KNO3)
A. Tan nhiều trong nước
B. Tan rất ít trong nước
C. Không tan trong nước
D. Không bị phân hủy ở nhiệt độ cao
Đáp án: A
Giải thích:
Muối kali nitrat (KNO3) là chất rắn màu trắng, tan nhiều trong nước.
Muối KNO3 bị phân hủy ở nhiệt độ cao, tạo muối KNO2 và giải phóng oxi.
2KNO3 2KNO2 + O2
Câu 8: Để có được dung dịch NaCl 10% thì khối lượng NaCl cần lấy hòa tan vào 108 gam nước là
A. 11 gam
B. 12 gam
C. 13 gam
D. 14 gam
Đáp án: B
Giải thích:
Ta có:
Suy ra 0,9mNaCl = 10,8
Vậy mNaCl = 12 gam
Câu 9: Để loại bớt muối Na2SO4 có lẫn trong dung dịch NaCl ta dùng
A. Dung dịch AgNO3.
B. Dung dịch HCl.
C. Dung dịch BaCl2.
D. Dung dịch H2SO4
Đáp án: C
Giải thích:
Sử dụng dung dịch BaCl2:
Na2SO4 + BaCl2 → BaSO4 (↓ trắng) + 2NaCl
Sau đó lọc bỏ kết tủa.
Câu 10: Hoà tan 40 gam muối ăn vào 160 gam nước thu được dung dịch có nồng độ là
A. 10%
B. 15%
C. 20%
D. 25%
Đáp án: C
Giải thích:
Nồng độ dung dịch thu được là:
Câu 11: Muối nào có thể điều chế bằng phản ứng của dung dịch muối cacbonat với dung dịch axit clohidric?
A. KNO3
B. ZnSO4
C. CaCO3
D. NaCl
Đáp án: D
Giải thích:
Muối có thể điều chế bằng phản ứng của dung dịch muối cacbonat với dung dịch axit clohidric là NaCl.
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Câu 12: Cho các phát biểu sau:
(1) Natri clorua có trong nước biển.
(2) KNO3 là chất rắn, không tan trong nước.
(3) KNO3 dùng chế tạo thuốc nổ, làm phân bón, bảo quản thực phẩm trong công nghiệp.
(4) Muối không độc nhưng cũng không được có trong nước ăn vì vị mặn của nó là NaCl.
Số phát biểu đúng là
A. 4
B. 3
C. 2
D. 1
Đáp án: B
Giải thích:
Số phát biểu đúng là (1), (3), (4)
Phát biểu (2) sai vì KNO3 là chất rắn, tan nhiều trong nước.
Câu 13: Nhiệt phân hoàn toàn 40,4 gam kali nitrat (KNO3) thu được V lít khí O2 ở đktc. Giá trị của V là
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Đáp án: D
Giải thích:
Số mol KNO3 là:
= 0,4 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có:
= 0,2 mol
Thể tích khí O2 là:
V = 0,2.22,4 = 4,48 lít
Câu 14: Muối nào sau đây bị nhiệt phân hủy?
A. Na2CO3
B. KCl
C. NaCl
D. KNO3
Đáp án: D
Giải thích:
Phương trình phản ứng:
2KNO3 2KNO2 + O2
Câu 15: Phương trình điện phân dung dịch muối ăn (có màng ngăn xốp) là
A. 2NaCl + 2H2O 2NaOH + H2 + Cl2
B. 2NaCl + 2H2O 2NaOH + 2HCl
C. 2NaCl + 3H2O 2NaOH + 2H2 + 2Cl2
D. 2NaCl + 2H2O 2NaOH + H2 + O2
Đáp án: A
Giải thích:
Phương trình phản ứng:
2NaCl + 2H2O 2NaOH + H2 + Cl2
Câu 16: Trong tự nhiên muối natri clorua có nhiều trong:
A. Nước biển.
B. Nước mưa.
C. Nước sông.
D. Nước giếng.
Đáp án: A
Câu 17: Nung kali nitrat (KNO3) ở nhiệt độ cao, ta thu được chất khí là
A. NO.
B. N2O
C. N2O5
D. O2.
Đáp án: D
Giải thích:
Câu 18: Muối kali nitrat (KNO3):
A. Không tan trong trong nước.
B. Tan rất ít trong nước.
C. Tan nhiều trong nước.
D. Không bị phân huỷ ở nhiệt độ cao.
Đáp án: C
Câu 19: Điện phân dung dịch natri clorua (NaCl) bão hoà trong bình điện phân có màng ngăn ta thu được hỗn hợp khí là:
A. H2 và O2.
B. H2 và Cl2.
C. O2 và Cl2.
D. Cl2 và HCl
Đáp án: B
Giải thích:
Câu 20: Để loại bớt muối Na2SO4 có lẫn trong dung dịch NaCl ta dùng:
A. Dung dịch AgNO3.
B. Dung dịch HCl.
C. Dung dịch BaCl2.
D. Dung dịch H2SO4
Đáp án: C
Giải thích:
Sử dụng dung dịch BaCl2:
Na2SO4 + BaCl2 → BaSO4 (↓ trắng) + 2NaCl
Sau đó lọc bỏ kết tủa.
Câu 21: Hoà tan 50 gam muối ăn vào 200 gam nước thu được dung dịch có nồng độ là:
A. 15%.
B. 20%.
C. 18%.
D. 25%
Đáp án: B
Giải thích:
Câu 22: Để có được dung dịch NaCl 32%, thì khối lượng NaCl cần lấy hoà tan vào 200 gam nước là:
A. 90g.
B. 94,12 g.
C. 100g.
D. 141,18 g.
Đáp án: B
Giải thích:
Câu 23: Hoà tan 7,18 gam muối NaCl vào 20 gam nước ở 20°C thì được dung dịch bão hoà. Độ tan của NaCl ở nhiệt độ đó là:
A. 35g.
B. 35,9g.
C. 53,85g.
D. 71,8g.
Đáp án: B
Giải thích:
Câu 24: Hoà tan 10,95 g KNO3 vào 150g nước thì được dung dịch bão hoà ở 20°C, độ tan của KNO3 ở nhiệt độ này là:
A. 6,3g.
B. 7 g
C. 7,3 g
D. 7,5 g.
Đáp án: C
Giải thích:
Câu 25: Hoà tan 5,85 g natri clorua vào nước thu được 50 ml dung dịch. Dung dịch tạo thành có nồng độ mol là:
A. 1M.
B. 1,25M.
C. 2M.
D. 2.75M.
Đáp án: C
Giải thích:
nNaCl = 5,85 : 58,5 = 0,1 mol
Đổi 50 ml = 0,05 lít.
Các câu hỏi trắc nghiệm Hóa học lớp 9 có đáp án, chọn lọc khác:
Trắc nghiệm Phân bón hóa học có đáp án
Trắc nghiệm Mối liên hệ giữa các loại chất vô cơ có đáp án
Trắc nghiệm Luyện tập chương 1: Các hợp chất vô cơ có đáp án
Xem thêm các chương trình khác:
- Trắc nghiệm Sinh học lớp 7 có đáp án
- Trắc nghiệm Toán lớp 7 có đáp án
- Trắc nghiệm Ngữ văn lớp 7 có đáp án
- Trắc nghiệm Sinh học 8 có đáp án
- Trắc nghiệm Toán lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Ngữ văn 8 có đáp án
- Trắc nghiệm Hóa học lớp 8 có đáp án
- Trắc nghiệm Địa Lí lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Tiếng Anh lớp 8 có đáp án
- Trắc nghiệm GDCD lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Lịch sử lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Vật Lí lớp 8 có đáp án
- Trắc nghiệm Công nghệ lớp 8 có đáp án
- Trắc nghiệm Tin học lớp 8 có đáp án
- Trắc nghiệm Sinh học lớp 10 có đáp án
- Trắc nghiệm Toán lớp 10 có đáp án
- Trắc nghiệm Hóa học lớp 10 có đáp án
- Trắc nghiệm Ngữ văn lớp 10 có đáp án
- Trắc nghiệm Vật Lí lớp 10 có đáp án
- Trắc nghiệm Tiếng Anh lớp 10 có đáp án
- Trắc nghiệm Sinh học lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Toán lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Hóa học lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Ngữ văn lớp 11 có đáp án
- Trắc nghiệm Tiếng Anh lớp 11 có đáp án
- Trắc nghiệm Vật Lí lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Địa lí lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm GDCD lớp 11 có đáp án
- Trắc nghiệm Lịch sử lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Công nghệ lớp 11 có đáp án
- Trắc nghiệm Giáo dục quốc phòng - an ninh lớp 11 có đáp án
- Trắc nghiệm Tin học lớp 11 có đáp án
- Trắc nghiệm Toán lớp 12 có đáp án
- Trắc nghiệm Sinh học lớp 12 có đáp án
- Trắc nghiệm Hóa học lớp 12 có đáp án
- Trắc nghiệm Ngữ văn lớp 12 có đáp án
- Trắc nghiệm Tiếng Anh lớp 12 có đáp án
- Trắc nghiệm Địa lí lớp 12 có đáp án
- Trắc nghiệm Vật Lí lớp 12 có đáp án
- Trắc nghiệm Công nghệ lớp 12 có đáp án
- Trắc nghiệm Giáo dục công dân lớp 12 có đáp án
- Trắc nghiệm Lịch sử lớp 12 có đáp án
- Trắc nghiệm Giáo dục quốc phòng - an ninh lớp 12 có đáp án