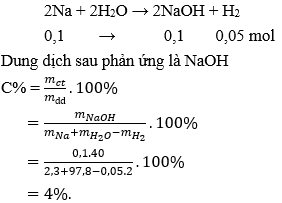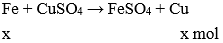TOP 40 câu Trắc nghiệm Luyện tập chương 2: Kim loại (có đáp án 2024) - Hóa học 9
Bộ 40 bài tập trắc nghiệm Hóa học lớp 9 Bài 22: Luyện tập chương 2: Kim loại có đáp án đầy đủ các mức độ giúp các em ôn trắc nghiệm Hóa học 9.
Trắc nghiệm Hóa học 9 Bài 22: Luyện tập chương 2: Kim loại
Bài giảng Hóa học 9 Bài 22: Luyện tập chương 2: Kim loại
Câu 1: Trong các kim loại sau, kim loại hoạt động mạnh nhất là
A. Cu.
B. Pb.
C. Al.
D. Na.
Đáp án: D
Giải thích:
Dãy hoạt động hóa học của một số kim loại:
K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au.
Vậy trong các kim loại đề bài cho thì Na hoạt động mạnh nhất.
Câu 2: Dung dịch ZnCl2 có lẫn dung dịch CuCl2. Kim loại nào dùng để làm sạch dung dịch ZnCl2
A. Ba.
B. Zn.
C. Cu.
D. Mg.
Đáp án: B
Giải thích:
Sử dụng một lượng dư kim loại kẽm cho vào dung dịch, có phản ứng hóa học sau:
Zn + CuCl2 → ZnCl2 + Cu
Kết thúc phản ứng, lọc bỏ kim loại thu được dung dịch ZnCl2 tinh khiết.
Câu 3: Những tính chất vật lý đặc trưng của kim loại là
A. Có tính ánh kim, nhiệt độ nóng chảy cao.
B. Dẫn điện, dẫn nhiệt, độ rắn cao.
C. Độ rắn cao, khối lượng riêng lớn.
D. Dẻo, có ánh kim, dẫn điện, dẫn nhiệt.
Đáp án: D
Giải thích: Kim loại có tính dẻo, dẫn điện, dẫn nhiệt và có ánh kim.
Câu 4: Kim loại dùng để làm sạch đồng nitrat có lẫn bạc nitrat là
A. Sắt (Fe).
B. Đồng (Cu).
C. Kali (K).
D. Bạc (Ag).
Đáp án: B
Giải thích:
Sử dụng một lượng dư kim loại đồng cho vào dung dịch, có phản ứng hóa học sau:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Kết thúc phản ứng, lọc bỏ kim loại thu được dung dịch Cu(NO3)2 tinh khiết.
Câu 5: Khi cho kim loại Mg (dư) vào dung dịch gồm 2 muối Cu(NO3)2 và AgNO3, sản phẩm thu được gồm
A. Hai kim loại và một muối.
B. Hai kim loại và hai muối.
C. Ba kim loại và một muối.
D. Ba kim loại và hai muối.
Đáp án: C
Giải thích:
Cho kim loại Mg (dư) vào dung dịch gồm 2 muối Cu(NO3)2 và AgNO3 có các phản ứng hóa học xảy ra như sau:
Mg + 2AgNO3 → Mg(NO3)2 + 2Ag
Mg + Cu(NO3)2 → Mg(NO3)2 + Cu
Sau phản ứng thu được 3 kim loại: Ag, Cu, Mg (dư) và 1 muối duy nhất Mg(NO3)2
Câu 6: Thả một mảnh nhôm vào ống nghiệm chứa dung dịch CuSO4 . Xảy ra hiện tượng:
A. Không có dấu hiệu phản ứng
B. Có chất rắn màu trắng bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
C. Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
D. Có chất khí bay ra, dung dịch không đổi màu
Đáp án: C
Giải thích:
Nhôm đứng trước đồng trong dãy hoạt động hóa học do đó sẽ đẩy đồng ra khỏi muối
3CuSO4 + 2Al → 3Cu↓ + Al2(SO4)3
Hiện tượng: Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
Câu 7: Cho hỗn hợp bột gồm: Al, Fe, Mg và Cu vào dung dịch HCl dư, sau phản ứng thu được chất rắn T không tan. Vậy T là
A. Al.
B. Fe.
C. Mg.
D. Cu.
Đáp án: D
Giải thích: Cu là kim loại đứng sau H trong dãy điện hóa nên không tan trong dd HCl ⇒ chất rắn T là Cu
Câu 8: Nhúng một thanh sắt vào dung dịch CuSO4, sau một thời gian thấy khối lượng chất rắn tăng 1,6 gam. Số mol CuSO4 đã tham gia phản ứng là
A. 0,1 mol.
B. 0,2 mol.
C. 0,3 mol.
D. 0,4 mol.
Đáp án: B
Giải thích:
Gọi số mol CuSO4 phản ứng là x (mol).
Phương trình hóa học:
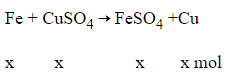
Khối lượng chất rắn tăng 1,6 gam.
m(tăng) = mCu – mFe
= MCu .nCu – MFe . nFe
1,6 = 64x – 56x = 8x
x = 0,2 (mol)
Câu 9: Hoà tan 16,8g kim loại hoá trị II vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H2 (đktc). Kim loại đem hoà tan là:
A. Mg.
B. Zn.
C. Pb.
D. Fe.
Đáp án: D
Giải thích:
Gọi A là kim loại cần tìm
A + 2HCl → ACl2 + H2
0,3→ 0,3mol

⇒ A là sắt
Câu 10: Kim loại vừa tác dụng với dd HCl vừa tác dụng được với dung dịch KOH:
A. Fe, Al
B. Ag, Zn
C. Al, Cu
D. Al, Zn
Đáp án: D
Giải thích:
Al, Zn vừa tác dụng với HCl vừa tác dụng với KOH
Phương trình hóa học minh họa:
2Al + 6 HCl → 2AlCl3 + 3H2
2Al + 2NaOH + 2H2O→2NaAlO2 + 3H2
Zn + 2HCl → ZnCl2 + H2
Zn + 2NaOH → Na2ZnO2 + H2
Câu 11: Có một mẫu Fe bị lẫn tạp chất là nhôm, để làm sạch mẫu sắt này bằng cách ngâm nó với
A. Dung dịch NaOH dư.
B. Dung dịch H2SO4 loãng.
C. Dung dịch HCl dư.
D. Dung dịch HNO3 loãng.
Đáp án: A
Giải thích:
Sử dụng một lượng dư dung dịch NaOH
2Al + 2H2O + 2NaOH → 2NaAlO2 + 3H2
Lọc lấy kim loại rửa sạch thu được Fe tinh khiết.
Chú ý: Một số kim loại như Al, Zn … có thể tác dụng được với dung dịch kiềm.
Câu 12: Hòa tan 12g hỗn hợp gồm Al, Ag vào dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H2 (ở đktc). Thành phần % khối lượng của Al, Ag trong hỗn hợp lần lượt là
A. 70% và 30%.
B. 10% và 90%.
C. 90% và 10%.
D. 30% và 70%.
Đáp án: C
Giải thích:
Cho Al, Ag phản ứng với H2SO4 loãng, dư chỉ có Al phản ứng:
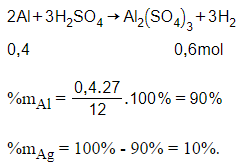
Câu 13: Đốt cháy hoàn toàn 1,35 gam nhôm trong oxi. Khối lượng nhôm oxit tạo thành và khối lượng oxi đã tham gia phản ứng là
A. 2,25 gam và 1,2 gam.
B. 2,55 gam và 1,2 gam.
C. 2,55 gam và 1,28 gam.
D. 2,7 gam và 3,2 gam.
Đáp án: B
Giải thích:
PTHH:
4Al + 3O2 → 2Al2O3
4 3 2
0,05 ? ?mol
Theo phương trình hóa học ta có:
Câu 14: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al2O3 trong dung dịch HCl dư. Sau phản ứng, người ta thu được 0,6 gam khí H2. Khối lượng muối AlCl3 thu được là
A. 53,4 gam.
B. 79,6 gam.
C. 80,1 gam.
D. 25,8 gam.
Đáp án: C
Giải thích:
Chỉ có Al tác dụng với HCl mới tạo ra khí H2 còn Al2O3 thì không.
Phương trình hóa học:
Xét cả 2 phương trình hóa học:
Tổng số mol AlCl3 là
Câu 15: Để khử hoàn toàn 8 gam Fe2O3 bằng bột nhôm ở nhiệt độ cao, trong điều kiện không có không khí thì khối lượng bột nhôm cần dùng là
A. 2,7 gam.
B. 4,05 gam.
C. 5,40 gam.
D. 6,75 gam.
Đáp án: A
Giải thích:

Câu 16: Trong các kim loại sau đây, kim loại dẫn điện tốt nhất là:
A. Nhôm (Al)
B. Bạc (Ag)
C. Đồng (Cu)
D. Magie (Mg)
Đáp án: B
Câu 17: Trong các kim loại sau đây, kim loại dẻo nhất là:
A. Đồng (Cu)
B. Chì (Pb)
C. Bạc (Ag)
D. Vàng (Au)
Đáp án: D
Câu 18: Để làm sạch mẫu chì bị lẫn kẽm, ngươì ta ngâm mẫu chì này vào một lượng dư dung dịch:
A. ZnSO4
B. Pb(NO3)2
C. CuCl2
D. Na2CO3
Đáp án: B
Giải thích:
Zn + Pb(NO3)2 → Zn(NO3)2 + Pb.
Câu 19: Dung dịch FeCl2 có lẫn tạp chất là CuCl2 có thể dùng kim loại nào sau đây để làm sạch dung dịch FeCl2 trên:
A. Zn
B. Fe
C. Mg
D. Ag
Đáp án: B
Giải thích:
Fe + CuCl2 → FeCl2 + Cu
Câu 20: Kim loại vừa tác dụng với dd HCl vừa tác dụng được với dung dịch KOH:
A. Fe, Al
B. Ag, Zn
C. Al, Cu
D. Al, Zn
Đáp án: D
Câu 21: Các kim loại tác dụng được với nước ở nhiệt độ thường tạo thành dung dịch kiềm và giải phóng khí hiđro:
A. K, Ca
B. Zn, Ag
C. Mg, Ag
D. Cu, Ba
Đáp án: A
Câu 22: Khi thả một cây đinh sắt sạch vào dung dịch CuSO4 loãng, có hiện tượng sau:
A. Sủi bọt khí, màu xanh của dung dịch nhạt dần.
B. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch đậm dần.
C. Có một lớp đồng màu đỏ phủ lên đinh sắt, dung dịch không đổi màu.
D. Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần
Đáp án: D
Giải thích:
Fe + CuSO4 → FeSO4 + Cu
Hiện tượng: Có một lớp đồng màu đỏ phủ lên đinh sắt, màu xanh của dung dịch nhạt dần
Câu 23: Hoà tan hết 2,3g Na kim loại vào 97,8g nước thu được dung dịch có nồng độ:
A. 2,4%.
B. 4,0%.
C. 23,0%.
D. 5,8%.
Đáp án: B
Giải thích:
Câu 24: Cho 4,6 g một kim loại M (hoá trị I) phản ứng với khí clo tạo thành 11,7g muối. M là kim loại nào sau đây:
A. Li
B. K
C. Na
D. Ag
Đáp án: C
Giải thích:
2M + Cl2 → 2MCl
Bảo toàn khối lượng có :
mclo = 11,7 – 4,6 = 7,1 gam → nclo = 7,1 :71 = 0,1 mol
Theo PTHH có nM = 2.nclo = 0,2 mol → MM = 4,6 : 0,2 = 23 (g/mol).
Vậy kim loại cần tìm là Na.
Câu 25: Nhúng một lá sắt vào dung dịch đồng sunfat sau một thời gian lấy lá sắt ra khỏi dung dịch cân lại thấy nặng hơn ban đầu 0,2g. Khối lượng đồng bám vào lá sắt là:
A. 0,2g
B. 1,6g
C. 3,2g
D. 6,4g
Đáp án: B
Giải thích:
Khối lượng lá sắt tăng = mCu sinh ra – mFe phản ứng → 64x – 56x = 0,2 → x = 0,025 mol
mCu sinh ra = 64.0,025 = 1,6 gam.
Các câu hỏi trắc nghiệm Hóa học lớp 9 có đáp án, chọn lọc khác:
Trắc nghiệm Ôn tập học kì 1 có đáp án
Xem thêm các chương trình khác:
- Trắc nghiệm Sinh học lớp 7 có đáp án
- Trắc nghiệm Toán lớp 7 có đáp án
- Trắc nghiệm Ngữ văn lớp 7 có đáp án
- Trắc nghiệm Sinh học 8 có đáp án
- Trắc nghiệm Toán lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Ngữ văn 8 có đáp án
- Trắc nghiệm Hóa học lớp 8 có đáp án
- Trắc nghiệm Địa Lí lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Tiếng Anh lớp 8 có đáp án
- Trắc nghiệm GDCD lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Lịch sử lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Vật Lí lớp 8 có đáp án
- Trắc nghiệm Công nghệ lớp 8 có đáp án
- Trắc nghiệm Tin học lớp 8 có đáp án
- Trắc nghiệm Sinh học lớp 10 có đáp án
- Trắc nghiệm Toán lớp 10 có đáp án
- Trắc nghiệm Hóa học lớp 10 có đáp án
- Trắc nghiệm Ngữ văn lớp 10 có đáp án
- Trắc nghiệm Vật Lí lớp 10 có đáp án
- Trắc nghiệm Tiếng Anh lớp 10 có đáp án
- Trắc nghiệm Sinh học lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Toán lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Hóa học lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Ngữ văn lớp 11 có đáp án
- Trắc nghiệm Tiếng Anh lớp 11 có đáp án
- Trắc nghiệm Vật Lí lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Địa lí lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm GDCD lớp 11 có đáp án
- Trắc nghiệm Lịch sử lớp 11 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Công nghệ lớp 11 có đáp án
- Trắc nghiệm Giáo dục quốc phòng - an ninh lớp 11 có đáp án
- Trắc nghiệm Tin học lớp 11 có đáp án
- Trắc nghiệm Toán lớp 12 có đáp án
- Trắc nghiệm Sinh học lớp 12 có đáp án
- Trắc nghiệm Hóa học lớp 12 có đáp án
- Trắc nghiệm Ngữ văn lớp 12 có đáp án
- Trắc nghiệm Tiếng Anh lớp 12 có đáp án
- Trắc nghiệm Địa lí lớp 12 có đáp án
- Trắc nghiệm Vật Lí lớp 12 có đáp án
- Trắc nghiệm Công nghệ lớp 12 có đáp án
- Trắc nghiệm Giáo dục công dân lớp 12 có đáp án
- Trắc nghiệm Lịch sử lớp 12 có đáp án
- Trắc nghiệm Giáo dục quốc phòng - an ninh lớp 12 có đáp án