1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 15)
Bộ 1000 câu hỏi ôn tập môn Hóa có đáp án Phần 15 hay nhất được biên soạn và chọn lọc giúp bạn ôn luyện và đạt kết quả cao trong bài thi môn Hóa.
1000 câu hỏi ôn tập Hóa (Phần 15)
a) Viết phương trình hóa học xảy ra.
b) Tính % khối lượng của các muối trong hỗn hợp G.
Lời giải: nAgNO3=0,5.1,4=0,7(mol)
Cho Mg dư vào dung dịch Z có khối lượng tăng so với kim loại Mg ban đầu ⇒ AgNO3 dư
Gọi số mol {nMgCl2=a(mol)nNaCl=b(mol)nNaBr=c(mol)
MgCl2 + 2AgNO3 → 2AgCl↓ + Mg(NO3)2
NaCl + AgNO3 → AgCl↓ + NaNO3
NaBr + AgNO3 → AgBr↓ + NaNO3
Ta có: nMgCl2+nNaCl+nNaBr=39,85
→ 95a + 58,5b + 103c = 39,58 (1)
Và mAgCl + mAgBr = 93,22
→ 143,5(2a + b) + 188c = 93,22 (2)
Mg + 2AgNO3 → Mg(NO3)2 + 2Ag
nMg phản ứng = x (mol) → nAg = 2x (mol)
→mtăng = mAg – mMg
→ 9,6 = 108.2x – 24x
→ x = 0,05
nAgNO3du=0,05.2=0,1(mol)
phản ứng với G = 0,7 – 0,1 = 0,6 (mol)
Theo phương trình phản ứng với G → 2a + b + c = 0,6 = (3)
Giải hệ (1), (2), (3){a=0,12b=0,2c=0,16
%mMgCl2=0,12.9539,58.100=28,8%%mNaCl=0,2.58,539,58.100=29,56%%mNaBr=100−28,8−29,56=41,64%
Lời giải:
Gọi R là kí hiệu trung bình của 2 kim loại
2R + 2H2O → 2ROH + H2
ROH + HCl → RCl + H2O
- Theo các PTHH ta có: nR = nROH = nHCl = 0,2 mol
MR=30,2=15(g/mol)
-Ta có: MLi =7 < MR = 15 < MNa = 23
Vậy A là liti (Li).
- Phần 1: Cho tác dụng hoàn toàn với 90 ml dung dịch HCl 1M, sau phản ứng dung dịch làm quỳ tím hoá xanh.
- Phần 2: Cho tác dụng với V(ml) dung dịch HCl 1M sau phản ứng dung dịch không làm đổi màu quỳ tím
a. Tìm công thức phân tử oxit
b. Tính V
Lời giải:
a. Gọi công thức oxit kim loại hóa trị I: M2O
nHCl = 1.0,09 = 0,09mol
Phương trình phản ứng: M2O + 2HCl → 2MCl + H2O (1)
1,5/(2M + 16) 3/(2M + 16)
(1) suy ra: 3/(2M + 16) > 0,09 → M < 8,67
Suy ra: M là Li
b. (1/2 hỗn hợp) = 1,5/30 = 0,05 mol
Phương trình phản ứng: Li2O + 2HCl → 2LiCl + H2O (2)
0,05 0,1
(2) suy ra: V = 0,1/1 = 0,1 lít = 100 ml.
A. 30 và 70;
B. 35 và 65;
C. 75 và 25;
D. 90 và 10.
Lời giải:
Đáp án đúng là: C
PTHH: C2H4 + Br2 → C2H4Br2
Khi cho hỗn hợp khí trên qua dung dich brom thì C2H4 bị giữ lại trong bình
=> mbình tăng = mC2H4= 1,4(g)
VC2H4=0,05.22,4=1,12(l)VC2H4=0,05.22,4=1,12(l)VCH4=4,48−1,12=3,36(l)%VCH4=3,364,48.100%=75%⇒%VC2H4=100%−75%=25%
A. CH3OH;
B. C2H5OH;
C. C3H7OH;
D. C4H9OH.
Lời giải:
Đáp án đúng là: B
Giả sử ancol đơn chức, no, mạch hở là ROH
Theo tăng giảm khối lượng:
nROH=6,8−4,622=0,1(mol)→MROH=4,60,1=46(g/mol)
Vậy ancol đơn chức, no, mạch hở là: C2H5OH.
Lời giải:
nMg=4,824=0,2(mol)nNO=2,2422,4=0,1(mol)
Dung dịch X có muối NH4NO3
Xét sự thay đổi e ta có:
0Mg→+3Mg+3e+5N+8e→−3N+5N+3e→+2N
Bảo toàn e ta có:
2nMg=3nNO+8nNH4NO3⇒nNH4NO3=2.0,2−0,1.38=0,0125(mol)
Dung dịch X gồm 2 muối NH4NO3: 0,0125 mol; Mg(NO3)2: 0,2 mol
mX = 0,0125.80 + 0,2.148 = 30,6 (g).
A. 1,940;
B. 1,120;
C. 2,240;
D. 0,448.
Lời giải:
Đáp án đúng là: D
nMg=4,824=0,2(mol)→ Số mol của Mg(NO3)2: 0,2 mol
→mMg(NO3)2=0,2.148=29,6(g)→mNH4NO3=32−29,6=2,4(g)→nNH4NO3=2,480=0,03(mol)
Xét sự thay đổi e ta có:
0Mg→+3Mg+3e+5N+8e→−3N2+5N+8e→2+1N
Bảo toàn e ta có:
2nMg=8nN2O+8nNH4NO3⇒nN2O=2.0,2−0,03.88=0,02(mol)⇒VN2O=0,02.22,4=0,448(l)
Câu 8: Cho 400 ml dung dịch KOH 0,1M vào 100 ml dung dịch H2SO4 0,1M thu được dung dịch Y.
a. Tính nồng độ mol của các ion trong Y?
b. Tính pH của dung dịch Y, xác định môi trường của dung dịch Y?
c. Tính thể tích dung dịch HCl 10% cần để trung hoà dung dịch Y biết D = 1,25 g/ml?
Lời giải:
a. nKOH = 0,4.0,1 = 0,04 (mol)
nH2SO4=0,1.0,1=0,01(mol)2KOH + H2SO4→ K2SO4+ H2O0,04...........0,010,02...........0,01..........0,010,02............0...............0,01
Vdd = 0,4 + 0,1 = 0,5 (l)
→CMKOHdu=0,020,5=0,04M→CMK2SO4=0,010,5=0,02M
b.
pH=14+log[OH−]
Vậy môi trường của dung dịch Y là bazơ.
c. Phương trình: HCl + KOH → KCl + H2O
→nHCl = nKOH dư = 0,02 (mol)
→mHCl = 0,02.36,5 = 0,73 (g)
A. 10;
B. 12;
C. 3;
D. 2.
Lời giải:
Đáp án đúng là: B
nHCl = 0,04.0,75 = 0,03 mol; ;
nKOH = 0,16.0,04 = 0,0064 (mol)
Lập tỉ lệ: dư
Lời giải
Ta có: mNaOH = 44.10% = 4,4 (g)
Ta có:
Vậy phản ứng tạo 2 muối: Na3PO4; Na2HPO4
3NaOH + H3PO4 → Na3PO4 + 3H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
Bảo toàn khối lượng:
+ mmuối
→mmuối = 4,4 + 3,92 – 0,11.18 = 6,34 (g).
Lời giải:
Ta quy đổi: C4H10 = 3H2 + 2C2H2
Ta có: x + y + z = 0,225 (1)
Bảo toàn nguyên tố C: 3x + 2y = 0,6 (2)
→ x+ 2y – z = 0,2 (3)
Từ (1) (2) (3) ta được:
Nếu cho 7,56 lít (đktc) hỗn hợp A đi qua bình đựng dung dịch Br2
Tỉ lệ: nên trong 7,56 lít (đktc) hỗn hợp A có C3H6: 0,285 mol; C2H2: 0,0225 mol; H2: 0,03 mol
Với , C2H2: b mol; H2: c mol ta có hệ phương trình:
A. 5,1 gam;
B. 10,2 gam;
C. 1,2 gam;
D. 20,4 gam.
Lời giải:
Đáp án đúng là: B
nAl = 5,4/27 = 0,2 mol.
Phương trình hoá học:
4Al + 3O2 → 2Al2O3.
Theo phương trình hoá học có:
Bảo toàn khối lượng:
Lời giải:
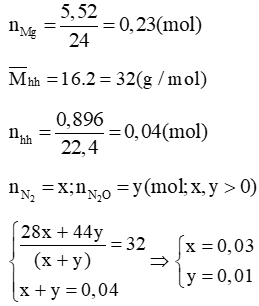
Dung dịch thu được có thể chứa NH4NO3: a (mol)
Quá trình nhường e
Quá trình nhận e

ne nhận =
Bảo toàn e ta có:
0,46 = 0,38 = 8a
→ a = 0,01 (mol)
→ = 0,01 (mol)
Vậy dung dịch thu được gồm: Mg(NO3)2: 0,23 (mol) và NH4NO3: 0,01 (mol)
Cô cạn thu được mrắn = = 0,23.148 + 0,01.80 = 34,84 (g)
Câu 14: Cho 5,6 gam Fe tác dụng với lượng dư dung dịch AgNO3 thu được m gam chất rắn. Giá trị m là:
A. 21,6;
B. 10,8;
C. 27,0;
D. 32,4.
Lời giải:
Đáp án đúng là: A
Vì Fe tác dụng với lượng dư dung dịch AgNO3 nên chỉ xảy ra phản ứng sau:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Theo phương trình: nAg = 2nFe = 2.0,1 = 0,2 (mol)
→mAg = 0,2.108 = 21,6 (g).
Lời giải:
Đáp án đúng là: D
Gọi kim loại cần tìm là A, oxit của kim loại A, hoá trị II là AO
Phương trình: AO + 2HCl → ACl2 + H2O
Ta có:
Theo phương trình:
Vậy A là canxi (Ca).
Lời giải
Do M thuộc nhóm IA nên M có hóa trị I
PTHH: 2M + 2HCl → 2MCl + H2
Vậy M là Na (Sodium).
Lời giải
Phương trình: SO2 + Br2 + 2H2O → 2HBr + H2SO4
Theo phương trình:
Khi cho Cu và Al tác dụng với H2SO4 đặc nguội thì chỉ có Cu phản ứng:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Theo phương trình trên:
→mCu = 0,05.64 = 3,2 (g)
→mAl = 5,9 – 3,2 = 2,7 (g)
Tổng số mol của hỗn hợp 2 kim loại trên là 0,05 + 0,1 = 0,15 (mol).
Câu 18: Cho 5,6 gam Fe tác dụng với 500 ml dung dịch HNO3 0,8M. Sau phản ứng thu được V lít hỗn hợp khí A gồm N2O và NO2 có tỉ khối so với H2 là 22,25 và dung dịch B.
a. Tính V (đktc)
b. Tính CM các chất trong dung dịch B.
Lời giải:
a. Đặt x, y lần lượt là số mol của N2O và NO2.
PTHH xảy ra:
8Fe + 30HNO3 → 8Fe(NO3)3 + 3N2O + 15H2O (1)
Fe + 6HNO3 → Fe(NO3)3 + 3NO2 + 3H2O (2)
Theo PTHH (1), (2),
Tỉ lệ thể tích các khí trên là:
Gọi a là thành phần % theo thể tích của khí N2O
Vậy (1 – a) là thành phần % của khí NO2
Ta có: 44a + 46(1 – a) = 22,25.2 = 44,5
→ a = 0,75 hay % của khí N2O là 75% và của khí NO2 là 25%
Tỉ lệ về thể tích cũng là tỉ lệ về số mol nên x = 3y (**)
Giải (*), (**) ta được x = 0,036, y = 0,012
Vậy thể tích của các khí thu được là:
V = ( 0,012 + 0,036).22,4 = 1,08 (l)
b.
Vậy nồng độ các chất trong dung dịch là:
A. Mg;
B. Ca;
C. Fe;
D. Ba.
Lời giải:
Đáp án đúng là:
Gọi hoá trị của kim loại M là n ( )
PTHH: 2M + 2nHCl → 2MCln + nH2
Theo phương trình:
Với n = 2 thì MM = 24 (g/mol)
Vậy M là magie (Mg).
Lời giải:
Sau phản ứng, hỗn hợp khí gồm O2 (dư) và N2
Gọi
Ta có :
nkhí = a + b = = 0,3 (mol)
mkhí = 32a + 28b = 0,3.15.2 = 9(gam)
⇒ a = 0,15; b = 0,15
Gọi
Ta có :
mkhí =
⇒ 32a + 0,15.28 = (a + 0,15).15,6.2
⇒ a = 0,6
⇒ = a − 0,15 = 0,6 − 0,15 = 0,45(mol)
Gọi hóa trị của Y là n
4Y + nO2 2Y2On
Theo phương trình, ta có :
Với n =1thì MY = 32,5 (loại)
Với n = 2 thì MY = 65 (Zn)
Với n = 3 thì MY = 97,5 (loại)
Vậy Y là kim loại Zn (kẽm).
a. Xác định 2 kim loại kiềm
b. Tính khối lượng 2 hiđroxit thu được
c. Tính V dung dịch H2SO4 1M cần trung hòa hết 2 hiđroxit này.
Lời giải:
a) 2M + 2H2O → 2MOH + H2
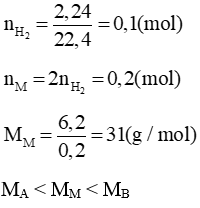
→ A: Natri (Na), B: Kali (K)
b) Hỗn hợp: Na (a mol), K (b mol)
nNaOH = nNa = 0,1 (mol)
mNaOH = 0,1.40 = 4 (g)
nKOH = nK = 0,1 (mol)
mKOH = 0,1.56 = 5,6 (g)
c. 2NaOH + H2SO4 → Na2SO4 + 2H2O
2KOH + H2SO4 → K2SO4 + 2H2O
A. 42%;
B. 28%;
C. 50%;
D. 56%.
Lời giải:
Đáp án đúng là: B
Bảo toàn nguyên tố C, ta có:
A. 1,344;
B. 0,896;
C. 15,933;
D. 0,672.
Lời giải:
Đáp án đúng là: A
nCu = 0,1 mol; = 0,24 mol; = 0,12 mol.
⇒ H+ hết ⇒ nNO = 0,06 mol ⇒ V = 1,344 lít.
a/. Tính khối lượng CuO trong hỗn hợp ban đầu ?
A. 2,4;
B. 4,0;
C. 6,0;
D. Kết quả khác.
b/ Tính nồng độ mol các chất trong dd sau phản ứng ? Biết thể tích dung dịch không thay đổi.
A. 4M; 1,8M;
B. 1,5M; 1M;
C. 2M; 4M;
D. 0,31M; 0,18M.
Lời giải:
a/ Đáp án đúng là: A
a/ nNO = 0,6 (mol)
→ ne nhận = 3nNO = 1,8 (mol)
→ nCu = ne nhận : 2 = 0,9 (mol)
→ mCu = 0,9.64 = 57,6 (g) → mCuO = 60 – 57,6 = 2,4 (g).
b/ Đáp án đúng là: D
b/ nCuO = 0,03 (mol)
= ne nhận + nNO + 2nCuO = 1,8 + 0,6 + 2.0,03 = 2,46 (mol)
→ dư = 3 – 2,46 = 0,54 (mol)
Lời giải:
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
Fe + 2HCl → FeCl2 + H2↑
ZnS + 2HCl → ZnCl2 + H2S↑
Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O
CaSO3 + 2HCl → CaCl2 + SO2↑ + H2O
9Fe(NO3)2 + 12HCl → 5Fe(NO3)3 + 4FeCl3 + 3NO↑+ 6H2O
CaC2 + 2HCl → CaCl2 + CH≡CH↑
Al4C3 + 12HCl → 4AlCl3 + 3CH4↑
Na2O2 + 2HCl → 2NaCl + H2O + ½ O2↑
A. 11,36 gam;
B. 5,5 gam;
C. 10,65 gam;
D. 9,94 gam.
Lời giải:
Đáp án đúng là: C
Hỗn hợp rắn X gồm P2O5 (x mol) và P2O3 (y mol);
= 0,075.142 = 10,65 gam.
Câu 27: Cho 7,8 gam hỗn hợp hai kim loại Al và Mg vào dung dịch HCl dư thu được 8,96 lít khí H2
a) Viết các phương trình phản ứng xảy ra
b) Tính thành phần % khối lượng mỗi kim loại trong hỗn hợp ban đầu
c) Tính khối lượng muối thu được sau phản ứng.
Lời giải:
1,
2, Đặt a = nAl, b = nMg
Ta có:
→ nAl = 0,2 mol → mAl = 5,4 (g)
→ %Al = 69,23%, %Mg= 30, 76%
3, mmuối = = 0,2.133,5 + 0,1. 95 = 36,2 (g).
A. 0,8 mol;
B. 0,4 mol;
C. 0,3 mol;
D. 0,25 mol.
Lời giải:
Đáp án đúng là: A
Nhận xét: Kim loại + HCl → muối + H2
Ta có: mdung dịch tắng = mkim loại – mkhí thoát ra
= 7,8 – 7 = 0,8 (gam)
Áp dụng bảo toàn nguyên tố H:
Lời giải:
2A + Cl2 → 2ACl ( vì A hóa trị I → ACl)
2 1 2 ( mol)
Ta có: nA = nACl
→ MA = 39 (g/mol)
Vậy A là kali (K).
a) Tính khối lượng thể tích dung dịch HCl cần dùng để hòa tan hỗn hợp.
b) Tính C% của dung dịch thu được sau phản ứng.
Lời giải:
Khí thu được sau phản ứng là: CO2
1. MgCO3 + 2HCl → MgCl2 + H2O + CO2
0,2 ← 0,4 ← 0,2 0,2 (mol)
→ mMgO = mhh - = 24,8 - 16,8 = 8 (g)
2. MgO + 2HCl→ MgCl2 + H2O
0,2 → 0,4 → 0,2 (mol)
nHCl = 0,4 + 0,4 = 0,8 ( mol)
mHCl = n.M = 0,8. 36,5 = 29,2 (g)
a)
VddHCl = n.22,4 = 0,8.22,4 = 17,92 (l)
b) = n.M = (0,2 + 0,2).95 = 38(g)
mdd sau phản ưng = mhh đầu + mddHCl - = 24,8+ 146 - 0,2. 44 = 162(g)
a/ Tính khối lượng mỗi chất trong hỗn hợp đầu.
b/ Tính thể tích dung dịch H2SO4 cần dùng.
Lời giải:
a. = 0,2 mol
1. MgO + H2SO4 → MgSO4 + H2O
2. MgCO3 + H2SO4 → MgSO4 + H2O + CO2
Ta có: = = 0,2 mol → = 16,8 g
→ mMgO = 4 g.
b. nMgO = 0,1 mol → = 0,3 mol
→ V = 6,72 lít.
a) Tính số mol mỗi khí trong hỗn hợp khí thu được.
b) Tính tỉ khối hỗn hợp khí so với hiđro?
c) Nồng độ của dd HNO3 đã dùng là bao nhiêu?
Lời giải:
Ta có:
Gọi số mol NO; NO2 lần lượt là x; y (mol)
→x + y =
Bảo toàn e:
→ 3x + y = 0,13.2 = 0,26
Giải được: x = 0,02; y = 0,2
Vậy:
NO: 0,02 mol; NO2: 0,2 mol
b. Ta có:
mhh = 0,02.30 + 0,2.46 = 9,8 gam.
c.
Bảo toàn N:
= 0,13.2 + 0,02 + 0,2 = 0,48 mol.
Câu 33: Cho 8,4 gam hỗn hợp Zn và Mg tác dụng với 500ml dung dịch HCl 2M.
a) Chứng minh rằng sau phản ứng axit vẫn còn dư.
b) Nếu thoát ra 4,48 lít khí ở đktc. Hãy tính số gam Mg và Zn đã dùng ban đầu.
c) Tính thể tích đồng thời của 2 dung dịch KOH 2M và Ba(OH)2 1M cần dùng để trung hòa lượng axit dư.
Lời giải:
a, Ta có 500 ml = 0,5 lít
→ nHCl = 0,5.2 = 1 (mol)
Mg + 2HCl → MgCl2 + H2
x…... 2x…….. x……….x (mol)
Zn + 2HCl → ZnCl2 + H2
y….. 2y…….. y………y (mol)
→ 2x + 2y = 1 → 2( x + y ) = 1→ x + y = 0,5
Ta có 24x + 24y < 24x + 65y < 65x + 65y
Þ nhỗn hợp max =
Mà nHCl = 1 (mol)
→ 1 > 0,7 → nHCl > nhỗn hợp max
→ Sau phản ứng axit vẫn còn dư.
b. Ta có
Mg + 2HCl → MgCl2 + H2 (1)
x…... 2x…….. x……….x (mol)
Zn + 2HCl → ZnCl2 + H2 (2)
y….. 2y…….. y………y (mol)
Theo định luật bảo toàn khối lượng
→ mhỗn hợp = mmuối + - mHCl
= - mHCl
= 95.+ 136. + 0,2.2 - 0,4.36,5 = 9,4 (g).
b/ Tính thể tích khí, khối lượng thu được sau phản ứng.
Lời giải:
a)
Al + 6HNO3 → Al(NO3)3 + 3NO2 + 3H2O
0,3….1,8………0,3………..0,9 (mol)
b)
mmuối =
Lời giải:
Gọi nguyên tử khối của kim loại A là A.
Phương trình hóa học của phản ứng:
2A + Cl2 → 2ACl
mA = 9,2g; mACl = 23,4g.
Có nA = nACl
⇒ 9,2. (MA + 35,5) = MA. 23,4.
⇒ MA = 23. Vậy kim loại A là Na.
Câu 36: Cho 9,6 gam Mg vào dung dịch chứa 0,2 mol Cu(NO3)2 và 0,3 mol Fe(NO3)3. Phản ứng kết thúc khối lượng chất rắn thu được là nhiêu?
Lời giải:
Quy tắc :
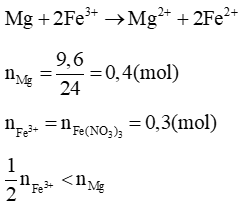
→Mg dư
nMg dư = 0,4 – 0,15 = 0,25 (mol)
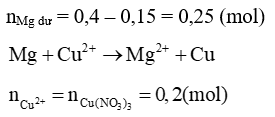
→Mg dư
BT e:
nMg dư = 0,25 – 0,2 = 0,05 (mol)
→ dư
BT e:
nFe = nMg = 0,05 (mol)
Bảo toàn Fe:
mrắn = 0,05.56 + 0,2.64 = 15,6 (g).
Lời giải:
Gọi Kim loại nhóm IIA cần tìm là R có hóa trị II.
Khi cho dung dịch sau phản ứng tác dụng với NaOH, có khí thoát ra ⇒ sản phẩm có NH4NO3.
PTHH:
NH4NO3 + NaOH → NH3 + H2O + NaNO3
Có
Áp dụng định luật bảo toàn e, ta có
(NH4NO3)
Vậy n e nhận = 8 = 0,1.8 = 0,8 mol
Có mR = 0,4.MR = 9,6
( Magie)
Vậy kim loại cần tìm là Mg.
Câu 38: Hòa tan 9,4 gam kali oxit vòa nước thu được 200ml dung dịch A.
a. Tính nồng độ mol dung dịch A thu được.
Lời giải:
a)
VddA = 200 ml = 0,2 lít
PTHH: K2O + H2O → 2KOH (1)
nKOH = 0,1.2 = 0,2 (mol)
→CM ddA = CM KOH =
b) PTHH: 2KOH + H2SO4 → K2SO4 + 2H2O
→
a. Viết các phương trình hoá học?
b. Tính a?
Lời giải:
a, 2A + 2xHCl → 2AClx + xH2
2B + 2yHCl → 2BCly + yH2
b,
Theo PTHH,
mHCl = 0,8.36,5 = 29,2 (g)
Bảo toàn khối lượng: a = 67 + 0,8 − 29,2 = 38,6 (g).
Lời giải:
MY = 20,143.2 = 40,286
→ mY = 40,286.0,14 = 5,64 (g)
Gọi số mol NO2, NO lần lượt là a và b (mol)
Ta có hệ phương trình:
Gọi số mol FeO, CuO, Fe2O3 là x (mol)
Theo bảo toàn e ta có:
→ x = 0,09 + 3.0,05 = 0,24 (mol)
→
→ m = 0,24.72 + 0,24.80 + 0,24.160 = 74,88 (g).
Lời giải:
Gọi hoá trị của kim loại M là n ()
PTHH: 2M + 2nHCl → 2MCln + nH2 (1)
Theo PTHH (1): nHCl phản ứng = 2
Mà theo đề bài nHCl < 2nên kim loại M có xảy ra phản ứng với nước:
2M + 2nH2O → 2M(OH)n + nH2 (2)
Theo PTHH (1)
Theo PTHH (1):
Theo PTHH (2):
Dung dịch X chứa 16,21 gam chất tan nên ta có:
→ MM = 39n
Với n = 1 thì MM = 39 (g/mol)
Vậy M là kali (K).
2) Hòa tan 2,668 gam hỗn hợp B gồm Fe3O4 và FeCO3 cần vừa đủ 100 ml dung dịch A. Xác định khối lượng từng chất trong hỗn hợp B?
Lời giải:
1) ; nKOH = 0,2.2 = 0,4 (mol)
Trường hợp 1: H2SO4 dư
H2SO4 + 2KOH → K2SO4 + 2H2O
0,2……..0,4
dư = 0,5a – 0,2 (mol) →= 0,25a – 0,1 (mol)
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
0,005………0,075
→ 0,25a – 0,1 = 0,075 → a = 0,43
Trường hợp: KOH dư
H2SO4 + 2KOH → K2SO4 + 2H2O
0,5a……..a
nKOH dư = 0,4 – a (mol) → = 0,2 – 0,5a (mol)
Al(OH)3 + KOH → KAlO2 + 2H2O
0,005…….0,005
→ 0,2 – 0,5a = 0,005 →a = 0,39
b) Vì A tác dụng với Fe3O4 và FeCO3 →dung dịch A chứa H2SO4 dư, chọn trường hợp 1: a = 0,43
trong 100 ml dung dịch A = 0,1.0,43 = 0,043 (mol)
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
x……….4x
FeCO3 + H2SO4 → FeSO4 + H2O + CO2
y………..y
mhhB = 2,668 (g) → 233x + 116y = 2,668 (1)
= 0,043 (mol) → 4x + y = 0,043 (2)
Giải (1) và (2), ta được: x = 0,01; y = 0,003
a) Hãy xác định bộ 4 số lượng tử của e cuối cùng của A, B
b) Viết cấu hình e của nguyên tử nguyên tố A, B.
Lời giải:
a) Do A và B là hai nguyên tử kế tiếp, lại có nA > nB (theo đề) nên nA - nB = 1, nghĩa là A nằm đầu chu kỳ mới và B nằm cuối chu kỳ cũ.
A và B có tổng số n + l bằng nhau lên lB - lA = 1.
Vì A nằm đầu chu kỳ mới nên lA = 0 (phân lớp s), ml(A) = 0, ms(A) = +1/2.
Þ lB = 1.
Theo đề B có nB + lB + ml(B) + ms(B) = 4,5.
Do electron (e) cuối cùng có ms = -1/2, giá trị ml = l;
Vậy B có nB + 2lB -1/2 = 4,5 hay nB = 3; ⇒ nA = 4.
Vậy bộ số lượng tử của A (4, 0, 0, +1/2) và B (3, 1, +1, -1/2).
b) Cấu hình electron của A: 1s22s22p63s23p64s1.
Cấu hình electron của B: 1s22s22p63s23p6
Câu 44: Cho các phát biểu sau:
(a) Cho Ba vào dung dịch H2SO4 loãng, thu được chất kết tủa và có khí thoát ra.
(b) Kim loại dẻo nhất là Au, kim loại có nhiệt độ nóng chảy thấp nhất là Hg.
(c) Để khử chua cho đất và tăng năng suất cây trồng cần trộn vôi với đạm ure để bón.
(d) Đốt sợi dây thép trong khí Cl2 xảy ra ăn mòn điện hoá học.
Số phát biểu đúng là
A. 1. B. 4. C. 2. D. 3.
Lời giải:
Đáp án đúng là: C
Phát biểu (a) và (b) đúng.
A.8.88 gam;
B.13.92 gam;
C.6.52 gam;
D.13.32 gam.
Lời giải:
Đáp án đúng là: B
nMg = 0,09 mol
nNO = 0,04 mol
Nhận thấy: 2nMg > 3nNO → sản phẩm khử chứa NH4NO3
Bảo toàn electron: 2nMg = 3nNO + 8
Muối khan gồm:
Mg(NO3)2: 0,09 mol; NH4NO3: 7,5.10-3 mol
mmuối = 0,09.148 + 7,5.10-3.80 = 13,92 gam.
Lời giải:
1 mol H2 chứa 6,02 × 1023 phân tử H2.
436 kJ = 436 × 103 J.
Năng lượng cần thiết để phá vỡ liên kết trong một phân tử H2 là:
Năng lượng cần thiết (theo eV) để phá vỡ liên kết trong một phân tử H2 là:
Lời giải:
Ta có: 2Z + N = 58
Kết hợp:
Nếu Z = 18 → N = 22 → A = 40 (Loại)
Nếu Z = 19 → N = 20 → A = 39 (Nhận)
→Nguyên tử A có 19p, 19e, 20n.
Câu 48: Cho biết nguyên tử khối trung bình của Iriđi là 192,22. Iriđi trong tự nhiên có hai đồng vị là 191Ir và 193Ir. Phần trăm số nguyên tử của 193Ir là
D. 61,0%.
Lời giải:
Đáp án đúng là: D
Gọi thành phần phần trăm của 191Ir và 193Ir lần lượt x, y
Ta có hệ :
Phần trăm số nguyên tử của 193Ir là 61%.
Câu 49: Cho sơ đồ phản ứng sau:
b. Cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong phản ứng.
c. Cho biết tỉ lệ số nguyên tử, số phân tử của hai cặp chất trong phản ứng.
Lời giải:
a. 4K + O2 → 2K2O
b. Tỉ lệ số nguyên tử K : Số phân tử O2 : Số phân tử K2O là 4 : 1 : 2.
c. Tỉ lệ số nguyên tử K: Số phân tử O2 là 4 : 1
Tỉ lệ số phân tử O2: Số phân tử K2O là 1 : 2.
C. 22,2;
D. 22,75.
Lời giải:
Đáp án đúng là: B
C+ 4HNO3 đặc nóng→ CO2 + 4NO2 + 2H2O
Đặt số mol CO2 là x mol → nNO2= 4x mol
→mhh = = 44x+ 46.4x = 228x (g)
Và nhh= = x + 4x = 5x (mol)
Xem thêm các câu hỏi ôn tập Hóa học chọn lọc, hay khác:
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 10)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 11)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 12)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 13)
1000 câu hỏi ôn tập môn Hóa có đáp án (Phần 14)
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
