Công thức tính độ bất bão hòa hợp chất hữu cơ và cách giải các dạng bài tập (2025) chi tiết nhất
Với công thức tính độ bất bão hòa hợp chất hữu cơ Hóa học lớp 11 chi tiết nhất giúp học sinh dễ dàng nhớ toàn bộ các công thức tính độ bất bão hòa hợp chất hữu cơ từ đó biết cách làm bài tập Hóa học 11. Mời các bạn đón xem:
Công thức tính độ bất bão hòa hợp chất hữu cơ hay nhất – Hóa học lớp 11
Hợp chất hữu cơ là hợp chất của cacbon (trừ CO, CO2, muối cacbonat, xianua, cacbua,…). Việc biết chất đó có bao liên kết pi và vòng sẽ giúp chúng ta giải bài toán hữu cơ một cách nhanh chóng. Để biết chất có tổng bao nhiêu liên kết pi và vòng, người ta sẽ tính độ bất bão hòa của chất đó. Các em hãy tham khảo bài viết dưới đây để biết cách xác định độ bất bão hòa của chất hữu cơ.
I. KHÁI QUÁT VỀ ĐỘ BẤT BÃO HÒA
1. Định nghĩa
Độ bất bão hòa (k) là đại lượng đặc trưng cho mức độ chưa no của một hợp chất hữu cơ, được tính bằng tổng số liên kết π và số vòng trong CTCT.
2. Công thức tính độ bất bão hòa hợp chất hữu cơ
Xét hợp chất có công thức: CxHyOzNtXr ( X là halogen)
Độ bất bão hòa =
3. Bạn nên biết
- Công thức tính độ bất bão hòa chỉ áp dụng cho hợp chất cộng hóa trị.
- Các nguyên tố hóa trị II như oxi, lưu huỳnh không ảnh hưởng tới độ bất bão hòa.
- Một số dạng/công thức thường gặp:
+ CnH2n+2 (chỉ chứa nối đơn, mạch hở)
+ CnH2n (có 1 nối đôi, mạch hở hoặc vòng no)
+ CnH2n-2 (có 1 nối ba, mạch hở hoặc 2 nối đôi, mạch hở hoặc 1 nối đôi 1 vòng …)
+ CnH2n-6 (chứa vòng benzen …)
+ CxHyO (dạng R-OH; R-O -R’, R-CHO, R-CO-R’)
+ CxHyO2 (dạng R-COOH, R-COO -R’, HO-R-CHO…)
+ CxHyN (dạng R-NH2; R1-NH-R2,...)
II. ỨNG DỤNG CỦA ĐỘ BẤT BÃO HÒA
1. Xác định số đồng phân
- Để xác định được số đồng phân của một chất hữu cơ, nhất thiết phản phân tích được đặc điểm của các thành phần cấu tạo nên chất hữu cơ đó (gốc, nhóm chức), trong đó có các đặc điểm về mạch C và loại nhóm chức.
- Để xác định được các đặc điểm này, vai trò của k là rất quan trọng, thể hiện qua biểu thức:
kphân tử = kmạch + knhóm chức
VD1: số đồng phân của C4H10O (7 đồng phân = 4 rượu + 3 ete).
VD2: số đồng phân của C4H8O.
2. Xác định CTPT từ CT thực nghiệm
Xác định CTPT chất hữu cơ là yêu cầu phổ biến và cơ bản nhất của bài tập Hóa hữu cơ. Có nhiều phương pháp để xác định CTPT chất hữu cơ (trung bình, bảo toàn nguyên tố, bảo toàn khối lượng, …), tùy thuộc vào đặc điểm số liệu của bài toán đưa ra. Trong bài học này, ta xét trường hợp đề bài yêu cầu xác định CTPT từ CT thực nghiệm mà không cho KLPT của chất hữu cơ đó.
Cách làm: gồm 3 bước:
Bước 1: Từ CT thực nghiệm, viết lại CTPT theo n
VD: Công thức thực nghiệm của một acid hữu cơ (C2H3O2)n có thể viết lại là C2nH3nO2n .
Bước 2: Tính k theo n.
Bước 3: So sánh giá trị k tìm được với đặc điểm Hóa học của chất hữu cơ đã cho hoặc tính chất của k. VD1: Hiđrocacbon X tác dụng với Brom, thu được chất Y có công thức đơn giản nhất là C3H6Br. CTPT của X là:
A. C3H6
B. C6H12.
C. C6H14.
D. B hoặc C đều đúng.
VD2: Một hợp chất hữu cơ X chứa 87,805% C và 12,195% H về khối lượng. Biết 8,2 gam X khi tác dụng với AgNO3/NH3 dư tạo ra 18,9 gam kết tủa vàng nhạt. Số CTCT có thể thỏa mãn các tính chất của X là:
A. 5. B. 3. C. 2. D. 4.
3. Sử dụng số liên kết π trung bình
Áp dụng cho các bài toán Hóa hữu cơ mà các chất trong hỗn hợp: khác nhau về số liên kết π, có thể xác định được số liên kết π trung bình thông qua tỷ lệ số mol của hỗn hợp trong các phản ứng định lượng số liên kết π (phản ứng cộng H2, Br2, ...), hay gặp nhất là các bài toán hỗn hợp gồm ankan và ankin hoặc anken và ankin, ...
VD: Cho 4,48 lít hỗn hợp X (đktc) gồm hai hiđrocacbon mạch hở tác dụng vừa đủ với 700 ml dung dịch Br2 0,5M. Sau khi toàn bộ lượng khí bị hấp thụ hết thì khối lượng bình tăng thêm 5,3 gam. Công thức phân tử của hai hiđrocacbon là:
A. C2H2 và C2H4.
B. C2H2 và C3H8.
C. C3H4 và C4H8.
D. C2H2 và C4H6.
4. Phân tích hệ số trong các phản ứng đốt cháy
- Ta đã biết một chất hữu cơ bất kỳ chứa 3 nguyên tố C, H, O có CTPT là bão hòa (bằng tổng số vòng và số liên kết π trong CTCT).
Xét phản ứng cháy của hợp chất này, ta có:
Cn H2n+2-2k Ox nCO2+ (n+1-k)H2O
Với nX là số mol chất hữu cơ bị đốt cháy.
2 trường hợp riêng hay gặp trong các bài tập phổ thông là:
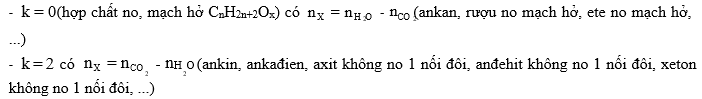
Kết quả này cũng có thể mở rộng cho cả các phản ứng cháy của hợp chất hữu cơ chứa Nitơ.
VD: Hỗn hợp X gồm rượu metylic, rượu etylic, rượu propylic và nước. Cho a gam G tác dụng với Natri dư được 0,7 mol H2. Đốt cháy hoàn toàn a gam X thu được b mol CO2 và 2,6 mol H2O. Giá trị của a và b lần lượt là:
A. 42 gam và 1,2 mol .
B. 19,6 gam và 1,9 mol.
C. 19,6 gam và 1,2 mol.
D. 28 gam và 1,9 mol.
5. Biện luận CTCT từ CTPT và ngược lại từ các đặc điểm Hóa học
III. BÀI TẬP
Câu 1: Công thức CxHyOzNt có độ bất bão hòa là
A. (2x – y + t + 2)/2
B. (2x – y + t + 2)
C. (2x – y – t + 2)/2
D. (2x – y + z + t + 2)/2
Hướng dẫn
Đáp án A
Câu 2: Vitamin A công thức phân tử C20H30O, có chứa 1 vòng 6 cạnh và không có chứa liên kết ba. Số liên kết đôi trong phân tử vitamin A là:
A. 7.
B. 6.
C. 5.
D. 4.
Hướng dẫn
Độ bất bão hòa là:
Mà
Do hợp chất không chứa liên kết ba nên số liên kết đôi trong phân tử vitamin A là 5.
Đáp án C
Câu 3: Chất nào sau đây có số liên kết π nhiều nhất (mạch hở)?
A. C3H9N.
B. C2H5N.
C. C4H8O3.
D. C3H4O4.
Hướng dẫn
Do các chất đều mạch hở ⇒ k = π + v = π.
A. π = k = (2 × 3 + 2 + 1 - 9) ÷ 2 = 0.
B. π = k = (2 × 2 + 2 + 1 - 5) ÷ 2 = 1.
C. π = k = (2 × 4 + 2 - 8) ÷ 2 = 1.
D. π = k = (2 × 3 + 2 - 4) ÷ 2 = 2.
⇒ C3H4O4 chứa nhiều liên kết π nhất
Đáp án D
Xem thêm tổng hợp công thức môn Hóa học lớp 11 đầy đủ và chi tiết khác:
Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ
Công thức phân tử hợp chất hữu cơ
Công thức xác định số nguyên tử trong hợp chất hữu cơ
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
