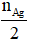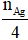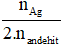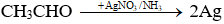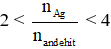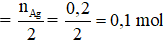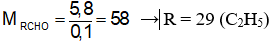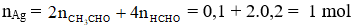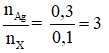Công thức phản ứng tráng gương (tráng bạc) của anđehit và cách giải các dạng bài tập (2025) chi tiết nhất
Với tài liệu về Công thức phản ứng tráng gương (tráng bạc) của anđehit bao gồm: lý thuyết và bài tập cũng như những định nghĩa, tính chất, các dạng bài sẽ giúp bạn nắm vững kiến thức và học tốt môn Hóa học hơn.
Công thức phản ứng tráng gương (tráng bạc) của anđehit
Phản ứng tráng gương (tráng bạc) là phản ứng đặc trưng của anđehit. Tuy nhiên giải dạng bài toán này bằng cách viết phương trình và tính theo phương trình sẽ làm tốn nhiều thời gian. Vậy để giải nhanh các bài tập trắc nghiệm về phản ứng tráng gương (tráng bạc) của anđehit em cần ghi nhớ những công thức gì? Phản ứng này có những trường hợp gì đặc biệt? Các em hãy cùng theo dõi bài viết dưới đây.
1. Công thức phản ứng tráng gương (tráng bạc) của anđehit
- Đối với anđehit đơn chức R-CHO (R ≠ H)
R-CHO + 2AgNO3 + 3NH3 + H2O 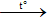
nAg = 2.n anđehit
→ n anđehit =
- Đặc biệt đối với HCHO phản ứng xảy ra như sau :
HCHO + 4AgNO3 + 6NH3 + 2H2O 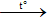
nAg = 4.nHCHO
→ nHCHO =
- Phản ứng tráng gương (tráng bạc) của của anđehit đa chức
R(CHO)x + 2xAgNO3 + 3xNH3 + xH2O 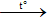
Trong đó: x là số nhóm chức -CHO của anđehit.
nAg = 2x.n anđehit
→ Số nhóm chức –CHO =
Ví dụ: Khối lượng Ag thu được khi cho 0,1 mol CH3CHO phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, đun nóng là
A. 21,6 gam. B. 43,2 gam. C. 16,2 gam. D. 10,8 gam.
Hướng dẫn giải:
Sơ đồ phản ứng:
nAg = 2.n anđehit = 2.0,1 = 0,2 mol
→ mAg = 0,2.108 = 21,6 gam.
→ Đáp án A
2. Bạn nên biết:
- Nếu 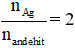
- Nếu 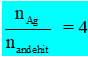
- Nếu hỗn hợp 2 anđehit mạch thẳng có
→ 1 anđehit là đơn chức và 1 anđehit là hai chức
Hoặc 1 anđehit đơn chức và 1 anđehit là HCHO
3. Mở rộng
Ngoài anđehit các hợp chất sau cũng có khả năng tham gia phản ứng tráng bạc:
+ HCOOH và muối hoặc este của nó: HCOONa, HCOONH4, HCOOCH3,...
nAg = 2nHCOO-
+ Các hợp chất tạp chức có chứa nhóm chức -CHO: Glucozơ, fructozơ,...
nAg = 2.n-CHO = 2n glucozơ (fructozơ)
4. Bài tập minh họa
Câu 1: Cho 5,8 gam một anđehit X phản ứng hoàn toàn với lượng dư AgNO3 trong dung dịch NH3 thu được 21,6 gam Ag. Công thức cấu tạo thu gọn của anđehit X là
A. HCHO. B. OHC – CHO. C. CH3CHO. D. CH3CH2CHO.
Hướng dẫn giải:
Ta có: nAg = 0,2 mol
Nếu X là HCHO
→ n HCHO 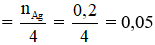
→ m HCHO = 0,05.30 = 1,5 gam ≠ 5,8 → không thỏa mãn.
Nếu X là anđehit đơn chức (R ≠ H)
→ nanđehit
Ta có:
→ X là C2H5CHO (thỏa mãn đáp án D)
Nếu X là anđehit hai chức:
Ta có: 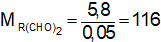
→ Đáp án D
Câu 2: Cho hỗn hợp gồm 0,1 mol CH3CHO và 0,2 mol HCHO tác dụng hết với dung dịch AgNO3/NH3 dư thì khối lượng Ag thu được là
A. 216,0 gam. B. 10,8 gam. C. 64,8 gam. D. 108,0 gam.
Hướng dẫn giải
→ mAg = 1.108 = 108 gam.
→ Đáp án D.
Câu 3: Cho 0,1 mol hỗn hợp X gồm 2 anđehit no, đơn chức, mạch hở kế tiếp nhau trong dãy đồng đẳng phản ứng hoàn toàn với lượng dư dung dịch AgNO3/NH3 thu được 32,4g Ag. Hai anđehit trong X là:
A. HCHO và C2H5CHO
B. HCHO và CH3CHO
C. CH3CHO và C2H5CHO
D. C2H3CHO và C3H5CHO
Hướng dẫn giải:
nAg = 0,3 mol
Xét
→ Hỗn hợp X phải có HCHO. Anđehit kế tiếp còn lại là CH3CHO
→ Đáp án B.
Xem thêm các dạng bài tập và công thức Hoá học lớp 11 hay, chi tiết khác:
Công thức tính nhanh số đồng phân Anđehit no, đơn chức, mạch hở
Công thức tính nhanh số đồng phân Axit cacboxylic no, đơn chức, mạch hở
Công thức tính nhanh số đồng phân Xeton no, đơn chức, mạch hở
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11