TOP 40 câu Trắc nghiệm Luyện tập: Ankin (có đáp án 2023) - Hóa 11
Bộ 40 bài tập trắc nghiệm Hóa học lớp 11 Bài 33: Luyện tập: Ankin có đáp án đầy đủ các mức độ giúp các em ôn trắc nghiệm Hóa học 11 .
Trắc nghiệm Hóa học lớp 11 Bài 33: Luyện tập: Ankin
Bài giảng Hóa học lớp 11 Bài 33: Luyện tập: Ankin
Câu 1: Có bao nhiêu ankin ứng với công thức phân tử C5H8 ?
A. 2.
B. 4.
C. 3.
D. 1.
Đáp án: C
Giải thích:
Có 3 công thức thỏa mãn :
CH≡C – CH2 – CH2 – CH3
CH3 – C≡C – CH2 – CH3
CH≡C – CH(CH3) – CH3
Câu 2: Hidrocacbon nào sau đây tác dụng với dung dịch AgNO3 trong NH3 tạo thành kết tủa
A. Stiren
B. Đimetyl axetilen
C. But-1-in
D. But-1,3-dien
Đáp án: C
Giải thích: But – 1 – in: CH≡C –CH2 – CH3 có liên kết ba đầu mạch nên có phản ứng tạo kết tủa với AgNO3/NH3
Câu 3: X là hidrocacbon mạch hở, phân nhánh, có công thức phân tử C5H8. Biết X có khả năng làm mất màu nước brom và tham gia phản ứng với AgNO3 trong dung dịch NH3. Tên của X theo IUPAC là :
A. 2-metylbut-3-in
B. 3-metylbut-1-in
C. 2-metylbuta-1,3-dien
D. pent-1-in
Đáp án: B
Giải thích:
X phản ứng với AgNO3/NH3 → có nối 3 đầu mạch
→ X là CH≡C-CH(CH3)2 (3-metylbut-1-in)
Câu 4: Hiđrocacbon X ở điều kiện thường là chất khí. Khi oxi hoá hoàn toàn X thì thu được thể tích khí CO2 và hơi H2O là 2 : 1 ở cùng điều kiện. X phản ứng với dung dịch AgNO3 trong NH3 tạo kết tủa. Số cấu tạo của X thoả mãn tính chất trên là
A. 2.
B. 3.
C. 4.
D. 1.
Đáp án: A
Giải thích:
X thể khí → số C ≤ 4
Mà
Vì X phản ứng được với AgNO3/NH3
→ có liên kết 3 đầu mạch
→ có 2 công thức cấu tạo thỏa mãn: C2H2 ; C4H4 (CH≡C – CH=CH2)
Câu 5: Hidrat hóa có xúc tác 3,36 lit C2H2(dktc) thu được hỗn hợp A (hiệu suất phản ứng 60%). Cho hỗn hợp A tác dụng với AgNO3/NH3 thu được m gam kết tủa. Giá trị của m là :
A. 48,24
B. 33,84
C.14,4
D.19,44
Đáp án: B
Giải thích:
C2H2 + H2O CH3CHO
C2H2 Ag2C2 ↓
CH3CHO 2Ag ↓
Câu 6: Dẫn hỗn hợp khí X gồm etilen và axetilen qua bình đựng dung dịch AgNO3 trong NH3 (dư) đến khi phản ứng xảy ra hoàn toàn thì thu được 28,8 gam kết tủa và thấy có 2,912 lít khí (đo ở đktc) thoát ra. Phần trăm khối lượng của axetilen trong X là
A. 53,85%.
B. 46,15%.
C. 50,15%.
D. 49,85%.
Đáp án: B
Giải thích:
Chỉ có C2H2 phản ứng tạo Ag2C2
Câu 7: Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy một lượng hỗn hợp X cho qua chất xúc tác, đun nóng được hỗn hợp Y. Dẫn Y qua nước brom thấy bình nước brom tăng 10,8 gam và thoát ra 4,48 lit hỗn hợp khí (đktc), có tỉ khối so với hidro là 8. Thể tích khí O2 (đktc) vừa đủ để đốt cháy hoàn toàn hỗn hợp Y là
A. 26,88 lit
B. 44,8 lit
C. 33,6 lit
D. 22,4 lit
Đáp án: C
Giải thích:
M hh khí thoát ra = 6.2 = 16
→ Hỗn hợp khí thoát ra gồm: C2H6 và H2 dư
BTKL: mX = mY = m hh khí thoát ra + m bình Brom tăng
→ mX = mY = 0,2.8.2 + 10,8 = 14 gam
Đặt số mol C2H2 và H2 là x mol
→ mX = 26x + 2x = 14 → x = 0,5 mol
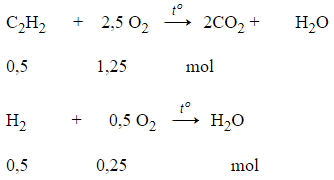
lít
Câu 8: Khi điều chế axetilen bằng phương pháp nhiệt phân nhanh CH4 thu được hỗn hợp A gồm axetilen, hiđro và một phần metan chưa phản ứng. Tỷ khối hơi cuả A so với hiđro bằng 5. Hiệu suất chuyển hóa metan thành axetilen là
A. 60%
B. 50%
C. 40%
D. 80%.
Đáp án: A
Giải thích:
Xét 1 mol CH4
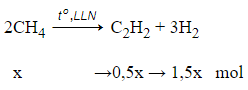
→ Sau phản ứng :
nhh = 1-x + 0,5x + 1,5x = 1 + x (mol)
Bảo toàn khối lượng :
mtrước = msau
→ 16.1 = 5.2.(1 + x)
→ x = 0,6 mol
→ H = 60%
Câu 9: Hỗn hợp X gồm propin (0,15 mol), axetilen (0,1 mol), etan (0,2 mol) và hiđro (0,6 mol). Nung nóng X với xúc tác Ni một thời gian, thu được hỗn hợp khí Y. Sục Y vào dung dịch AgNO3 trong NH3 dư, thu được a mol kết tủa và 15,68 lít (đktc) hỗn hợp khí Z. Khí Z phản ứng tối đa với 8 gam Br2 trong dung dịch. Giá trị của a là
A. 0,16.
B. 0,18.
C. 0,10.
D. 0,12.
Đáp án: C
Giải thích:
a mol kết tủa là số mol của ankin còn lại.
Số mol khí giảm là số mol H2 đã phản ứng:
Bảo toàn liên kết π ta có:
→ 2.0,15 + 2.0,1 – (0,35-a)
= 2a + 0,05 → a = 0,1 mol
Câu 10: Hỗn hợp X gồm 2 ankin. Đốt cháy hoàn toàn 0,05 mol hỗn hợp X trên thu được 0,17 mol CO2. Mặt khác cứ 0,05 mol hỗn hợp X phản ứng vừa đủ với 300 ml dung dịch AgNO3 0,1M trong dung dịch NH3. Hỗn hợp X là :
A. axetien, but - 1 - in
B. axetilen, propin
C. propin, but - 1 - in
D. propin, but - 2 - in
Đáp án: D
Giải thích:
Số C trung bình 2 ankin =
Vì Trong X có 1 ankin không phản ứng với AgNO3
Dựa vào đáp án → Chỉ có đáp án D thỏa mãn vì but – 2 – in không phản ứng với AgNO3
Câu 11: Trong phân tử ankin X, hidro chiếm 11,76% khối lượng. Công thức phân tử của X là :
A. C2H2
B. C5H8
C. C4H6
D. C3H4
Đáp án: B
Giải thích:
Công thức ankin là CnH2n-2 (n ≥ 2)
→ n = 5
Vậy X là C5H8
Câu 12: Đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm etan, propan, propilen, axetilen thu được số mol H2O ít hơn số mol CO2 là 0,02 mol. Mặt khác 0,1 mol X có thể làm mất màu tối đa m gam dung dịch Br2 16%. Giá trị của m là
A. 180
B. 120
C. 100
D.60
Đáp án: B
Giải thích:
Gọi số mol ankan là a, anken là b, ankin là c
→ a + b + c = 0,1
Mà
→ b + 2c
= a+ b+ c + c – a
= 0,1 + 0,02 = 0,12 mol
→ 0,12.160 = 19,2 gam.
→ m = 120g
Câu 13: Dẫn V lít (đktc) hỗn hợp X gồm axetilen và hiđro đi qua ống sứ đựng bột niken nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z được 2,24 lít khí CO2 (đktc) và 4,5 gam H2O. Giá trị của V bằng
A. 11,2
B. 13,44
C. 5,60
D. 8,96
Đáp án: A
Giải thích:
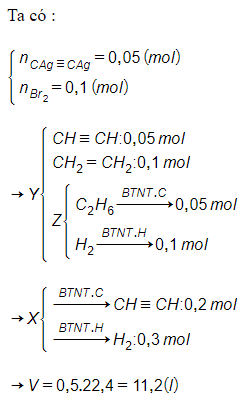
Câu 14: Trong bình kín chứa hiđrocacbon X và hiđro. Nung nóng bình đến khi phản ứng hoàn toàn thu được khí Y duy nhất. Ở cùng nhiệt độ, áp suất trong bình trước khi nung nóng gấp 3 lần áp suất trong bình sau khi nung. Đốt cháy một lượng Y thu được 8,8 gam CO2 và 5,4 gam nước. Công thức phân tử của X là
A. C2H2.
B. C2H4.
C. C4H6.
D. C3H4.
Đáp án: A
Giải thích:
→ Y chứa ankan
Ta có: nY = 0,3 – 0,2 = 0,1 mol
→ số C = 2
Vậy công thức phân tử của Y: C2H6
Vì áp suất trong bình trước khi nung nóng gấp 3 lần áp suất trong bình sau khi nung ở cùng điều kiện nhiệt độ
→ nhỗn hợp trước = 3n hỗn hợp sau
→ X là ankin C2H2
Câu 15: Hỗn hợp X gồm C2H2 và H2 lấy cùng số mol. Lấy một lượng hỗn hợp X cho đi qua chất xúc tác thích hợp, đun nóng được hỗn hợp Y gồm 4 chất. Dẫn Y qua bình đựng nước brom thấy khối luợng bình tăng 10,8 gam và thoát ra 4,48 lít khí Z (đktc) có ti khối so với H2 là 8. Thể tích O2 (đktc) cần để đốt cháy hoàn toàn hỗn hợp Y là
A. 33,6 lít.
B. 22,4 lít.
C. 16,8 lít.
D. 44,8 lít.
Đáp án: A
Giải thích:
Y gồm 4 chất :
C2H2(dư) ; C2H4 ; C2H6 ; H2
m bình tăng =
→ Khí thoát ra là C2H6 và H2
mZ = M.n = 8.2.0,2 = 3,2 g
Bảo toàn khối lượng:
Mà
→ x = 0,5
thể tích O2 cần để đốt cháy hỗn hợp Y = thể tích O2 cần để đốt cháy hỗn hợp X
lít
Câu 16: Cho 17,92 lít hỗn hợp X gồm 3 hiđrocacbon khí là ankan, anken và ankin lấy theo tỉ lệ mol 1:1:2 lội qua bình đựng dd AgNO3/NH3 lấy dư thu được 96 gam kết tủa và hỗn hợp khí Y còn lại. Đốt cháy hoàn toàn hỗn hợp Y thu được 13,44 lít CO2. Biết thể tích đo ở đktc. Khối lượng của X là
A. 19,2 gam.
B. 1,92 gam.
C. 3,84 gam.
D. 38,4 gam.
Đáp án: A
Giải thích:
Đặt nankan = x
→ nanken = x, n ankin = 2x
→ n hỗn hợp X = x + x + 2x = 0,8 mol
→ x = 0,2
ankin là C2H2
Gọi CTPT của ankan, anken lần lượt CnH2n+2 ; CmH2m
→ hỗn hợp X có 0,2 mol CH4 ; 0,2 mol C2H4 và 0,4 mol C2H2
→ m hỗn hợp = 19,2 g
Câu 17: Trong một bình kín chứa hiđrocacbon A ở thể khí (đktc) và O2 (dư). Bật tia lửa điện đốt cháy hết A đưa hỗn hợp về điều kiện ban đầu trong đó % thể tích của CO2 và hơi nước lần lượt là 30% và 20%. Công thức phân tử của A và % thể tích của hiđrocacbon A trong hỗn hợp là
A. C3H4 và 10%.
B. C3H4 và 90%.
C. C3H8 và 20%.
D. C4H6 và 30%.
Đáp án: A
Giải thích:
Ta có
Tỉ lệ % theo thể tích = tỉ lệ số mol
Giả sử
nC : nH = 3 : 4 → CTĐGN: (C3H4)n
Mà hidrocacbon ở thể khí nên n = 1 → C3H4
BTNT oxi :
Câu 18: Đốt cháy hoàn toàn 1 lít hỗn hợp khí gồm C2H2 và hiđrocacbon X sinh ra 2 lít khí CO2 và 2 lít hơi H2O (các thể tích khí và hơi đo trong cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X là
A. C2H4.
B. CH4.
C. C2H6.
D. C3H8.
Đáp án: C
Giải thích:
Ta có:
Hiđrocacbon X cũng có 2C.
Hiđrocacbon X có số H lớn hơn 4
→ có số H = 6
→ X là C2H6
Câu 19: Một hỗn hợp X gồm 0,14 mol axetilen, 0,1 mol vinylaxetilen, 0,2 mol H2 và một ít bột Ni trong bình kín. Nung hỗn hợp X thu được hỗn hợp Y gồm 7 hidrocacbon. Cho toàn bộ hỗn hợp Y đi qua bình đựng dung dịch AgNO3 dư/NH3, thu được m gam kết tủa vàng nhạt và 3,136 lít hỗn hợp khí Z (đktc) gồm 5 hidrocacbon thoát ra khỏi bình. Để làm no hoàn toàn hỗn hợp khí Z cần vừa đủ 120 ml dung dịch Br2 1M. Giá trị của m gần nhất với giá trị nào sau đây?
A. 25
B. 20
C. 34
D. 24
Đáp án: B
Giải thích:
∑nπ bđ = 0,14.2 + 0,1.3 = 0,58 mol
→ n lk π sau pư hidro hóa = 0,58 – 0,2 = 0,38 mol
nhh khí có lk 3 đầu mạch bị giữ lại :
0,14 + 0,1 – nZ = 0,1 mol (I)
n lk π trong hh Z = 0,12 mol (II)
→ Số mol π đã biết
= 2.n π(I) + nπ(II) = 0,32 mol ≠ n π thực tế = 0,38 mol
→ Trong 2 hợp chất bị AgNO3/ NH3 giữ lại chứa CH≡C – CH = CH2 dư
dư = 0,38 – 0,32 = 0,06 mol
Vì ∑n khí có liên kết ba = 0,1 mol → khí còn lại phải là C2H2 : 0,04 mol (Nếu là C4H6 thì Y không thể chứa tới 7 HC)
→ m↓ =
= 0,04. 240 + 0,06. 159
=19,14 g ≈ 20 g
Câu 20: Ankin C6H10 có bao nhiêu đồng phân phản ứng với dung dịch AgNO3/NH3 ?
A. 3
B. 4
C. 5
D. 6
Đáp án: B
Giải thích:
CH≡C-CH2-CH2-CH2-CH3
CH≡C-CH2-CH(CH3)-CH3
CH≡C-CH(CH3)-CH2-CH3
CH≡C-C(CH3)3
Vậy có 4 đồng phân thỏa mãn đề bài.
Câu 21: Hỗn hợp khí A gồm 0,6 mol H2 và 0,15 mol vinylaxetilen. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với H2 bằng 10. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là:
A. 16.
B. 0.
C. 24.
D. 8.
Đáp án: C
Giải thích:
BTKL: ns.Ms = nđ.Mđ
→ 0,6.2 + 0,15.52 = ns.20
→ ns = 0,45 mol
Số mol khí sau phản ứng giảm là số mol H2 phản ứng:
= nđ – ns = 0,75 – 0,45 = 0,3 mol
BT liên kết π ta có:
n π đầu – n π pư = n π sau
hay 3nvinylaxetilen – pư =
→ pư = 3.0,15 – 0,3 = 0,15 mol
→ = 0,15.160 = 24 gam
Câu 22: Hỗn hợp khí X chứa H2 và một ankin. Tỉ khối của X đối với H2 là 3,4. Đun nóng nhẹ X có mặt xúc tác Ni thì nó biến thành hỗn hợp Y không làm mất màu nước brom và có tỉ khối đối với H2 là 34/6. Công thức phân tử của ankin là :
A. C2H2
B. C3H4
C. C4H6
D. C4H8
Đáp án: A
Giải thích:
Chọn số mol hỗn hợp X là 1 mol (nX = 1 mol)
→ mX = 6,8 (g)
BTKL mX = mY = 6,8 (g)
→ nY = = 0,6 mol
= nX - nY = 1 - 0,6 = 0,4 mol
Vì hỗn hợp Y không làm mất màu nước Br2 nên trong Y chỉ có ankan.
![]()
Theo phương trình mol ankin = mol H2 phản ứng = 0,2 mol
mX = (14n – 2).0,2 + 2(1 - 0,2) = 6,8
→ n = 2. CTPT: C2H2.
Câu 23: Đốt cháy 3,4 gam hiđrocacbon A tạo ra 11g CO2. Mặt khác, khi cho 3,4g A tác dụng với lượng dư dung dịch AgNO3 trong NH3 thấy tạo thành a gam kết tủa. CTPT của A và a là:
A. C2H2; 8,5g
B. C3H4; 8,5g
C. C4H6; 8,75g
D. C5H8; 8,75g
Đáp án: D
Giải thích:
Do A tác dụng được với AgNO3 trong NH3 nên A là ank-1-in:
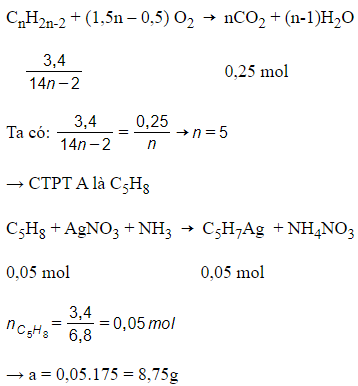
Câu 24: Hỗn hợp ban đầu gồm 1 ankin, 1 anken, 1 ankan và H2 với áp suất 4 atm. Đun nóng bình với Ni xúc tác để thực hiện phản ứng cộng sau đó đưa bình về nhiệt độ ban đầu được hỗn hợp Y, áp suất hỗn hợp Y là 3 atm. Tỉ khối hỗn hợp X và Y so với H2 lần lượt là 24 và x. Giá trị của x là
A. 18.
B. 34.
C. 24.
D. 32.
Đáp án: D
Giải thích:
Do nhiệt độ và thể tích bình không thay đổi
Giả sử nX = 4 → nY = 3
mX = 4.24.2 = 192 = mY
→ MY = = 64
→ x = 32
Câu 25: Hỗn hợp A gồm H2, C3H8, C3H4. Cho từ từ 12 lít A qua bột Ni xúc tác. Sau phản ứng được 6 lít khí duy nhất (các khí đo ở cùng điều kiện). Ti khối hơi của A so với H2 là
A. 11.
B. 22.
C. 26.
D. 13.
Đáp án: A
Giải thích:
Khí duy nhất là C3H8.
BTKL: mđ = ms
→ nđ.Mđ = ns.Ms
→ Mđ =
= 22
= 11
Câu 26: Đun nóng hỗn hợp X gồm 0,1 mol C3H4; 0,2 mol C2H4; 0,35 mol H2 với bột Ni xúc tác được hỗn hợp Y. Dẫn toàn bộ Y qua bình đựng dung dịch KMnO4 dư, thấy thoát ra 6,72 lít hỗn hợp khí Z (đktc) có tỉ khối so với H2 là 12. Bình đựng dung dịch KMnO4 tăng số gam là:
A. 17,2.
B. 9,6.
C. 7,2.
D. 3,1.
Đáp án: D
Giải thích:
Bảo toàn khối lượng
→ m hỗn hợp X = m hỗn hợp Y
= m bình tăng + m hỗn hợp khí thoát ra
m hỗn hợp X = m bình tăng + m hỗn hợp khí thoát ra
0,1.40 + 0,2.28 + 0,35.2 = m bình tăng + 0,3.12.2
→ m bình tăng = 3,1 g
Câu 27: Đốt cháy m gam hỗn hợp C2H6, C3H4, C3H8, C4H10 được 35,2 gam CO2 và 21,6 gam H2O. Giá trị của m là
A. 14,4.
B. 10,8.
C. 12.
D. 56,8.
Đáp án: C
Giải thích:
m hidrocacbon = mC + mH
= = 12g
Câu 28: Ankin là những hiđrocacbon không no, mạch hở, có công thức chung là
A. CnH2n+2 (n ≥ 1).
B. CnH2n (n ≥ 2).
C. CnH2n-2 (n ≥ 2).
D. CnH2n-6 (n ≥ 6).
Đáp án: C
Giải thích:
Ankin là những hiđrocacbon không no, mạch hở, có công thức chung là CnH2n-2
(n ≥ 2).
Câu 29: Trong các đồng phân mạch hở có cùng công thức phân tử C5H8 có bao nhiêu chất khi cộng H2 tạo sản phẩm isopentan:
A. 3
B. 5
C. 2
D. 4
Đáp án: A
Giải thích:
Độ bất bão hòa k = = 2
+ TH1: 1 liên kết ba
CH3 – CH(CH3) – C ≡ CH
+ TH2: 2 liên kết đôi
CH2 = C(CH3) – CH = CH3
CH3 – C(CH3) = C = CH2
→ Có 3 chất thỏa mãn đề bài.
Câu 30: Dẫn hỗn hợp X gồm 0,05 mol C2H2, 0,1 mol C3H4 và 0,1 mol H2 qua ống chứa Ni nung nóng một thời gian thu được hỗn hợp Y gồm 7 chất. Đốt cháy hoàn toàn Y bằng O2 dư rồi cho sản phẩm cháy hấp thụ hết vào 700 ml dung dịch NaOH 1M, thu được dung dịch Z. Tổng khối lượng chất tan trong Z là
A. 35,8
B. 45,6
C. 38,2
D. 40,2
Đáp án: D
Giải thích:
Đốt cháy Y cũng là cháy X
BTNT “C”
→
Lại có:
→ tạo 2 muối Na2CO3 và NaHCO3
Trong đó
= 0,3 mol
→
m chất tan trong Z = 0,3.106 + 0,1.84 = 40,2g
Các câu hỏi trắc nghiệm Hóa học lớp 11 có đáp án, chọn lọc khác:
Trắc nghiệm Benzen và đồng đẳng. Một số hidrocacbon thơm khác có đáp án
Trắc nghiệm Luyện tập: Hiđrocacbon thơm có đáp án
Trắc nghiệm Nguồn hiđrocacbon thiên nhiên có đáp án
Trắc nghiệm Hệ thống hóa về hidrocacbon thiên nhiên có đáp án
Xem thêm các chương trình khác:
- Trắc nghiệm Sinh học lớp 7 có đáp án
- Trắc nghiệm Toán lớp 7 có đáp án
- Trắc nghiệm Ngữ văn lớp 7 có đáp án
- Trắc nghiệm Sinh học 8 có đáp án
- Trắc nghiệm Toán lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Ngữ văn 8 có đáp án
- Trắc nghiệm Hóa học lớp 8 có đáp án
- Trắc nghiệm Địa Lí lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Tiếng Anh lớp 8 có đáp án
- Trắc nghiệm GDCD lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Lịch sử lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Vật Lí lớp 8 có đáp án
- Trắc nghiệm Công nghệ lớp 8 có đáp án
- Trắc nghiệm Tin học lớp 8 có đáp án
- Trắc nghiệm Sinh học lớp 9 có đáp án
- Trắc nghiệm Toán lớp 9 có đáp án
- Trắc nghiệm Ngữ văn 9 có đáp án
- Trắc nghiệm Hóa học lớp 9 có đáp án
- Trắc nghiệm Địa lí lớp 9 có đáp án
- Trắc nghiệm Tiếng Anh lớp 9 có đáp án
- Trắc nghiệm GDCD lớp 9 có đáp án
- Trắc nghiệm Lịch sử lớp 9 có đáp án
- Trắc nghiệm Vật lí lớp 9 có đáp án
- Trắc nghiệm Công nghệ lớp 9 có đáp án
- Trắc nghiệm Sinh học lớp 10 có đáp án
- Trắc nghiệm Toán lớp 10 có đáp án
- Trắc nghiệm Hóa học lớp 10 có đáp án
- Trắc nghiệm Ngữ văn lớp 10 có đáp án
- Trắc nghiệm Vật Lí lớp 10 có đáp án
- Trắc nghiệm Tiếng Anh lớp 10 có đáp án
- Trắc nghiệm Toán lớp 12 có đáp án
- Trắc nghiệm Sinh học lớp 12 có đáp án
- Trắc nghiệm Hóa học lớp 12 có đáp án
- Trắc nghiệm Ngữ văn lớp 12 có đáp án
- Trắc nghiệm Tiếng Anh lớp 12 có đáp án
- Trắc nghiệm Địa lí lớp 12 có đáp án
- Trắc nghiệm Vật Lí lớp 12 có đáp án
- Trắc nghiệm Công nghệ lớp 12 có đáp án
- Trắc nghiệm Giáo dục công dân lớp 12 có đáp án
- Trắc nghiệm Lịch sử lớp 12 có đáp án
- Trắc nghiệm Giáo dục quốc phòng - an ninh lớp 12 có đáp án
