TOP 40 câu Trắc nghiệm Phản ứng trao đổi ion trong dung dịch các chất điện li (có đáp án 2023) – Hóa 11
Bộ 40 bài tập trắc nghiệm Hóa lớp 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li có đáp án đầy đủ các mức độ giúp các em ôn trắc nghiệm Hóa 11.
Trắc nghiệm Hóa 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
Bài giảng Hóa 11 Bài 4: Phản ứng trao đổi ion trong dung dịch các chất điện li
Câu 1: Dãy ion không thể tồn tại đồng thời trong dung dịch là
A. Na+, OH−, Mg2+, NO−3
B. K+, H+, Cl−, SO2−4
C. HSO−3, Mg+, Ca2+, NO−3
D. OH−, Na+, Ba2+, Cl−
Đáp án: A
Giải thích:
Mg2++2OH−→Mg(OH)2↓
Câu 2: Phương trình phản ứng: Ba(OH)2 + 2HCl → BaCl2 + 2H2O có phương trình ion rút gọn là:
A. H+ + OH– → H2O
B. Ba2+ + 2OH– + 2H+ + 2Cl– → BaCl2 + 2H2O
C. Ba2+ + 2Cl– → BaCl2
D. Cl– + H+ → HCl
Đáp án: A
Giải thích:
Phương trình phân tử:
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
Phương trình ion đầy đủ:
Ba2+ + 2OH– + 2H+ + 2 → Ba2+ + 2 + 2H2O
Phương trình ion rút gọn:
H+ + OH– → H2O
Câu 3: Cho phản ứng: Mg(OH)2 + 2HCl → MgCl2 + H2O.
Phương trình ion thu gọn của phản ứng trên là
A. HCl + OH – → H2O + Cl−.
B. 2H+ + Mg(OH)2 → Mg2+ + 2H2O.
C. H+ + OH – → H2O.
D. 2HCl + Mg(OH)2 → Mg2+ + 2Cl− + 2H2O.
Đáp án: B
Giải thích:
Ta có phản ứng: Mg(OH)2 + 2HCl → MgCl2 + 2H2O.
Phương trình ion đầy đủ là:
Mg(OH)2 + 2H+ + 2Cl− → Mg2+ + 2Cl− + 2H2O.
→ Phương trình ion thu gọn là: Mg(OH)2 + 2H+ → Mg2+ + 2H2O.
Câu 4: Phương trình ion rút gọn Ba2+ + SO2−4 → BaSO4 tương ứng với phương trình phân tử nào sau đây?
A. Ba(OH)2 + CuSO4 → BaSO4 + Cu(OH)2.
B. H2SO4 + BaCO3 → BaSO4 + CO2 + H2O.
C. Na2SO4 + Ba(NO3)2 → BaSO4 + 2NaNO3.
D. H2SO4 + Ba(OH)2 → BaSO4 + 2H2O.
Đáp án: C
Giải thích:
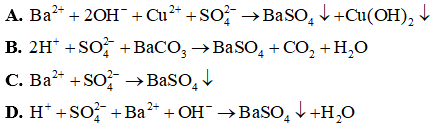
Câu 5: Phản ứng nào sau đây là phản ứng trao đổi ion trong dung dịch các chất điện li?
A. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
B. 2HCl + FeS → FeCl2 + H2S
C. NaOH + HCl → NaCl + H2O
D. Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Đáp án: C
Giải thích: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau: chất kết tủa, chất điện li yếu, chất khí.
Câu 6: Trong dung dịch, ion OH- không tác dụng được với ion
A. K+.
B. H+.
C. HCO−3
D. Fe3+.
Đáp án: A
Giải thích:
A. K+ không phản ứng được với
B. H++OH−→H2O
C. H++HCO−3→CO2+H2O
D. Fe3++3OH−→Fe(OH)3↓
Câu 7: Cho dung dịch X chứa các ion: H+, Ba2+, NO−3 vào dung dịch Y chứa các ion: Na+, SO2−3, SO2−4, S2−. Số phản ứng xảy ra là
A. 1.
B. 2.
C. 3.
D. 4.
Đáp án: D
Câu 8: Cho các phản ứng hóa học sau:
(1) NaHS + NaOH →
(2) Ba(HS)2 + KOH →
(3) Na2S + HCl →
(4) CuSO4 + Na2S →
(5) FeS + HCl →
(6) NH4HS + NaOH →
Các phản ứng đều có cùng một phương trình ion rút gọn là:
A. (3), (4), (5).
B. (1), (2).
C. (1), (2), (6).
D. (1), (6).
Đáp án: B
Giải thích:
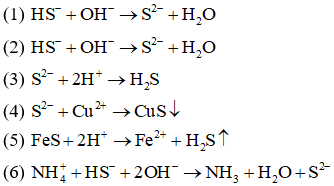
Câu 9: Phương trình ion thu gọn: Ca2++CO2−3→CaCO3↓ là của phản ứng xảy ra giữa cặp chất nào sau đây?
(1) CaCl2 + Na2CO3
(2) Ca(OH)2 + CO2
(3) Ca(HCO3)2 + NaOH
(4) Ca(NO3)2 + (NH4)2CO3
A. (1) và (2).
B. (2) và (3).
C. (1) và (4).
D. (2) và (4).
Đáp án: C
Giải thích:
(1), (4) có cùng phương trình ion thu gọn là Ca2++CO2−3→CaCO3↓
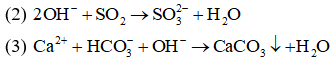
Câu 10: Phản ứng nào dưới đây là phản ứng trao đổi ion trong dung dịch?
A. Zn + H2SO4 ZnSO4 + H2
B. Fe(NO3)3 + 3NaOH Fe(OH)3 + 3NaNO3
C. 2Fe(NO3)3 + 2KI 2Fe(NO3)2 + I2 + 2KNO3
D. Zn + 2Fe(NO3)3 Zn(NO3)2 + 2Fe(NO3)2
Đáp án: B
Giải thích:
A, C, D là phản ứng oxi hóa khử
B là phản ứng trao đổi ion trong dung dịch:
Fe3++3OH−→Fe(OH)3↓
Câu 11: Phương trình H++OH−→H2O là phương trình ion thu gọn của phản ứng có phương trình sau:
A. NaOH + NaHCO3 → Na2CO3 + H2O
B. NaOH + HCl → NaCl + H2O
C. H2SO4 + BaCl2 → BaSO4 + 2HCl
D. 3HCl + Fe(OH)3 → FeCl3 + 3H2O
Đáp án: B
Giải thích:
Phản ứng có phương trình ion H++OH−→H2O
→ Phản ứng trung hòa axit với bazơ tan sinh ra muối tan và nước.
Câu 12: Cho phương trình phản ứng: KOH + HCl → KCl + H2O. Phương trình ion rút gọn của phản ứng trên là
A. H++OH−→H2O
B. K++Cl−→KCl
C. 2H++OH−→H2O
D. H++2OH−→H2O
Đáp án: A
Giải thích: Phương trình ion thu gọn là: H+ + OH-→ H2O
Câu 13: Dãy ion nào sau đây có thể tồn tại trong cùng một dung dịch?
A. Na+, Cl- , S2-, Cu2+.
B. K+,OH- , Ba2+, HCO−3.
C.NH+4 , Ba2+, NO−3,OH- .
D. HSO−4,NH+4 , Na+, NO−3.
Đáp án: D
Giải thích:
Các ion cùng tồn trong 1 dung dịch khi chúng không phản ứng với nhau.
A. Loại vì S2−+Cu2+→CuS↓
B. Loại vì Ba2++HCO−3+OH−→BaCO3↓+H2O
C. Loại vì NH+4+OH−→NH3↑+H2O
Câu 14: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi:
A. các chất phản ứng phải là những chất dễ tan.
B. các chất phản ứng phải là những chất điện li mạnh.
C. một số ion trong dung dịch kết hợp được với nhau tạo thành chất kết tủa hoặc chất khí hoặc chất điện li yếu.
D. phản ứng không phải là thuận nghịch.
Đáp án: C
Giải thích: Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau: chất kết tủa, chất điện li yếu, chất khí.
Câu 15: Cho 26,8 gam hỗn hợp X gồm CaCO3 và MgCO3 vào dung dịch HCl vừa đủ, thoát ra 6,72 lít khí (đktc) và dung dịch Y chứa m gam muối clorua. Giá trị của m là
A. 30,1.
B. 31,7.
C. 69,4.
D. 64,0.
Đáp án: A
Giải thích:
Gọi số mol CaCO3 và MgCO3 trong hỗn hợp X lần lượt là x, y mol
Phương trình:
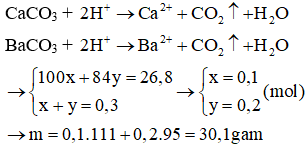
Câu 16: Cho 1 lít dung dịch X gồm Na2CO3 0,1M và (NH4)2CO3 0,25M tác dụng với 43 gam hỗn hợp rắn Y gồm BaCl2 và CaCl2. Sau khi phản ứng kết thúc, thu được 39,7 gam kết tủa. Tỉ lệ khối lượng của BaCl2 trong Y là
A. 24,19%.
B. 51,63%.
C. 75,81%.
D. 48,37%
Đáp án: D
Giải thích:
Dung dịch X {Na+ : 0,2 molNH+4 : 0,5 molCO2−3 : 0,35 mol
+ 43 gam Y {BaCl2 x molCaCl2 y mol
Phương trình ion:
Ba2++CO2−3→BaCO3↓Ca2++CO2−3→CaCO3↓
Giả sử CO2−3 dư
→{208x+111y=43197x+100y=39,7→{x=0,1y=0,2(mol)
nCO2−3 phản ứng = x + y = 0,3 mol < 0,35 mol
→ Thoả mãn
% mBaCl2=0,1.20843=48,37%
Câu 17: Phương trình ion rút gọn của phản ứng cho biết
A. Những ion nào tồn tại trong dung dịch.
B. Nồng độ những ion nào trong dung dịch lớn nhất.
C. Bản chất của phản ứng trong dung dịch các chất điện li.
D. Không tồn tại phân tử trong dung dịch các chất điện li.
Đáp án: C
Giải thích: Phương trình ion rút gọn của phản ứng cho biết bản chất của phản ứng trong dung dịch các chất điện li.
Câu 18: Dung dịch X có chứa 0,07 mol Na+; 0,02 mol SO2−4 và x mol OH-. Dung dịch Y có chứa ClO−4, NO−3 và y mol H+; tổng số mol ClO−4, NO−3 là 0,04 mol. Trộn X và T được 100 ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là :
A. 1.
B. 12.
C. 13.
D. 2.
Đáp án: A
Giải thích:
- Xét dung dịch X
Bảo toàn điện tích ta có:
0,07 = 0,02.2 + x
→ x = 0,03 mol
- Xét dung dịch Y
Bảo toàn điện tích ta có:
0,04 = y
- Trộn X với Y → Z
Phương trình ion: H++OH−→H2O
x < y→ H+dư, OH- hết
→ [H+] dư = 0,04−0,030,1=0,1M
→ pH = -lg[H+] dư = 1
Câu 19: Cho 47 gam K2O vào m gam dung dịch KOH 14%, thu được dung dịch KOH 21%. Giá trị của m là
A. 353.
B. 659.
C. 753.
D. 800.
Đáp án: B
Giải thích:
K2O + H2O → 2KOH
nK2O=0,5 mol→0,5.2.56+0,14m47+m=0,21→m=659 gam
Câu 20: Dung dịch X chứa 0,2 mol Ca2+; 0,15 mol Mg2+; 0,4 mol và a mol . Đun dung dịch X đến cạn thu được muối khan có khối lượng là
A. 43,8 gam
B. 44,1 gam
C. 34,8 gam
D. 25,5 gam
Đáp án: C
Giải thích:
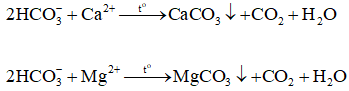
Bảo toàn điện tích ta có:
0,2.2 + 0,15.2 = 0,4 + a
→ a = 0,3 mol
→ nCO2−3muối khan = a2=0,15 mol
→ mmuối khan = 0,2.40 + 0,15.24 + 0,4.35,5 + 0,15.60 = 34,8 gam
Câu 21: Hãy chọn câu trả lời đúng: Phản ứng trao đổi trong dung dịch các chất điện li chỉ có thể xảy ra khi có ít nhất một trong các điều kiện sau:
A. tạo thành chất kết tủa.
B. tạo thành chất khí
C. tạo thành chất điện li yếu.
D. hoặc A, hoặc B, hoặc C.
Đáp án: D
Giải thích:
Phản ứng trao đổi trong dung dịch các chất điện li chỉ có thể xảy ra khi có ít nhất một trong các điều kiện sau:
- Tạo thành chất kết tủa
- Tạo thành chất khí
- Tạo thành chất điện li yếu
Câu 22: Dung dịch X chứa hỗn hợp cùng số mol CO2−3và . Cho dung dịch X tác dụng với dung dịch BaCl2 dư thu được 43 gam kết tủa. Số mol mỗi ion có trong dung dịch X là
A. 0,05
B. 0,1
C. 0,15
D. 0,20
Đáp án: B
Giải thích:
Phương trình hóa học:
Ba2++SO2−4→BaSO4↓
Ba2++CO2−3→BaCO3↓
Gọi số mol mỗi ion CO2−3 và SO2−4 là x mol
→ 197x + 233x = 43
→ x = 0,1 mol
Câu 23: Dung dịch X chứa các ion: Fe3+, SO2−4, NH+4, Cl−. Chia dung dịch X thành hai phần bằng nhau:
- Phần một tác dụng với lượng dư dung dịch NaOH, đun nóng thu được 0,672 lít khí (đktc) và 1,07 gam kết tủa.
- Phần hai cho tác dụng với lượng dư dung dịch BaCl2, thu được 4,66 gam kết tủa.
Tổng khối lượng (gam) các muối khan thu được khi cô cạn dung dịch X là
A. 3,52
B. 3,73
C. 7,04
D. 7,46
Đáp án: D
Giải thích:
- Phần 1:
Fe3++3OH−→Fe(OH)3↓
NH+4+OH−→NH3↑+H2O
nNH3=0,03 mol→nNH+4=0,03 moln↓=1,07107=0,01 mol→nFe3+=0,01 mol
- Phần 2:
Ba2++SO2−4→BaSO4↓→n↓=4,66233=0,02 mol→nSO2−4=0,02 mol
Áp dụng định luật bảo toàn điện tích ta có:
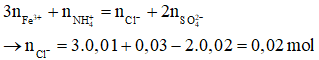
- Tổng khối lượng muối khan khi cô cạn dung dịch X là:
m = mcation + manion
→ m = 2.(0,01.56 + 0,03.18 + 0,02.35,5 + 0,02.96) = 7,46 gam
Câu 24: Cho dung dịch NaOH có dư tác dụng với dung dịch Ba(HCO3)2. Tìm phương trình ion rút gọn của phản ứng này.
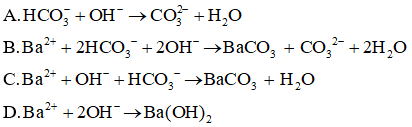
Đáp án: B
Giải thích:
Phương trình ion rút gọn:
![]()
Câu 25: Cho dung dịch chứa 0,1 mol (NH4)2CO3 tác dụng với dung dịch chứa 34,2 gam Ba(OH)2. Sau phản ứng thu được m(g) kết tủa. Giá trị của m là
A. 39,4.
B. 17,1.
C. 15,5.
D. 19,7.
Đáp án: D
Giải thích:
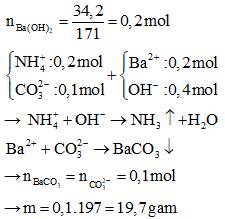
Câu 26: Phương trình phân tử nào sau đây, có phương trình ion rút gọn là
CO2−3+2H+→CO2↑+H2O
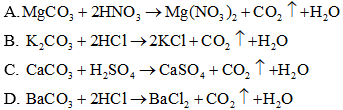
Đáp án: B
Giải thích:
Phương trình ion rút gọn
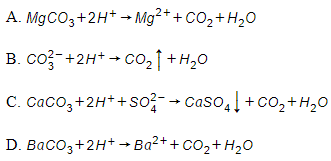
Câu 27: Trộn 40 ml dung dịch H2SO4 0,25M với 60ml dung dịch NaOH 0,5M. Giá trị pH của dung dịch thu được sau khi trộn là
A. pH=14.
B. pH=13.
C. pH=12.
D. pH= 9.
Đáp án: B
Giải thích:
nH2SO4=0,01 mol→nH+=0,02 molnNaOH=0,03 mol>0,02
→ H+ hết, OH- dư
Sau phản ứng có:
[OH-] = 0,03−0,020,04+0,06=0,1M
→ pH = 14 + lg[OH-] = 13
Câu 28: Một trong các nguyên nhân gây bệnh đau dạ dày là do lượng axit trong dạ dày quá cao. Để giảm bớt lượng axit, người ta thường uống dược phẩm Nabica (NaHCO3). Phương trình ion rút gọn của phản ứng xảy ra là
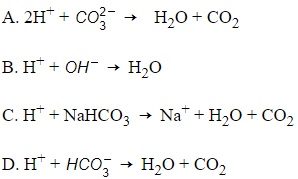
Đáp án: D
Giải thích: H+ + HCO3- → H2O + CO2
Câu 29: Trong dãy các ion sau dãy nào chứa các ion đều phản ứng được với
A. NH+4, HCO−3, CO2−3
B. Mg2+, HSO−3, SO2−3
C. H+, Ba2+, Al3+
D. Fe3+, HPO2−4, HS−
Đáp án: D
Giải thích:
A loại vì CO2−3 không phản ứng với OH-
B loại vì SO2−3 không phản ứng với OH-.
C loại vì Ba2+ không phản ứng với OH-.
D thỏa mãn.
Câu 30: Cho dung dịch Ba(OH)2 dư vào dung dịch đồng thời chứa các ion: NH+4, HCO−3, SO2−4, K+. Số phản ứng dạng ion thu gọn xảy ra là
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án: C
Giải thích:
Ba(OH)2 → Ba2++2OH−
1. NH+4+OH−→NH3↑+H2O
2. OH−+HCO−3→CO2−3+H2O
3. Ba2++SO2−4→BaSO4↓
4. Ba2++CO2−3→BaCO3↓
Bài 31: Cho 26,8 gam hỗn hợp X gồm CaCO3 và MgCO3 vào dung dịch HCl vừa đủ, thoát ra 6,72 lít khí (đktc) và dung dịch Y chứa m gam muối clorua. Giá trị của m là
A. 30,1.
B. 31,7.
C. 69,4.
D. 64,0.
Đáp án: A
Bài 32: Cho 47 gam K2O vào m gam dung dịch KOH 14%, thu được dung dịch KOH 21%. Giá trị của m là
A. 353.
B. 659.
C. 753.
D. 800.
Đáp án: B
Bài 33: Để pha được 1 lít dung dịch chứa Na2SO4 0,04M, K2SO4 0,05 M và KNO3 0,08M cần lấy
A. 12,15 gam K2SO4 và 10,2 gam NaNO3.
B. 8,08 gam KNO3 và 12,78 gam Na2SO4.
C. 15,66 gam K2SO4 và 6,8 gam NaNO3.
D. 9,09 gam KNO3 và 5,68 gam Na2SO4.
Đáp án: C
Bài 34: Hòa tan một hỗn hợp 7,2 gam gồm hai muối sunfat của kim loại A và B vào nước được dung dịch X. Thêm vào dung dịch X môt lượng vừa đủ BaCl2 đã kết tủa ion SO42-, thu được 11,65 gam BaSO4 và dung dịch Y. Tổng khối lượng hai muối clorua trong dung dịch Y là
A. 5,95 gam.
B. 6,5 gam.
C. 7,0 gam.
D. 8,2 gam.
Đáp án: A
Bài 35: Cho 1 lít dung dịch gồm Na2CO3 0,1M và (NH4)2CO3 0,25M tác dụng với 43 gam hỗn hợp rắn Y gồm BaCl2 và CaCl2. Sau khi phản ứng kết thúc, thu được 39,7 gam kết tủa. Tỉ lệ khối lượng của BaCl2 trong Y là
A. 24,19%.
B. 51,63%.
C. 75,81%.
D. 48,37%
Đáp án: D
Bài 36: Cho dung dịch Fe2(SO4)3 phản ứng với dung dịch Na2CO3 thì sản phẩm tạo ra là:
A. Fe2(CO3)3 và Na2SO4
B. Na2SO4; CO2 và Fe(OH)3
C. Fe2O3; CO2; Na2SO4 và CO2
D. Fe(OH)3; CO2; Na2SO4; CO2
Đáp án: B
Bài 37: Phương trình ion rút gọn của phản ứng cho biết
A. Những ion nào tồn tại trong dung dịch.
B. Nồng độ những ion nào trong dung dịch lớn nhất.
C. Bản chất của phản ứng trong dung dịch các chất điện li.
D. Không tồn tại phân tử trong dung dịch các chất điện li.
Đáp án: C
Bài 38: Các ion nào sau không thể cùng tồn tại trong một dung dịch
A. Na+, Mg2+, NO3-, SO42-.
B. Ba2+, Al3+, Cl-, HSO4-.
C. Cu2+, Fe3+, SO42-, Cl-.
D. K+, NH4+, OH-, PO43-.
Đáp án: B
Bài 39: Các ion có thể tồn tại trong cùng một dung dịch là:
A. Na+, NH4+, SO42-, Cl-.
B. Mg2+, Al3+, NO3-, CO32-.
C. Ag+, Mg2+, NO3-, Br-.
D. Fe2+, Ag+, NO3-, CH3COO-.
Đáp án: A
Bài 40: Dung dịch X có chứa 0,07 mol Na+, 0,02 mol SO42-, và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4-, NO3- là 0,04 mol. Trộn X và T được 100 ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là :
A. 1.
B. 12.
C. 13.
D. 2.
Đáp án: A
Các câu hỏi trắc nghiệm Hóa học lớp 11 có đáp án, chọn lọc khác:
Trắc nghiệm Xicloankan có đáp án
Xem thêm các chương trình khác:
- Trắc nghiệm Sinh học lớp 7 có đáp án
- Trắc nghiệm Toán lớp 7 có đáp án
- Trắc nghiệm Ngữ văn lớp 7 có đáp án
- Trắc nghiệm Sinh học 8 có đáp án
- Trắc nghiệm Toán lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Ngữ văn 8 có đáp án
- Trắc nghiệm Hóa học lớp 8 có đáp án
- Trắc nghiệm Địa Lí lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Tiếng Anh lớp 8 có đáp án
- Trắc nghiệm GDCD lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Lịch sử lớp 8 có đáp án (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Trắc nghiệm Vật Lí lớp 8 có đáp án
- Trắc nghiệm Công nghệ lớp 8 có đáp án
- Trắc nghiệm Tin học lớp 8 có đáp án
- Trắc nghiệm Sinh học lớp 9 có đáp án
- Trắc nghiệm Toán lớp 9 có đáp án
- Trắc nghiệm Ngữ văn 9 có đáp án
- Trắc nghiệm Hóa học lớp 9 có đáp án
- Trắc nghiệm Địa lí lớp 9 có đáp án
- Trắc nghiệm Tiếng Anh lớp 9 có đáp án
- Trắc nghiệm GDCD lớp 9 có đáp án
- Trắc nghiệm Lịch sử lớp 9 có đáp án
- Trắc nghiệm Vật lí lớp 9 có đáp án
- Trắc nghiệm Công nghệ lớp 9 có đáp án
- Trắc nghiệm Sinh học lớp 10 có đáp án
- Trắc nghiệm Toán lớp 10 có đáp án
- Trắc nghiệm Hóa học lớp 10 có đáp án
- Trắc nghiệm Ngữ văn lớp 10 có đáp án
- Trắc nghiệm Vật Lí lớp 10 có đáp án
- Trắc nghiệm Tiếng Anh lớp 10 có đáp án
- Trắc nghiệm Toán lớp 12 có đáp án
- Trắc nghiệm Sinh học lớp 12 có đáp án
- Trắc nghiệm Hóa học lớp 12 có đáp án
- Trắc nghiệm Ngữ văn lớp 12 có đáp án
- Trắc nghiệm Tiếng Anh lớp 12 có đáp án
- Trắc nghiệm Địa lí lớp 12 có đáp án
- Trắc nghiệm Vật Lí lớp 12 có đáp án
- Trắc nghiệm Công nghệ lớp 12 có đáp án
- Trắc nghiệm Giáo dục công dân lớp 12 có đáp án
- Trắc nghiệm Lịch sử lớp 12 có đáp án
- Trắc nghiệm Giáo dục quốc phòng - an ninh lớp 12 có đáp án
