Công thức tính nhanh số mol OH- khi cho H2S tác dụng với dung dịch kiềm (2025) chi tiết nhất
Với tài liệu về Công thức tính nhanh số mol OH- khi cho H2S tác dụng với dung dịch kiềm bao gồm: lý thuyết và bài tập cũng như những định nghĩa, tính chất, các dạng bài sẽ giúp bạn nắm vững kiến thức và học tốt môn Hóa học hơn.
Công thức tính nhanh số mol OH- khi cho H2S tác dụng với dung dịch kiềm
1. Công thức tính nhanh
TH1 : Khí H2S tác dụng dung dịch kiềm chỉ sinh ra muối
nOH- = nHS- = nH2S
TH2: Khí H2S tác dụng dung dịch kiềm chỉ sinh ra muối
nOH- = 2nS2- = 2nH2S
TH3: : Khí H2S tác dụng dung dịch kiềm sinh ra hỗn hợp muối HS- và S2-
nOH-= nH2S + nS2- = 2nH2S - nHS- = nHS- + 2nS2-
2. Bạn nên biết
Khi cho khí H2S tác dụng dung dịch NaOH hoặc KOH
H2S + NaOH →NaHS + H2O (1);
H2S + 2NaOH →Na2S + 2H2O (2)
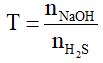
T ≤ 1 : tạo muối NaHS phản ứng (1) và H2Sdư
1 < T < 2 : tạo 2 muối NaHSvà Na2S : phản ứng (1) và (2)
T > 2 : tạo muối Na2S phản ứng (2) và NaOH dư
3. Mở rộng
Khi cho a mol H2S vào b mol Ba(OH)2 thu được dung dịch A
H2S + Ba(OH)2 -> BaS + 2 H2O (1)
2 H2S + Ba(OH)2 -> Ba(HS)2 + 2H2O (2)
Khi a < b, chỉ xảy ra phương trình 1, A chứa BaS và Ba(OH)2 dư
Khi a = b, chỉ xảy ra phương trình 1, A chứa BaS
Khi 2b > a, xảy ra phương trình (1)(2), A chứa BaS và Ba(HS)2
Khi 2b = a, chỉ xảy ra phương trình 2, A chứa Ba(HS)2
Khi 2b < a, chỉ xảy ra phương trình 2, A chứa Ba(HS)2
4. Bài tập minh họa
Câu 1: Hấp thụ hoàn toàn 4,48 lít khí H2S (đkc) vào 100ml dung dịch KOH 1,5M. Tính khối lượng muối thu được sau phản ứng?
A. 9,8 gam
B. 10,2 gam
C. 10,8 gam
D. 11,2 gam
Hướng dẫn
nH2S = 0,2 mol
nKOH = 0,1.1,5 =0,15 mol
Vì 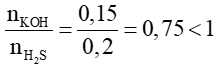 nên muối gồm KHS ; H2S dư
nên muối gồm KHS ; H2S dư
PTHH :
KOH + H2S -> KHS + H2O
-> nKHS = nKOH = 0,15mol
-> nKHS = 0,15.72 =10,8 gam
Đáp án C
Câu 2: Dẫn 3,36 lít khí H2S (đktc) vào 250 ml dung dịch KOH 2M, sau khi phản ứng hoàn toàn thu được dung dịch X. Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là:
A. 16,5 gam.
B. 27,5 gam.
C. 14,6 gam.
D. 27,7gam.
Hướng dẫn
nH2S =0,15 mol ; nKOH = 0,5 mol
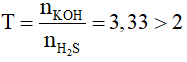
-> Chỉ tạo muối K2S
Phương trình hóa học:
H2S + 2KOH -> K2S + H2O
Dung dịch X gồm K2S và KOH dư
Chất rắn khan gồm K2S và KOH dư
nK2S = nH2S = 0,15 mol ; nKOHdu = 2nH2S = 0,3 mol
-> nKOHdu = 0,5-0,3 =0,2 mol
-> mcr = mK2S + mKOHdu = 0,15.110 + 0,2.56 = 27,7 gam
Đáp án D
Câu 3: Hấp thụ hoàn toàn V lít khí H2S (đktc) vào 200 ml dung dịch NaOH 1,25M thu được dung dịch X có chứa 12,3 gam hỗn hợp muối. Giá trị của V là
A. 4,48 lít.
B. 5,60 lít.
C. 3,36 lít.
D. 4,032 lít.
Hướng dẫn
Dung dịch X chứa hỗn hợp muối gồm NaHS (x mol) và Na2S (y mol)
mmuối = 56x+78y = 12,3 (1)
Bảo toàn nguyên tố Na:
nNaOH = nNaHS + 2. nNa2S
0,2. 1,25 = x+ 2y (2)
Từ (1) và (2) -> 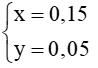
Bảo toàn nguyên tố S:
nH2S = nNaHS + nNa2S = 0,15 + 0,05 = 0,2 mol
-> VH2S = 0,2.22,4 = 4,48 lit
Đáp án A
Xem thêm các dạng bài tập và công thức Hoá học lớp 10 hay, chi tiết khác:
Các dạng bài toán tính tốc độ trung bình của phản ứng hóa học
Trắc nghiệm lý thuyết Tốc độ phản ứng và cân bằng hóa học
Các dạng bài toán tốc độ phản ứng trong đề thi Đại học
Các dạng bài toán tính nồng độ các chất ở trạng thái cân bằng
Xem thêm các chương trình khác:
- Giải sgk Vật Lí 10 | Giải bài tập Vật lí 10 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 10
- Tóm tắt tác phẩm Ngữ văn 10
- Soạn văn 10 (hay nhất) | Để học tốt Ngữ Văn 10 (sách mới)
- Soạn văn 10 (ngắn nhất) | Để học tốt Ngữ văn 10 (sách mới)
- Văn mẫu lớp 10 (cả ba sách) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Lịch sử 10 | Giải bài tập Lịch sử 10 Học kì 1, Học kì 2 (sách mới)
