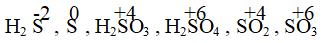Các dạng bài toán xác định số oxi hóa của các nguyên tố và cách giải
Với tài liệu về Các dạng bài toán xác định số oxi hóa của các nguyên tố bao gồm: lý thuyết và bài tập cũng như những định nghĩa, tính chất, các dạng bài sẽ giúp bạn nắm vững kiến thức và học tốt môn Hóa học hơn.
Các dạng bài toán xác định số oxi hóa của các nguyên tố
A. Phương pháp & Ví dụ
I. Lý thuyết và Phương pháp giải
- Quy tắc 1 : Số oxi hóa của các nguyên tố trong đơn chất bằng 0.
Ví dụ : Số oxi hóa của các nguyên tố Na, Fe, H, O, Cl trong đơn chất tương ứng Na, Fe, H2, O2, Cl2 đều bằng 0.
- Quy tắc 2 : Trong hầu hết các hợp chất :
Số oxi hóa của H là +1 (trừ các hợp chất của H với kim loại như NaH, CaH2, thì H có số oxi hóa –1).
Số oxi hóa của O là –2 (trừ một số trường hợp như H2O2, F2O, oxi có số oxi hóa lần lượt là : –1, +2).
- Quy tắc 3 : Trong một phân tử, tổng đại số số oxi hóa của các nguyên tố bằng 0. Theo quy tắc này, ta có thể tìm được số oxi hóa của một nguyên tố nào đó trong phân tử nếu biết số oxi hóa của các nguyên tố còn lại.
- Quy tắc 4 : Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích của ion đó. Trong ion đa nguyên tử, tổng đại số số oxi hóa của các nguyên tử trong ion đó bằng điện tích của nó.
Ví dụ : Số oxi hóa của Na, Zn, S và Cl trong các ion Na+, Zn2+, S2-, Cl- lần lượt là : +1, +2, –2, –1.
Tổng đại số số oxi hóa của các nguyên tố trong các ion SO42-, MnO4-, NH4+ lần lượt là : –2, –1, +1.
Chú ý: Để biểu diễn số oxi hóa thì viết dấu trước, số sau, còn để biểu diễn điện tích của ion thì viết số trước, dấu sau.
Nếu điện tích là 1+ (hoặc 1–) có thể viết đơn giản là + (hoặc -) thì đối với số oxi hóa phải viết đầy đủ cả dấu và chữ (+1 hoặc –1).
Trong hợp chất, kim loại kiềm, kiềm thổ, nhôm luôn có số oxi hóa lần lượt là : +1, +2, +3.
II. Ví dụ minh họa
Ví dụ 1: Tìm số oxi hóa của S trong phân tử H2SO4 ?
Hướng dẫn:
Gọi số oxi hóa của S trong H2SO4 là x, ta có :
2.(+1) + 1.x + 4.(–2) = 0 → x = +6
Vậy số oxi hóa của S là +6.
Ví dụ 2 : Tìm số oxi hóa của Mn trong ion MnO4- ?
Hướng dẫn:
Gọi số oxi hóa của Mn là x, ta có :
1.x + 4.( –2) = –1 → x = +7
Vậy số oxi hóa của Mn là +7.
Ví dụ 3. Xác định số oxi hóa của các ion sau: Na+, Cu2+, Fe2+, Fe3+, Al3+.
Hướng dẫn:
| Ion | Na+ | Cu2+ | Fe2+ | Fe3+ | Al3+ |
| Số oxi hóa | +1 | +2 | +2 | +3 | +3 |
*Lưu ý: Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích của ion đó.
B. Bài tập trắc nghiệm
Câu 1. Cho các hợp chất : NH , NO2, N2O, NO , N2
Thứ tự giảm dần số oxi hóa của N là :
A. N2 > NO > NO2 > N2O > NH .
B. NO > N2O > NO2 > N2 > NH .
C. NO > NO2 > N2O > N2 > NH .
D. NO > NO2 > NH > N2 > N2O.
Lời giải:
Đáp án: C
Số oxi hóa của N trong các hợp chất NH , NO2, N2O, NO , N2 lần lượt là: +3, +4, +1, +5, 0
Câu 2. Số oxi hóa của Cl trong các hợp chất sau lần lượt là: HCl, HClO, NaClO3, HClO4
A. -1, 0, +5, +7 B. -1, +1, +5, +7
C. +1, +3, +1 , +5 D. +1, -1, +3, +5
Lời giải:
Đáp án: B
Câu 3. Xác định số oxi hóa của crom trong các hợp chất sau: Cr2O3, K2CrO4, Cr2(SO4)3 , K2Cr2O7
A. +3, +6, + 3; +6 B. +1, +3, +1 , +5
C. +3, +7, + 4; +6 D. +3, +4, +2; +7
Lời giải:
Đáp án: A
Câu 4. Cho biết thứ tự giảm dần số oxi hóa của các ion sau: MnO4-, SO42-, NH4+, ClO3-.
A. MnO4-, SO42-, NH4+, ClO3-
B. MnO4-, NH4+, ClO3- SO42-.
C. NH4+, ClO3-, MnO4-, SO42-.
D. NH4+, ClO3- , SO42-, MnO4-.
Lời giải:
Đáp án: D
Số oxi hóa của MnO4-, SO42-, NH4+, ClO3- lần lượt là: +7, +6, +3, +5
Câu 5. Cho các chất: H2S, S, H2SO3, H2SO4, SO2, SO3. Xác định số oxi hóa của S trong các chất trên
A. -2, 0, +4, +6, +4, +6
B. -2, 0, +4, +6, +2, +3
C. -2, 0, +3, +4, +4, +6
D. +2, 1, +4, +6, +4, -3
Lời giải:
Đáp án: A
Áp dụng quy tắc xác định số oxi hóa:
Xem thêm các dạng bài tập và công thức Hoá học lớp 10 hay, chi tiết khác:
Các dạng bài toán Phương pháp, cách cân bằng phản ứng oxi hóa khử
Các dạng bài toán Phương pháp bảo toàn electron
Xem thêm các chương trình khác:
- Giải sgk Vật Lí 10 | Giải bài tập Vật lí 10 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 10
- Tóm tắt tác phẩm Ngữ văn 10
- Soạn văn 10 (hay nhất) | Để học tốt Ngữ Văn 10 (sách mới)
- Soạn văn 10 (ngắn nhất) | Để học tốt Ngữ văn 10 (sách mới)
- Văn mẫu lớp 10 (cả ba sách) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Lịch sử 10 | Giải bài tập Lịch sử 10 Học kì 1, Học kì 2 (sách mới)