Vở bài tập KHTN 8 Bài 2 (Cánh diều): Phản ứng hóa học và năng lượng của phản ứng hóa học
Với giải vở bài tập Khoa học tự nhiên 8 Bài 2: Phản ứng hóa học và năng lượng của phản ứng hóa học sách Cánh diều hay nhất, ngắn gọn sẽ giúp học sinh dễ dàng làm bài tập trong VBT KHTN 8 Bài 2.
Giải VBT KHTN 8 Bài 2: Phản ứng hóa học và năng lượng của phản ứng hóa học
A. Học theo sách giáo khoa
CH1 trang 15 Vở bài tập KHTN 8: Những quá trình biến đổi hoá học là:
…………………………………………………………………………………………………………………………………………………………………………………………
|
……………………………………………………………………… ……………………………………………………………………… ……………………………………………………………………… ……………………………………………………………………… |
Lời giải:
Những quá trình biến đổi hoá học là:
+ Quá trình cho dung dịch HCl vào bình chứa Zn sinh ra khí H2.
+ Quá trình đốt cháy hydrogen trong bình chứa oxygen tạo thành nước (H2O).
|
Phản ứng hoá học là quá trình biến đổi từ chất này thành chất khác. Chất ban đầu bị biến đổi trong phản ứng được gọi là chất tham gia phản ứng, chất tạo thành sau phản ứng được gọi là chất sản phẩm. |
LT1 trang 15 Vở bài tập KHTN 8: Xác định chất phản ứng và chất sản phẩm:
a) …………………………………………………………………………………………………………………………………………………………………………………………
b) …………………………………………………………………………………………………………………………………………………………………………………………
Lời giải:
a)
+ Chất tham gia phản ứng là methane và oxygen.
+ Chất sản phẩm là carbon dioxide và nước.
b)
+ Chất tham gia phản ứng là carbon và khí oxygen.
+ Chất sản phẩm là khí carbon dioxide.
CH2 trang 16 Vở bài tập KHTN 8:
a) Trước phản ứng những nguyên tử liên kết với nhau:
…………………………………………………………………………………………………………………………………………………………………………………………
b) Sau phản ứng những nguyên tử liên kết với nhau:
…………………………………………………………………………………………………………………………………………………………………………………………
c)
…………………………………………………………………………………………………………………………………………………………………………………………
|
………………………………………………… ………………………………………………… ………………………………………………… ………………………………………………… |
Lời giải:
a) Trước phản ứng những nguyên tử liên kết với nhau: 2 nguyên tử H liên kết với nhau; 2 nguyên tử O liên kết với nhau.
b) Sau phản ứng những nguyên tử liên kết với nhau: 1 nguyên tử O liên kết với 2 nguyên tử H.
c) Số nguyên tử H và số nguyên tử O trước và sau phản ứng là bằng nhau.
|
- Các biến đổi hoá học xảy ra khi có sự phá vỡ liên kết trong các chất tham gia phản ứng và sự hình thành các liên kết mới để tạo ra chất sản phẩm. - Trong phản ứng hoá học, chỉ có liên kết giữa các nguyên tử thay đổi làm cho phân tử này biến đổi thành phân tử khác, kết quả là chất này biến đổi thành chất khác. Số nguyên tử của mỗi nguyên tố trước và sau phản ứng không thay đổi. |
CH3 trang 16 Vở bài tập KHTN 8: Sự khác biệt về tính chất của nước với hydrogen và oxygen:
…………………………………………………………………………………………………………………………………………………………………………………………
Lời giải:
Sự khác biệt về tính chất của nước với hydrogen và oxygen: Ở điều kiện thường, nước ở thể lỏng; hydrogen và oxygen ở thể khí.
TN1 trang 16 Vở bài tập KHTN 8:
- Trạng thái của đường trước và sau khi đun:
…………………………………………………………………………………………………………………………………………………………………………………………
- Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra là:
…………………………………………………………………………………………………………………………………………………………………………………………
|
………………………………………………… ………………………………………………… ………………………………………………… |
Lời giải:
- Trạng thái của đường trước và sau khi đun:
+ Trước khi đun: Đường là chất rắn, màu trắng, vị ngọt, không mùi, tan trong nước.
+ Sau khi đun: Thu được chất rắn, màu đen, vị đắng, mùi khét, không tan trong nước.
- Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra là: có sự thay đổi màu sắc (từ trắng sang đen); vị (từ ngọt sang đắng); mùi (từ không mùi sang khét); độ tan (từ tan trong nước sang chất mới không tan trong nước).
|
Để nhận biết có phản ứng hoá học xảy ra có thể dựa vào các dấu hiệu sau: - Có sự thay đổi màu sắc, mùi, … của các chất; tạo ra chất khí hoặc chất không tan (kết tủa); … - Có sự toả nhiệt và phát sáng. |
LT2 trang 17 Vở bài tập KHTN 8: Những dấu hiệu thường để nhận biết có phản ứng hoá học xảy ra là:
…………………………………………………………………………………………………………………………………………………………………………………………
Lời giải:
Những dấu hiệu thường để nhận biết có phản ứng hoá học xảy ra là:
+ Để nhận biết có phản ứng hoá học xảy ra có thể dựa vào các dấu hiệu sau: có sự thay đổi màu sắc, mùi, … của các chất; tạo ra chất khí hoặc chất không tan (kết tủa); …
+ Ngoài ra, sự toả nhiệt và phát sáng cũng có thể là dấu hiệu của phản ứng hoá học xảy ra.
VD1 trang 17 Vở bài tập KHTN 8: Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra là:
…………………………………………………………………………………………………………………………………………………………………………………………
Lời giải:
Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra là: sự thay đổi vị của nước đường (từ vị ngọt sang vị chua).
TH1 trang 17 Vở bài tập KHTN 8:
……………………………………………………………………………………………
- Cảm nhận khi chạm tay vào thành bình:
……………………………………………………………………………………………
Lời giải:
- Hiện tượng: Mẩu than cháy sáng trong bình khí oxygen.
- Cảm nhận khi chạm tay vào thành bình: Chạm tay vào thành bình thấy nóng.
TH2 trang 17 Vở bài tập KHTN 8:
……………………………………………………………………………………………
- Cảm nhận khi chạm tay vào thành bình:
……………………………………………………………………………………………
Lời giải:
- Hiện tượng: Bột NaHCO3 tan dần, có khí thoát ra.
- Cảm nhận khi chạm tay vào thành bình: Chạm tay vào thành bình thấy lạnh.
CH4 trang 17 Vở bài tập KHTN 8:
Phản ứng toả nhiệt: ………………………………………………………………………
Phản ứng thu nhiệt: ………………………………………………………………………
|
……………………………………………………… ……………………………………………………… ……………………………………………………… ……………………………………………………… |
Lời giải:
Phản ứng toả nhiệt: Phản ứng ở thí nghiệm 2.
Phản ứng thu nhiệt: Phản ứng ở thí nghiệm 3.
+ Phản ứng toả ra năng lượng (dưới dạng nhiệt) được gọi là phản ứng toả nhiệt. Phản ứng toả nhiệt làm nóng môi trường xung quanh.
+ Phản ứng thu vào năng lượng (dưới dạng nhiệt) được gọi là phản ứng thu nhiệt. Phản ứng thu nhiệt làm lạnh môi trường xung quanh.
LT3 trang 18 Vở bài tập KHTN 8:
a) …………………………………………………………………………………………………………………………………………………………………………………………
b) …………………………………………………………………………………………………………………………………………………………………………………………
Lời giải:
a) Phân huỷ đường tạo thành than và nước là phản ứng thu nhiệt.
b) Cồn cháy trong không khí là phản ứng toả nhiệt.
2. Ứng dụng của phản ứng toả nhiệt trang 18 Vở bài tập KHTN 8:
|
…………………………………………………………… …………………………………………………………… …………………………………………………………… …………………………………………………………… |
Lời giải:
Trong sản xuất và đời sống, các phản ứng toả nhiệt có ứng dụng chính là cung cấp năng lượng nhiệt (nhiệt năng) cho các ngành công nghiệp, làm cho các động cơ hay máy phát điện hoạt động.
…………………………………………………………………………………………………………………………………………………………………………………………
Lời giải:
- Một số phản ứng xảy ra trong tự nhiên là phản ứng thu nhiệt:
+ Phản ứng quang hợp (là phản ứng thu năng lượng dưới dạng ánh sáng).
+ Phản ứng nung vôi.
- Một số phản ứng xảy ra trong tự nhiên là phản ứng toả nhiệt:
+ Phản ứng tạo gỉ sắt.
+ Phản ứng oxi hoá glucose trong cơ thể.
Ghi nhớ trang 18 Vở bài tập KHTN 8:
|
Ghi nhớ: ………………………………………………………… ………………………………………………………… ………………………………………………………… ………………………………………………………… |
Lời giải:
- Phản ứng hoá học là quá trình biến đổi từ chất này thành chất khác.
- Trong phản ứng hoá học, chỉ có liên kết giữa các nguyên tử thay đổi làm cho phân tử này biến đổi thành phân tử khác, kết quả là chất này biến đổi thành chất khác.
- Một số dấu hiệu thường dùng để nhận biết phản ứng hoá học xảy ra: Có sự thay đổi màu sắc, mùi, … của các chất; tạo ra chất khí hoặc chất không tan (kết tủa); có sự toả nhiệt và phát sáng.
- Phản ứng toả ra năng lượng (dưới dạng nhiệt) được gọi là phản ứng toả nhiệt.
- Phản ứng thu vào năng lượng (dưới dạng nhiệt) được gọi là phản ứng thu nhiệt.
B. Câu hỏi và bài tập
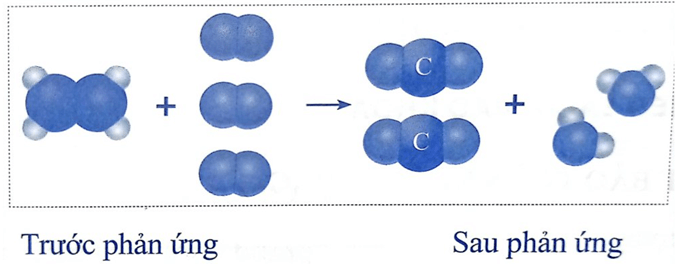
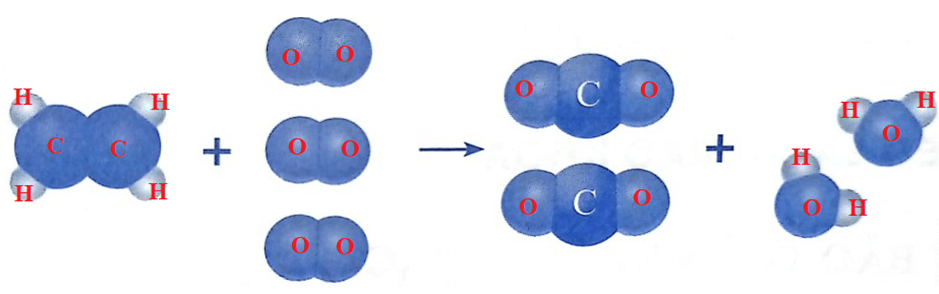
a) Xác định chất phản ứng và chất sản phẩm trong phản ứng hoá học trên.
b) Dự đoán dấu hiệu chứng tỏ có phản ứng hoá học xảy ra trong trường hợp trên.
c) Trước phản ứng, những nguyên tử nào liên kết với nhau? Sau phản ứng, những nguyên tử nào liên kết với nhau. Hãy so sánh số nguyên tử H và số nguyên tử O trước và sau phản ứng.
Lời giải:
a) Chất phản ứng: khí ethylene (C2H4) và khí oxygen (O2).
Chất sản phẩm: khí carbon dioxide (CO2) và hơi nước (H2O).
b) Dự đoán: Phản ứng toả nhiều nhiệt.
c) Liên kết giữa các nguyên tử trước và sau phản ứng:
Trước phản ứng: C liên kết với C; C liên kết với H; O liên kết với O.
Sau phản ứng: C liên kết với O; H liên kết với O.
So sánh: Số nguyên tử O và số nguyên tử H trước và sau phản ứng không thay đổi.
a) Ngọn nến cháy trong không khí.
b) Sắt bị ăn mòn trong không khí.
c) Đá vôi bị nung trong lò tạo thành vôi sống.
Lời giải:
- Phản ứng toả nhiệt: a, b.
- Phản ứng thu nhiệt: c.
Xem thêm lời giải Vở bài tập Khoa học tự nhiên 8 sách Cánh diều hay, chi tiết khác:
Bài 3: Định luật bảo toàn khối lượng. Phương trình hóa học
Bài 4: Mol và tỉ khối của chất khí
Xem thêm các chương trình khác:
- Soạn văn lớp 8 Cánh diều (hay nhất)
- Văn mẫu lớp 8 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 8 – Cánh diều
- Bố cục tác phẩm Ngữ văn lớp 8 – Cánh diều
- Tác giả tác phẩm Ngữ văn lớp 8 - Cánh diều
- Giải SBT Ngữ văn 8 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 8 – Cánh diều
- Soạn văn 8 Cánh diều (ngắn nhất)
- Giải sgk Toán 8 – Cánh diều
- Lý thuyết Toán 8 – Cánh diều
- Giải sbt Toán 8 – Cánh diều
- Giải sgk Tiếng Anh 8 – iLearn Smart World
- Giải sbt Tiếng Anh 8 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 8 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 8 ilearn Smart World
- Bài tập Tiếng Anh 8 iLearn Smart World theo Unit có đáp án
- Giải sgk Lịch sử 8 – Cánh diều
- Lý thuyết Lịch sử 8 - Cánh diều
- Giải sbt Lịch sử 8 – Cánh diều
- Giải sgk Địa lí 8 – Cánh diều
- Lý thuyết Địa lí 8 - Cánh diều
- Giải sbt Địa lí 8 – Cánh diều
- Giải sgk Giáo dục công dân 8 – Cánh diều
- Lý thuyết Giáo dục công dân 8 – Cánh diều
- Giải sbt Giáo dục công dân 8 – Cánh diều
- Giải sgk Công nghệ 8 – Cánh diều
- Lý thuyết Công nghệ 8 - Cánh diều
- Giải sbt Công nghệ 8 – Cánh diều
- Giải sgk Tin học 8 – Cánh diều
- Lý thuyết Tin học 8 - Cánh diều
- Giải sbt Tin học 8 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 8 – Cánh diều