Lý thuyết Nước (mới 2023 + Bài Tập) - Hóa học 8
Tóm tắt lý thuyết Hóa 8 Bài 36: Nước ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 8 Bài 36.
Lý thuyết Hóa 8 Bài 36: Nước
Bài giảng Hóa 8 Bài 36: Nước
I. Thành phần hóa học
1. Sự phân hủy nước
- Khi tiến hành điện phân nước bằng dòng điện một chiều, trên bề mặt hai điện cực sinh ra khí hiđro và oxi với tỉ lệ thể tích là 2:1.
- Phương trình hóa học:
2H2O 2H2↑ + O2↑
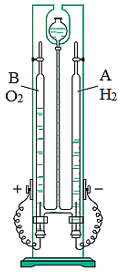
Hình 1: Phân hủy nước bằng dòng điện
2. Sự tổng hợp nước
Thí nghiệm: Cho nước vào đầy ống thủy tinh hình trụ. Cho vào ống lần lượt 2 thể tích khí hiđro và 2 thể tích khí oxi.
→ Mực nước trong ống ở vạch số 4.
Đốt bằng tia lửa điện hỗn hợp khí, ta thấy sau cùng hỗn hợp chỉ còn 1 thể tích oxi. Vậy 1 thể tích oxi đã hóa hợp với 2 thể tích hiđro tạo thành nước.
Phương trình hóa học:
2H2 + O2 2H2O
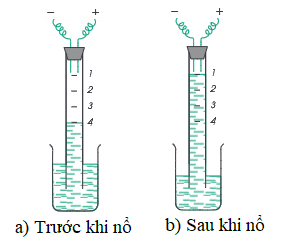
Hình 2: Tổng hợp nước
Kết luận:
- Nước là hợp chất tạo bởi 2 nguyên tố oxi và hiđro. Chúng đã hóa hợp với nhau
- Bằng thực nghiệm, người ta tìm được công thức hóa học của nước là H2O.
II. Tính chất của nước
1. Tính chất vật lý
- Nước là chất lỏng không màu (tuy nhiên lớp nước dày có màu xanh da trời), không mùi, không vị, sôi ở 100°C (p = 760 mmHg), hóa rắn ở 0°C thành nước đá và tuyết.
- Khối lượng riêng ở 4°C là 1 g/ml (hay 1kg/lít).
- Nước có thể hòa tan được nhiều chất rắn (muối ăn, đường,…), chất lỏng (cồn, axit,...), chất khí (HCl, NH3,…)
2. Tính chất hóa học
a) Tác dụng với kim loại: Nước có thể tác dụng với một số kim loại ở nhiệt độ thường như Na, Ca, Ba, K,…
Phương trình hóa học:
2Na + 2H2O → 2NaOH + H2↑
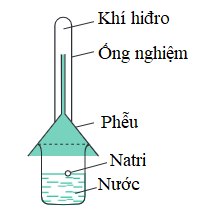
Hình 3: Phản ứng của nước với natri
b) Tác dụng với một số oxit bazơ như CaO, K2O,… tạo ra bazơ tương ứng Ca(OH)2, KOH,…
- Dung dịch bazơ làm quỳ tím chuyển xanh.
Phương trình hóa học:
K2O + H2O → 2KOH
c) Tác dụng với một số oxit axit như SO3, P2O5,… tạo thành axit tương ứng H2SO4, H3PO4,…
- Dung dịch axit làm quỳ tím chuyển đỏ.
Phương trình hóa học:
SO3 + H2O → H2SO4
III. Vai trò của nước và cách chống ô nhiễm nguồn nước:
- Vai trò của nước trong đời sống và sản xuất:
+ Hòa tan chất dinh dưỡng cho cơ thể sống

Hình 4: Dịch truyền tĩnh mạch glucose 5%
+ Tham gia vào quá trình hóa học trong cơ thể người và động vật.
+ Tham gia quá trình quang hợp của cây xanh
6CO2 + 6H2O C6H12O6 + 6O2↑
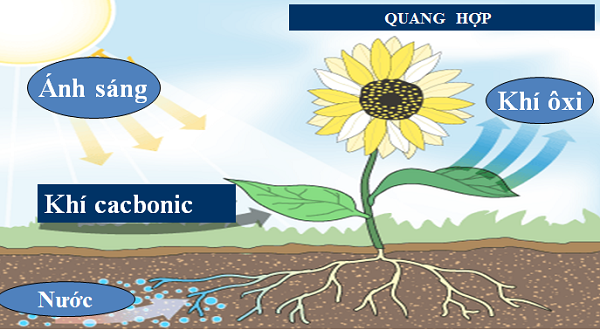
Hình 5: Mô hình quang hợp của cây xanh
+ Có vai trò rất quan trọng trong đời sống: sản xuất công nghiệp, nông nghiệp, giao thông vận tải,…

Hình 6: Một số ứng dụng của nước trong sản xuất, chăn nuôi
- Cách chống ô nhiễm nguồn nước:
+ Không vứt rác thải xuống nguồn nước.
+ Xử lý nước thải trước khi cho nước thải chảy vào sông, hồ, biển.
- Lượng nước ngọt là rất nhỏ so với lượng nước trên Trái Đất. Nhiều nguồn nước ngọt đang bị ô nhiễm nặng do đó cần phải sử dụng tiết kiệm nước.
Trắc nghiệm Hóa 8 Bài 36: Nước
Câu 1: Công thức hoá học của nước là
A. H2O2.
B. H2O.
C. H3O.
D. HO2.
Câu 2: Khi cho dòng điện một chiều đi qua nước, trên bề mặt 2 điện cực sẽ sinh ra
A. khí hiđro và khí oxi.
B. khí hiđro và khí cacbon oxit.
C. khí oxi và khí cacbon oxit.
D. khí hiđro và khí clo.
Câu 3: Tỉ lệ khối lượng của các nguyên tố hiđro và oxi trong H2O là
A. 1 : 3.
B. 5 : 6.
C. 1 : 8.
D. 2 : 7.
Câu 4: Phần trăm về khối lượng của nguyên tố H trong nước là
A. 88,9%.
B. 11,1%.
C. 16,2%.
D. 83,8%.
Câu 5: Phát biểu nào sau đây không đúng?
A. Nước là chất lỏng không màu (tuy nhiên lớp nước dày thì có màu xanh da trời).
B. Nước là chất lỏng không màu, không mùi, không vị.
C. Nước sôi ở nhiệt độ trên 100oC và hoá rắn ở 0oC thành nước đá và tuyết.
D. Nước có thể hoà tan được nhiều chất rắn (đường, muối ăn …), chất lỏng (cồn, axit …), chất khí (HCl, NH3 …).
Câu 6: Kim loại nào sau đây tác dụng được với nước ở nhiệt độ thường?
A. Mg.
B. Cu.
C. Fe.
D. Na.
Câu 7: Oxit nào sau đây tác dụng với nước tạo thành bazơ?
A. CaO.
B. SO3.
C. Al2O3.
D. CuO.
Câu 8: Nước hoá hợp với các oxit: CO2, SO3, P2O5, N2O5 tạo ra axit tương ứng là:
A. H2CO3, H2SO3, H3PO4, HNO2.
B. H2CO3, H2SO3, H3PO3, HNO2.
C. H2CO3, H2SO4, H3PO3, HNO3.
D. H2CO3, H2SO4, H3PO4, HNO3.
Câu 9: Dung dịch nào sau đây làm đổi màu quỳ tím thành đỏ?
A. NaOH.
B. K2SO4.
C. NaNO3.
D. HNO3.
Câu 10: Có ba chất gồm CuO, N2O5, Na2O đựng riêng biệt trong ba lọ bị mất nhãn. Để nhận biết các chất trên, ta dùng thuốc thử là
A. nước.
B. nước và quỳ tím.
C. dung dịch HCl.
D. dung dịch H2SO4.
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 8 đầy đủ, chi tiết khác:
Lý thuyết Bài 37: Axit – Bazơ – Muối
Lý thuyết Bài 38: Bài luyện tập 7
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 8 (hay nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Soạn văn 8 (ngắn nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Văn mẫu lớp 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Vật Lí 8
- Giải sbt Vật Lí 8
- Lý thuyết Vật Lí 8
- Giải vở bài tập Vật lí 8
- Giải SGK Toán 8 | Giải bài tập Toán 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Toán 8 (sách mới) | Sách bài tập Toán 8
- Bài tập Ôn luyện Toán lớp 8
- Các dạng bài tập Toán lớp 8
- Lý thuyết Toán lớp 8 (sách mới) | Kiến thức trọng tâm Toán 8
- Giáo án Toán lớp 8 mới nhất
- Bài tập Toán lớp 8 mới nhất
- Chuyên đề Toán lớp 8 mới nhất
- Giải sgk Tiếng Anh 8 (sách mới) | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2
- Giải sgk Tiếng Anh 8 | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 8 (sách mới) | Sách bài tập Tiếng Anh 8
- Giải sbt Tiếng Anh 8 (thí điểm)
- Giải sgk Tin học 8 | Giải bài tập Tin học 8 Học kì 1, Học kì 2 (sách mới)
- Giải sgk Lịch Sử 8 | Giải bài tập Lịch sử 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch sử 8 (sách mới) | Kiến thức trọng tâm Lịch sử 8
- Giải vở bài tập Lịch sử 8
- Giải Tập bản đồ Lịch sử 8
- Đề thi Lịch Sử 8
- Giải vở bài tập Sinh học 8
- Giải sgk Sinh học 8
- Lý thuyết Sinh học 8
- Giải sgk Giáo dục công dân 8 | Giải bài tập Giáo dục công dân 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Giáo dục công dân 8 (sách mới) | Kiến thức trọng tâm GDCD 8
- Lý thuyết Địa Lí 8 (sách mới) | Kiến thức trọng tâm Địa Lí 8
- Giải sgk Địa Lí 8 | Giải bài tập Địa Lí 8 Học kì 1, Học kì 2 (sách mới)
- Giải Tập bản đồ Địa Lí 8
- Đề thi Địa lí 8
