Lý thuyết Tính chất - Ứng dụng của hiđro (mới 2023 + Bài Tập) - Hóa học 8
Tóm tắt lý thuyết Hóa 8 Bài 31: Tính chất - Ứng dụng của hiđro ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 8 Bài 31.
Lý thuyết Hóa 8 Bài 31: Tính chất - Ứng dụng của hiđro
Bài giảng Hóa 8 Bài 31: Tính chất - Ứng dụng của hiđro
- Kí hiệu của nguyên tố hiđro là H. Nguyên tử khối bằng 1.
- Công thức hóa học của đơn chất hiđro là H2. Phân tử khối bằng 2.
I. Tính chất vật lý
Khí hiđro là chất khí không màu, không mùi, không vị, nhẹ nhất trong các khí, tan rất ít trong nước.
II. Tính chất hóa học
Ở nhiệt độ thích hợp, hiđro có thể kết hợp với đơn chất oxi, kết hợp với nguyên tố oxi trong một số oxit kim loại. Hiđro có tính khử. Các phản ứng này đều tỏa nhiệt.
1. Tác dụng với oxi
- Nếu đốt cháy hiđro trong oxi: hiđro cháy mạnh, trên thành lọ xuất hiện những giọt nước nhỏ.
- Phương trình hóa học:
2H2 + O2 2H2O
- Hỗn hợp sẽ gây nổ nếu trộn hiđro và oxi theo tỉ lệ thể tích 2:1.
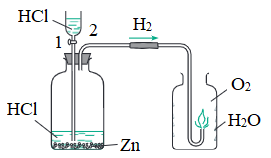
Hình 1: Khí hiđro cháy trong khí oxi
2. Tác dụng với đồng oxit (CuO)
- Khi đốt nóng CuO tới khoảng 400°C rồi cho luồng khí H2 đi qua: bột CuO màu đen chuyển thành lớp kim loại đồng màu đỏ gạch và có những giọt nước tạo thành trên thành cốc.
- Phương trình hóa học:
H2 + CuO (đen) Cu (đỏ) + H2O
⇒ Hiđro đã chiếm nguyên tố oxi trong CuO.
⇒ Vậy hiđro có tính khử.
III. Ứng dụng
- Do tính chất rất nhẹ, tính khử và khi cháy tỏa nhiềt nhiệt mà hiđro được ứng dụng trong đời sống:
+ Làm nguyên liệu cho động cơ tên lửa, nhiên liệu cho động cơ ô tô thay cho xăng, dùng trong đèn xi oxi – hiđro để hàn cắt kim loại.
+ Làm nguyên liệu trong sản xuất amoniac, axit và nhiều chất hữu cơ.
+ Dùng làm chất khử để điều chế kim loại từ oxit của chúng.
+ Bơm vào khinh khí cầu, bóng thám không vì là khí nhẹ nhất.
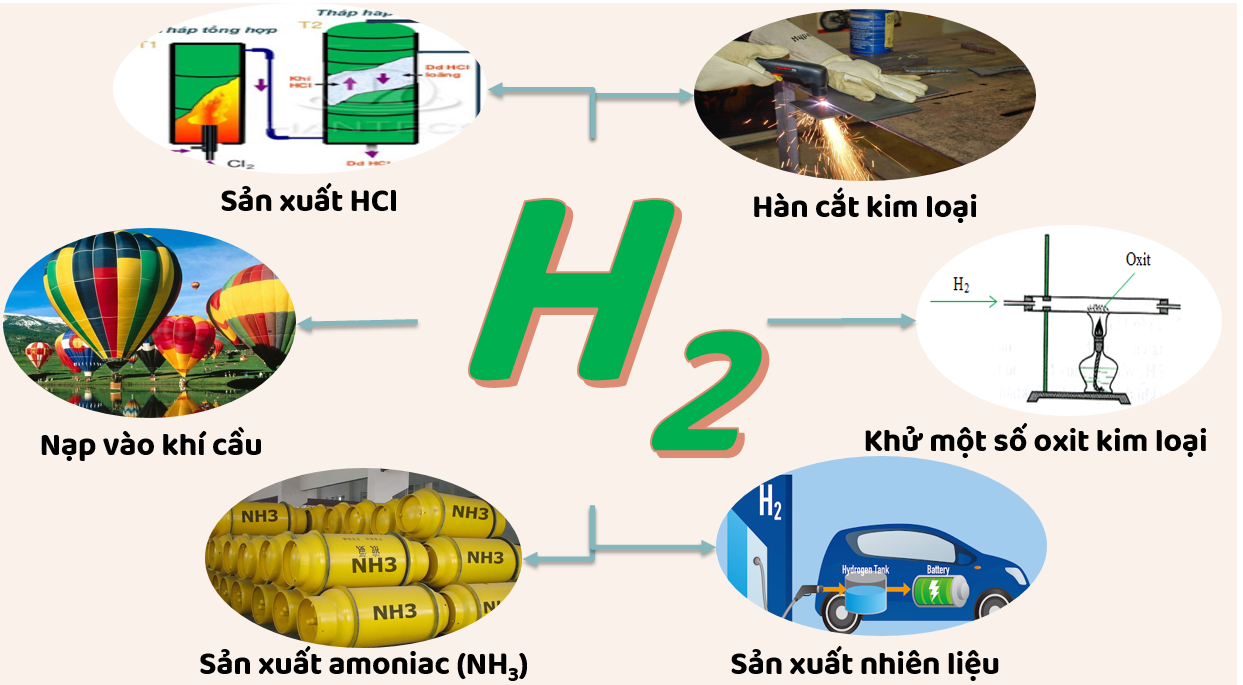
Hình 2: Một số ứng dụng của khí H2
Trắc nghiệm Hóa 8 Bài 31: Tính chất - ứng dụng của hiđro
Câu 1: Công thức hóa học của đơn chất hiđro là
A. 2H.
B. H2.
C. H.
D. O2.
Câu 2: Phát biểu nào sau đây không đúng?
A. Khí hiđro là chất khí không màu, không mùi, không vị.
B. Khí hiđro nhẹ nhất trong các chất khí.
C. Khí hiđro tan nhiều trong nước.
D. Khí hiđro nhẹ hơn không khí.
Câu 3: Một quả bóng bay đã được bơm khí hiđro, miệng quả bóng được buộc chặt bằng sợi dây chỉ dài. Khi không giữ dây chỉ thì quả bóng bay sẽ di chuyển như thế nào?
A. Di chuyển lên cao.
B. Di chuyển xuống dưới và chạm vào mặt đất.
C. Không di chuyển.
D. Di chuyển sang ngang.
Câu 4: Đưa ngọn lửa của khí H2 đang cháy vào trong lọ đựng khí oxi thì
A. ngọn lửa tắt dần.
B. ngọn lửa cháy mạnh hơn.
C. ngọn lửa tắt dần rồi bùng cháy trở lại.
D. ngọn lửa chuyển màu và tắt dần.
Câu 5: Hỗn hợp khí hiđro và khí oxi là hỗn hợp nổ. Hỗn hợp sẽ gây nổ mạnh nhất nếu trộn khí H2 và khí O2 theo tỉ lệ về thể tích là
A. 1 : 2.
B. 1 : 3.
C. 3 : 1.
D. 2 : 1.
Câu 6: Đốt nóng CuO tới khoảng 400oC rồi cho luồng khí H2 đi qua. Trong phản ứng trên, hiđro thể hiện
A. tính khử.
B. tính oxi hóa.
C. tính khử và tính oxi hóa.
D. không có tính khử và không có tính oxi hóa.
Câu 7: Cho hai thí nghiệm sau:
Thí nghiệm 1: Cho một luồng khí H2 (sau khi đã kiểm tra sự tinh khiết) đi qua bột đồng(II) oxit CuO có màu đen ở nhiệt độ thường.
Thí nghiệm 2: Đốt nóng CuO tới khoảng 400oC rồi cho luồng khí H2 đi qua.
Phát biểu nào sau đây không đúng?
A. Thí nghiệm 1: Không có phản ứng hóa học xảy ra.
B. Thí nghiệm 2: Bột CuO màu đen chuyển dần thành màu đỏ gạch.
C. Không có hiện tượng gì ở cả hai thí nghiệm.
D. Thí nghiệm 2: Có những giọt nước tạo thành.
Câu 8: Ứng dụng nào sau đây không phải của khí hiđro?
A. Dùng làm nhiên liệu cho động cơ tên lửa.
B. Dùng để bơm vào khinh khí cầu, bóng thám không.
C. Dùng trong đèn xì oxi-hiđro để hàn cắt kim loại.
D. Dùng để dập tắt đám cháy.
Câu 9: Phương trình hóa học của phản ứng hiđro khử sắt(III) oxit là
A. FeO + H2 Fe + H2O.
B. Fe2O3 + 3H2 2Fe + 3H2O.
C. Fe3O4 + 4H2 3Fe + 4H2O.
D. 2Fe + 3H2O Fe2O3 + 3H2.
Câu 10: Phát biểu không đúng là:
A. Hiđro là chất khí nhẹ nhất trong các chất khí.
B. Khí hiđro có tính khử, có thể kết hợp với nguyên tố oxi trong một số oxit kim loại.
C. Hiđro có nhiều ứng dụng, chủ yếu do tính chất rất nhẹ, do tính khử và khi cháy tỏa nhiều nhiệt.
D. Hiđro có thể tác dụng với tất cả oxit kim loại ở nhiệt độ cao.
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 8 đầy đủ, chi tiết khác:
Lý thuyết Bài 32: Phản ứng oxi hóa – khử
Lý thuyết Bài 33: Điều chế khí hiđro – Phản ứng thế
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 8 (hay nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Soạn văn 8 (ngắn nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Văn mẫu lớp 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Vật Lí 8
- Giải sbt Vật Lí 8
- Lý thuyết Vật Lí 8
- Giải vở bài tập Vật lí 8
- Giải SGK Toán 8 | Giải bài tập Toán 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Toán 8 (sách mới) | Sách bài tập Toán 8
- Bài tập Ôn luyện Toán lớp 8
- Các dạng bài tập Toán lớp 8
- Lý thuyết Toán lớp 8 (sách mới) | Kiến thức trọng tâm Toán 8
- Giáo án Toán lớp 8 mới nhất
- Bài tập Toán lớp 8 mới nhất
- Chuyên đề Toán lớp 8 mới nhất
- Giải sgk Tiếng Anh 8 (sách mới) | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2
- Giải sgk Tiếng Anh 8 | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 8 (sách mới) | Sách bài tập Tiếng Anh 8
- Giải sbt Tiếng Anh 8 (thí điểm)
- Giải sgk Tin học 8 | Giải bài tập Tin học 8 Học kì 1, Học kì 2 (sách mới)
- Giải sgk Lịch Sử 8 | Giải bài tập Lịch sử 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch sử 8 (sách mới) | Kiến thức trọng tâm Lịch sử 8
- Giải vở bài tập Lịch sử 8
- Giải Tập bản đồ Lịch sử 8
- Đề thi Lịch Sử 8
- Giải vở bài tập Sinh học 8
- Giải sgk Sinh học 8
- Lý thuyết Sinh học 8
- Giải sgk Giáo dục công dân 8 | Giải bài tập Giáo dục công dân 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Giáo dục công dân 8 (sách mới) | Kiến thức trọng tâm GDCD 8
- Lý thuyết Địa Lí 8 (sách mới) | Kiến thức trọng tâm Địa Lí 8
- Giải sgk Địa Lí 8 | Giải bài tập Địa Lí 8 Học kì 1, Học kì 2 (sách mới)
- Giải Tập bản đồ Địa Lí 8
- Đề thi Địa lí 8
