Lý thuyết Tính chất của oxi (mới 2023 + Bài Tập) - Hóa học 8
Tóm tắt lý thuyết Hóa 8 Bài 24: Tính chất của oxi ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 8 Bài 24.
Lý thuyết Hóa 8 Bài 24: Tính chất của oxi
Bài giảng Hóa 8 Bài 24: Tính chất của oxi
- Kí hiệu hóa học của nguyên tố oxi: O
- Công thức hóa học của đơn chất (khí) oxi: O2
- Nguyên tử khối: 16. Phân tử khối: 32
- Oxi là nguyên tố hóa học phổ biến nhất (chiếm 49,4% khối lượng vỏ Trái Đất).
+ Ở dạng đơn chất khí oxi có nhiều trong không khí.
+ Ở dạng hợp chất, nguyên tố oxi có trong nước, đường, quặng, đất đá, cơ thể người, động vật, thực vật …
I. Tính chất vật lí
- Khí oxi là chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
- Oxi hóa lỏng ở -183°C.
- Oxi lỏng có màu xanh nhạt.
II. Tính chất hóa học
Oxi có thể tác dụng với kim loại, phi kim và các hợp chất ở nhiệt độ cao. Trong các hợp chất hóa học oxi hóa trị II.
1. Tác dụng với phi kim
a) Với lưu huỳnh
- Lưu huỳnh cháy trong không khí với ngọn lửa nhỏ, màu xanh nhạt; cháy trong khí oxi mãnh liệt hơn, tạo thành khí lưu huỳnh đioxit SO2 (còn gọi là khí sunfurơ) và rất ít lưu huỳnh trioxit SO3.
- Phương trình hóa học:
S (r) + O2 (k) SO2 (k)

Hình 1: Lưu huỳnh cháy trong khí oxi
b) Với photpho
- Photpho cháy mạnh trong oxi với ngọn lửa sáng chói, tạo khói trắng dày đặc bám vào thành lọ dưới dạng bột tan được trong nước. Bột trắng đó là điphotpho pentaoxit có công thức hóa học là P2O5.
- Phương trình hóa học:
4P (r) + 5O2 (k) 2P2O5 (r)

Hình 2: Photpho cháy trong khí oxi
2. Tác dụng với kim loại
- Cho dây sắt cuốn một mẩu than hồng vào lọ khí oxi, mẩu than cháy trước tạo nhiệt độ đủ cao cho sắt cháy. Sắt cháy mạnh, sáng chói, không có ngọn lửa, không có khói, tạo ra các hạt nhỏ nóng chảy màu nâu là sắt(II, III) oxit, công thức hóa học là Fe3O4, thường được gọi là oxit sắt từ.
- Phương trình hóa học:
3Fe + 2O2 Fe3O4
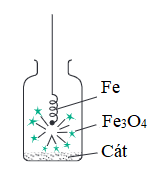
Hình 3: Sắt cháy trong khí oxi
3. Tác dụng với hợp chất
Khí metan (có trong khí bùn ao, bioga) cháy trong không khí do tác dụng với oxi, tỏa nhiều nhiệt.
Phương trình hóa học:
CH4 + 2O2 CO2 + 2H2O
Trắc nghiệm Hóa 8 Bài 24: Tính chất Oxi
Câu 1: Công thức hóa học của đơn chất (khí) oxi là
A. O3.
B. O2.
C. O.
D. 2O.
Câu 2: Trong các hợp chất hóa học, nguyên tố oxi có hóa trị
A. I.
B. II.
C. III.
D. IV.
Câu 3: Phát biểu nào sau đây không đúng?
A. Khí oxi là chất khí không màu, không mùi, ít tan trong nước.
B. Khí oxi nhẹ hơn không khí.
C. Oxi hóa lỏng ở − 183oC.
D. Oxi lỏng có màu xanh nhạt.
Câu 4: Khí oxi không tác dụng được với chất nào sau đây?
A. Fe.
B. S.
C. P.
D. Ag.
Câu 5: Khí metan (có trong khí bùn ao, khí biogas) cháy trong không khí do tác dụng với khí oxi, tỏa nhiều nhiệt. Phương trình hóa học biểu diễn sự cháy của metan là:
A. CH4 + O2 C + 2H2O.
B. CH4 + O2 CO2 + H2O.
C. CH4 + 2O2 CO2 + 2H2O.
D. CH4 + O2 CO2 + 2H2.
Câu 6: Cho các phát biểu sau:
(1) Khí oxi là một đơn chất phi kim hoạt động rất kém.
(2) Ở nhiệt độ cao, khí oxi dễ dàng tham gia phản ứng hóa học với nhiều phi kim, nhiều kim loại và hợp chất.
(3) Sắt cháy trong khí oxi thu được oxit sắt từ.
(4) Oxi là nguyên tố hóa học phổ biến nhất (chiếm 49,4% khối lượng vỏ Trái Đất).
(5) Ở dạng đơn chất, khí oxi có nhiều trong không khí.
Trong các phát biểu trên, số phát biểu đúng là
A. 3.
B. 2.
C. 5.
D. 4.
Câu 7: Vì sao cá sống được trong nước?
A. Vì trong nước có hòa tan khí nitơ.
B. Vì trong nước có hòa tan khí cacbon đioxit.
C. Vì trong nước có hòa tan khí hiđro.
D. Vì trong nước có hòa tan khí oxi.
Câu 8: Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 4 mol lưu huỳnh?
A. 128 gam.
B. 160 gam.
C. 144 gam.
D. 176 gam.
Câu 9: Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 3,2 gam metan là
A. 4,48 lít.
B. 5,60 lít.
C. 8,96 lít.
D. 2,24 lít
Câu 10: Biết oxi chiếm 20% thể tích không khí. Thể tích không khí (đktc) cần thiết để đốt cháy 1 mol cacbon là
A. 112,0 lít.
B. 224,0 lít.
C. 11,2 lít.
D. 22,4 lít.
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 8 đầy đủ, chi tiết khác:
Lý thuyết Bài 25: Sự oxi hóa – Phản ứng hóa hợp - Ứng dụng của oxi
Lý thuyết Bài 27: Điều chế khí oxi – Phản ứng phân hủy
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 8 (hay nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Soạn văn 8 (ngắn nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Văn mẫu lớp 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Vật Lí 8
- Giải sbt Vật Lí 8
- Lý thuyết Vật Lí 8
- Giải vở bài tập Vật lí 8
- Giải SGK Toán 8 | Giải bài tập Toán 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Toán 8 (sách mới) | Sách bài tập Toán 8
- Bài tập Ôn luyện Toán lớp 8
- Các dạng bài tập Toán lớp 8
- Lý thuyết Toán lớp 8 (sách mới) | Kiến thức trọng tâm Toán 8
- Giáo án Toán lớp 8 mới nhất
- Bài tập Toán lớp 8 mới nhất
- Chuyên đề Toán lớp 8 mới nhất
- Giải sgk Tiếng Anh 8 (sách mới) | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2
- Giải sgk Tiếng Anh 8 | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 8 (sách mới) | Sách bài tập Tiếng Anh 8
- Giải sbt Tiếng Anh 8 (thí điểm)
- Giải sgk Tin học 8 | Giải bài tập Tin học 8 Học kì 1, Học kì 2 (sách mới)
- Giải sgk Lịch Sử 8 | Giải bài tập Lịch sử 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch sử 8 (sách mới) | Kiến thức trọng tâm Lịch sử 8
- Giải vở bài tập Lịch sử 8
- Giải Tập bản đồ Lịch sử 8
- Đề thi Lịch Sử 8
- Giải vở bài tập Sinh học 8
- Giải sgk Sinh học 8
- Lý thuyết Sinh học 8
- Giải sgk Giáo dục công dân 8 | Giải bài tập Giáo dục công dân 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Giáo dục công dân 8 (sách mới) | Kiến thức trọng tâm GDCD 8
- Lý thuyết Địa Lí 8 (sách mới) | Kiến thức trọng tâm Địa Lí 8
- Giải sgk Địa Lí 8 | Giải bài tập Địa Lí 8 Học kì 1, Học kì 2 (sách mới)
- Giải Tập bản đồ Địa Lí 8
- Đề thi Địa lí 8
