Lý thuyết Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng (mới 2023 + Bài Tập) - Hóa học 11
Tóm tắt lý thuyết Hóa 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 11 Bài 13.
Lý thuyết Hóa 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng
Bài giảng Hóa 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng
Kiến thức trọng tâm
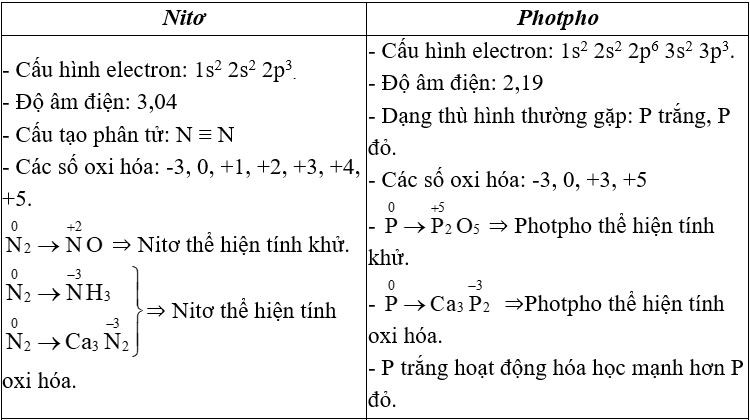
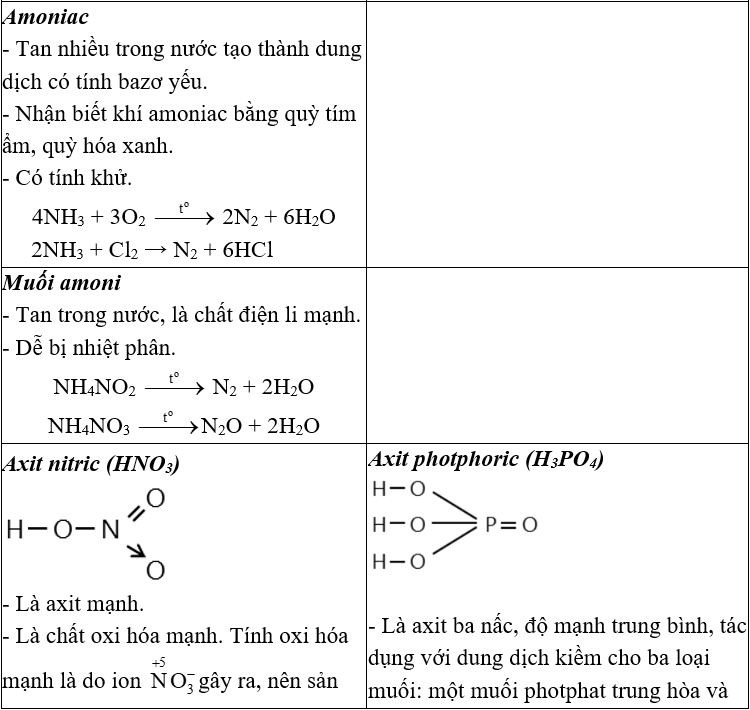
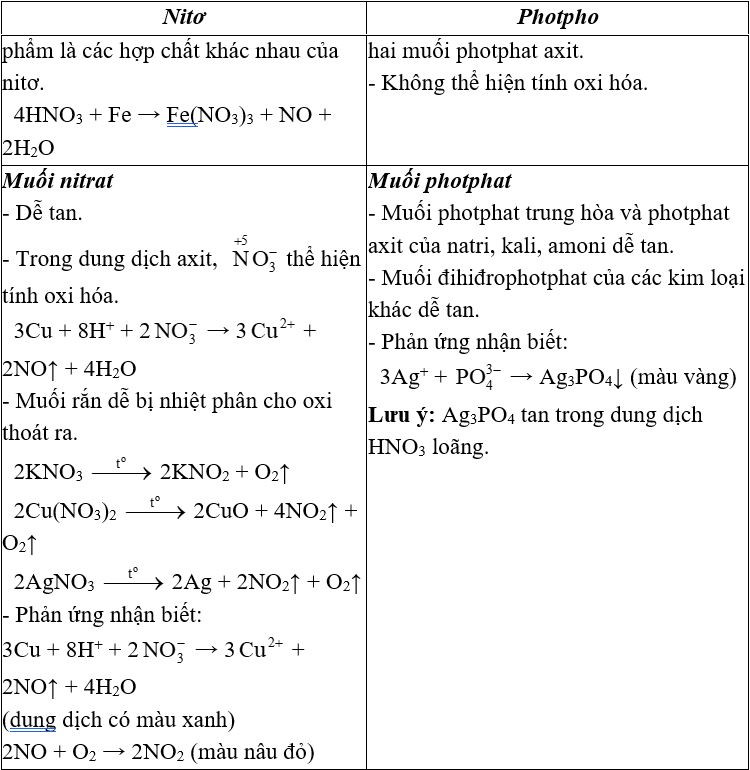
Trắc nghiệm Hóa 11 Bài 13: Luyện tập: Tính chất hóa học của nitơ, photpho và hợp chất của chúng
Câu 1: Nitơ có những đặc điểm về tính chất như sau:
(a) Nguyên tử nitơ có 5 electron ở lớp ngoài cùng nên chỉ có khả năng tạo hợp chất cộng hóa trị trong đó nitơ có số oxi hóa +5 và –3.
(b) Khí nitơ tương đối trơ ở nhiệt độ thường
(c) Nitơ là phi kim tương đối hoạt động ở nhiệt độ cao.
(d) Nitơ thể hiện tính oxi hóa khi tác dụng với kim loại mạnh và hiđro.
(e) Nitơ thể hiện tính khử khi tác dụng với nguyên tố có độ âm điện lớn hơn.
Nhóm nào sau đây chỉ gồm các câu đúng?
A. a, b, d, e.
B. a, c, d.
C. a, b, c.
D. b, c, d, e.
Đáp án: D
Giải thích:
a sai vì ngoài mức số oxi hóa +5, +3 thì nitơ còn có các mức oxi hóa khác như +2 (trong NO…), +1 (trong N2O…), +4 (trong NO2…), -3 (trong NH3…).
b, c, d, e đúng.
Câu 2: Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 3,913. Hiệu suất của phản ứng tổng hợp NH3 là ?
A. 25%.
B. 15%.
C. 30%.
D. 20%.
Đáp án: D
Giải thích:
N2 + 3H2
Giả sử: nX = 1 mol → nY = 0,92 mol
Hiệu suất tính theo N2
Và
Đặt:
→ 0,92 = (0,2 a) + (0,83a) + 2a
→ a = 0,04 mol
Câu 3: Trong các phát biểu sau:
(1) Trong NH3 và , nitơ đều có số oxi hóa –3.
(2) Trong NH3 và , nitơ đều có cộng hóa trị 3.
(3) Công thức của phân supephotphat kép là Ca(H2PO4)2.
(4) Để tạo độ xốp trong một số loại bánh có thể dùng muối NH4NO2.
(5) Kim cương là tinh thể phân tử.
(6) Độ dinh dưỡng của phân kali được đánh giá bằng hàm lượng % của K.
Số phát biểu không đúng là
A. 2.
B. 4
C. 3
D. 1.
Đáp án: B
Giải thích:
Những phát biểu sai là:
(2) sửa: NH3 có cộng hóa trị 3 còn có cộng hóa trị là 4.
(4) sửa: Để tạo độ xốp trong một số loại bánh có thể dùng muối NH4HCO3.
(5) sửa: Kim cương là tinh thể nguyên tử.
(6) sửa: Độ dinh dưỡng của phân kali được đánh giá bằng hàm lượng % của K2O.
Câu 4: Hòa tan hoàn toàn 24,48 gam Al2O3 bằng một lượng vừa đủ dung dịch HNO3, thu được 228 gam dung dịch X. Làm lạnh X đến 20 thì có m gam tinh thể Al(NO3)3.9H2O tách ra. Biết ở 20, cứ 100 gam H2O hòa tan được tối đa 75,44 gam Al(NO3)3. Giá trị của m gần nhất với giá trị nào sau đây?
A. 30.
B. 13.
C. 66.
D. 17.
Đáp án: A
Giải thích:
→ 228 gam dung dịch X
Đặt ntinh thể = a mol
→ Sau kết tinh, dung dịch chứa
Câu 5: Cho hỗn hợp X gồm a mol Fe và 0,2 mol Mg vào dung dịch Y chứa Cu(NO3)2 và AgNO3 ( tỉ lệ mol tương ứng 2:3). Sau khi các phản ứng kết thúc, thu được dung dịch Z và 50,8 gam chất rắn T gồm ba kim loại. Hòa tan toàn bộ T trong lượng dư dung dịch H2SO4 đặc nóng, thu được 0,5 mol SO2 (sản phẩm khử duy nhất của H2SO4). Gái trị của a là
A. 0,15.
B. 0,20.
C. 0,25.
D. 0,30.
Đáp án: C
Giải thích:
50,8 gam chất rắn T gồm
→ Dung dịch chỉ chứa muối Fe(NO3)2 và Mg(NO3)2.
Bảo toàn khối lượng:
56x + 64.2y + 108.3y = 50,8 (1)
Bảo toàn electron:
3x + 2.2y + 1.3y = 0,5.2 (2)
Từ (1) và (2) → x = y = 0,1 mol
Bảo toàn electron khi X tác dụng với Y:
Câu 6: Phát biểu nào sau đây là đúng ?
A. Photpho trắng có cấu trúc mạng tinh thể nguyên tử, photpho đỏ có cấu trúc polime.
B. Nitrophotka là hỗn hợp của NH4H2PO4 và KNO3.
C. Thủy tinh lỏng là dung dịch đậm đặc của Na2SiO3 và K2SiO3.
D. Cacbonmonoxit và silic đioxit là oxit axit.
Đáp án: C
Giải thích:
A. sai vì photpho trắng có cấu trúc mạng tinh thể phân tử.
B. sai vì nitrophotka là hỗn hợp của (NH4)2HPO4 và KNO3.
C. đúng
D. sai vì CO là oxit trung tính.
Câu 7: Cho các phát biểu sau:
(1) Ở điều kiện thường, nitơ là chất khí không màu, không mùi, không vị, nặng hơn không khí 1,1 lần.
(2) Nitơ lỏng dùng được để bảo quản máu và các mẫu vật sinh học.
(3) Amoniac là chất khí không màu, có mùi khai và xốc, nhẹ hơn không khí.
(4) Để làm khô khí, người ta cho khí amoniac có lẫn hơi nước đi qua bình đựng dung dịch axit sunfuric đặc.
Số phát biểu đúng là
A. 2.
B. 3.
C. 1.
D. 4.
Đáp án: A
Giải thích:
Phát biểu đúng gồm (2) và (3).
(1) sai vì N2 nhẹ hơn không khí.
(4) sai vì NH3 sẽ tác dụng với dung dịch axit.
Câu 8: Cho 21,30 gam P2O5 vào 440 gam dung dịch NaOH 10% thu được dung dịch X. Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là
A. 50,60 gam.
B. 57,20 gam
C. 52,70 gam.
D. 60,05 gam.
Đáp án: B
Giải thích:
Ta có:
→Chất rắn khan gồm Na3PO4 và NaOH.
Bảo toàn khối lượng ta có:
+ mNaOH = mRắn +
→ mRắn = 0,3.98 + 44 – 0,9.18 = 57,2 gam
Câu 9: Phát biểu nào sau đây là đúng?
A. Dung dịch hỗn hợp HCl và KNO3 không hòa tan được bột đồng.
B. Photpho trắng dễ bốc cháy trong không khí ở điều kiện thường.
C. Thổi không khí qua than nung đỏ, thu được khí than ướt.
D. Hỗn hợp FeS và CuS tan được hết trong dung dịch HCl dư.
Đáp án: B
Giải thích:
A sai vì có tính oxi hóa như axit HNO3 loãng → dung dịch chứa hỗn hợp HCl và KNO3 hòa tan được đồng.
B đúng vì P trắng cháy ở nhiệt độ > 40
C sai vì cho hơi nước qua than nung đỏ sẽ thu được khí than ướt.
D sai vì CuS không phản ứng với dung dịch HCl.
Câu 10: Cho dãy các chất; FeO, Fe3O4, Al2O3, Cu(OH)2, Fe2O3. Số chất trong dãy bị oxi hóa bởi dung dịch HNO3 đặc, nóng là:
A. 4
B. 2.
C. 3
D. 5.
Đáp án: B
Giải thích:
Chất bị oxi hóa bởi dung dịch HNO3 đặc, nóng → chất đó là chất khử.
Các chất thỏa mãn là: FeO, Fe3O4.
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 11 đầy đủ, chi tiết khác:
Lý thuyết Bài 16: Hợp chất của cacbon
Lý thuyết Bài 17: Silic và hợp chất của silic
Lý thuyết Bài 18: Công nghiệp silicat
Lý thuyết Bài 19: Luyện tập: Tính chất của cacbon, silic và hợp chất của chúng
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
