Lý thuyết Luyện tập: Dẫn xuất halogen, ancol và phenol (mới 2023 + Bài Tập) - Hóa học 11
Tóm tắt lý thuyết Hóa 11 Bài 42: Luyện tập: Dẫn xuất halogen, ancol và phenolngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 11 Bài 42.
Lý thuyết Hóa 11 Bài 42: Luyện tập: Dẫn xuất halogen, ancol và phenol
Bài giảng Hóa 11 Bài 42: Luyện tập: Dẫn xuất halogen, ancol và phenol
Kiến thức cần nắm vững về tính chất hóa học của dẫn xuất halogen, ancol, phenol:
1. Dẫn xuất halogen
a. Phản ứng thế nguyên tử halogen bằng nhóm –OH
Ví dụ:
CH3CH2Br + NaOH (loãng) CH3CH2OH + NaBr
Phương trình hóa học chung:
R – X + NaOH R -OH + NaX
b. Phản ứng tách hiđro halogenua
Ví dụ:
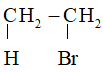 + KOH CH2 = CH2 + KBr + H2O
+ KOH CH2 = CH2 + KBr + H2O
Phản ứng tách hiđro halogenua tuân theo quy tắc tách Zai – xép: Khi tách HX khỏi dẫn xuất halogen, nguyên tử halogen X ưu tiên tách ra cùng nguyên tử H ở cacbon bậc cao hơn bên cạnh tạo sản phẩm chính.
2. Ancol no, đơn chức
a. Phản ứng thế H của nhóm OH ancol (phản ứng đặc trưng của ancol)
- Tính chất chung của ancol tác dụng với kim loại kiềm:
+ Với ancol đơn chức:
2ROH + 2Na → 2RONa + H2↑
+ Với ancol đa chức:
2R(OH)x + 2xNa → 2R(ONa)x + xH2↑
- Tính chất đặc trưng của glixerol hòa tan Cu(OH)2
Ví dụ:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Không chỉ glixerol, các ancol đa chức có các nhóm – OH liền kề cũng có tính chất này.
b. Phản ứng thế nhóm OH
- Phản ứng với axit vô cơ:
Ví dụ:
C2H5OH + HBr C2H5Br + H2O
Các ancol khác cũng có phản ứng tương tự, phản ứng này chứng tỏ phân tử ancol có nhóm – OH.
- Phản ứng với ancol
Ví dụ:
2C2H5OH C2H5OC2H5 + H2O
⇒ Công thức tính số ete tạo thành từ n ancol khác nhau là
c. Phản ứng tách nước (phản ứng đehidrat hoá)
Tổng quát:
CnH2n + 1OH CnH2n + H2O
d. Phản ứng oxi hoá
- Phản ứng oxi hoá hoàn toàn:
CnH2n + 2O + O2 nCO2 + (n + 1)H2O
- Phản ứng oxi hoá không hoàn toàn bởi CuO, to
+ Các ancol bậc I bị oxi hóa không hoàn toàn tạo thành anđehit. Ví dụ:
CH3CH2OH + CuO CH3CHO (anđehit axetic) + Cu + H2O
+ Các ancol bậc II bị oxi hóa không hoàn toàn tạo thành xeton. Ví dụ:
CH3- CH(OH) – CH3 + CuO CH3 – CO – CH3 + Cu + H2O
+ Trong điều kiện trên, ancol bậc III không phản ứng.
3. Phenol
a. Phản ứng thế nguyên tử hiđro của nhóm OH
- Tác dụng với kim loại kiềm:
2C6H5OH + 2Na → 2C6H5ONa (Natri phenolat) + H2↑
- Tác dụng với bazơ:
C6H5OH + NaOH → C6H5ONa + H2O
b. Phản ứng thế nguyên tử hiđro của vòng benzen
- Phản ứng với dung dịch brom:
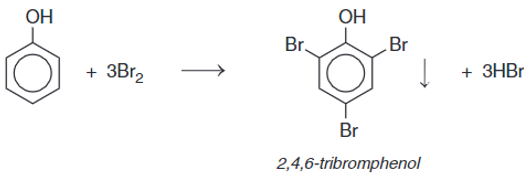
- Phản ứng với dung dịch HNO3
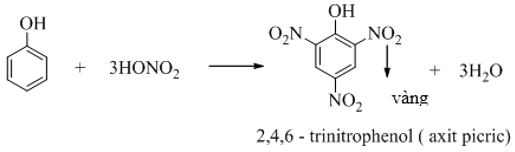
Trắc nghiệm Hóa học lớp 11 Bài 42: Luyện tập: Dẫn xuất halogen, ancol và phenol
Bài 1: Khẳng định nào dưới đây không đúng?
A. Hầu hết các ancol đều nhẹ hơn nước
B. Ancol tan tốt trong nước do có nhóm OH tạo liên kết hiđro với phân tử nước
C. Nhiệt độ sôi của ancol cao hơn nhiệt độ sôi của ete, anđehit
D. Phenol tan tốt trong nước do cũng có nhóm OH trong phân tử.
Đáp án: D
Giải thích: Theo tính chất vật lý thì: Phenol ít tan trong nước
Bài 2: Ancol no, đơn chức có 10 nguyên tử H trong phân tử có số đồng phân là
A. 5.
B. 3.
C. 4.
D. 2.
Đáp án: C
Giải thích:
C4H10O có 4 đồng phân ancol là: CH3(CH2)2CH2OH ; CH3CHOHCH2CH3 ; (CH3)2CHCH2OH ; (CH3)3C-OH
Bài 3: Tên quốc tế của hợp chất có công thức CH3CH(C2H5)CH(OH)CH3 là
A. 4-etylpentan-2-ol.
B. 2-etylbutan-3-ol.
C. 3-etylhexan-5-ol.
D. 3-metylpentan-2-ol.
Đáp án: D
Giải thích:
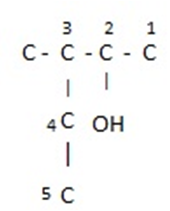
3 - metylpentan - 2 - ol
(Chú ý chọn mạch C dài nhất, có chứa nhóm -OH làm mạch chính)
Bài 4: Khi đun nóng dẫn xuất halogen X với dung dịch NaOH tạo thành hợp chất anđehit axetic. Tên của hợp chất X là
A. 1,2- đibrometan.
B. 1,1- đibrometan.
C. etyl clorua.
D. A và B đúng.
Đáp án: B
Giải thích:
CH3CHBr2 CH3CH(OH)2 CH3CHO
(1,1 - đibrometan)
Bài 5: X là dẫn xuất clo của etan. Đun nóng X trong NaOH dư thu được chất hữu cơ Y vừa tác dụng với Na vừa tác dụng với Cu(OH)2 ở nhiệt độ thường. Vậy X là
A. 1,1,2,2-tetracloetan.
B. 1,2-đicloetan.
C. 1,1-đicloetan.
D. 1,1,1-tricloetan.
Đáp án: B
Giải thích:
Ta thấy:
CH2Cl - CH2Cl CH2OH - CH2OH CH2ONa - CH2ONa
CH2Cl - CH2Cl CH2OH - CH2OH phức
Bài 6: Công thức nào dưới đây là công thức của ancol no, mạch hở chính xác nhất ?
A. R(OH)n.
B. CnH2n + 2O.
C. CnH2nOx.
D. CnH2n + 2 – x (OH)x.
Đáp án: D
Giải thích:
Thay thế x nguyên tử H của ankan CnH2n+2 bởi nhóm OH
=> Ancol là CnH2n+2-x(OH)x
Loại B vì đề bài không nói là ancol đơn chức.
Bài 7: Đun nóng một ancol X với H2SO4 đặc ở nhiệt độ thích hợp thu được một olefin duy nhất. Công thức tổng quát của X là (với n > 0, n nguyên)
A. CnH2n + 1OH.
B. ROH.
C. CnH2n + 2O.
D. CnH2n + 1CH2OH.
Đáp án: D
Giải thích:
Tách nước ancol tạo olein duy nhất thì ancol là bậc I, đơn chức.
Vậy ancol có dạng CnH2n+1CH2OH
Bài 8: Một ancol no có công thức thực nghiệm là (C2H5O)n. CTPT của ancol có thể là
A. C2H5O.
B. C4H10O2.
C. C4H10O.
D. C6H15O3.
Đáp án: B
Giải thích:
Ancol có dạng C2nH5nOn , mà ta có 2n.2 + 2 ≥ 5n
(với CxHy thì y ≤ 2x + 2)
→ n ≤ 2
Vậy n = 2 thỏa mãn. Ancol là C4H10O2.
Bài 9: Một ancol no đơn chức có %H = 13,04% về khối lượng. Công thức của ancol là
A. C6H5CH2OH.
B. CH3OH.
C. C2H5OH.
D. CH2=CHCH2OH.
Đáp án: C
Giải thích:
Ancol no, đơn chức : CnH2n+2O
→ n = 2. Ancol là C2H6O hay CTCT C2H5OH.
Câu 10: Một ancol no đơn chức có %O = 50% về khối lượng. Công thức của ancol là
A. C3H7OH.
B. CH3OH.
C. C6H5CH2OH.
D. CH2=CHCH2OH.
Đáp án: B
Giải thích:
Ancol no, đơn chức có chứa 1 oxi
32.
Vậy ancol là CH3OH.
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 11 đầy đủ, chi tiết khác:
Lý thuyết Bài 44: Anđehit – Xeton
Lý thuyết Bài 45: Axit cacboxylic
Lý thuyết Bài 46: Luyện tập: Anđehit – Xeton – Axit cacboxylic
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
