Lý thuyết Axit cacboxylic (mới 2023 + Bài Tập) Axit cacboxylic
Tóm tắt lý thuyết Hóa 11 Bài 45: Axit cacboxylic ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 11 Bài 45.
Lý thuyết Hóa 11 Bài 45: Axit cacboxylic
Bài giảng Hóa 11 Bài 45: Axit cacboxylic
I. Định nghĩa, phân loại, danh pháp
1. Định nghĩa
- Axit cacboxylic là những hợp chất hữu cơ mà phân tử có nhóm cacboxyl (-COOH) liên kết trực tiếp với nguyên tử cacbon hoặc nguyên tử hiđro.
- Ví dụ: H-COOH, C2H5COOH, HOOC-COOH
- Nhóm cacboxyl (-COOH) là nhóm chức của axit cacboxylic.
2. Phân loại
Dựa theo đặc điểm cấu tạo của gốc hiđrocacbon và số nhóm cacboxyl trong phân tử, các axit được chia thành:
- Axit no, đơn chức mạch hở, tổng quát (thường gặp):
CnH2n+1COOH (n ≥ 0) hay CmH2mO2 (m ≥ 1)
Ví dụ: H-COOH, C2H5COOH...
- Axit không no, đơn chức, mạch hở:
Ví dụ: CH2=CH-COOH,....
- Axit thơm, đơn chức:
Ví dụ: C6H5-COOH, CH3-C6H4-COOH,...
- Axit đa chức:
Ví dụ: HOOC-COOH, HOOC-CH2-COOH...
3. Danh pháp
a) Tên thường
Một số axit có tên thông thường liên quan đến nguồn gốc tìm ra chúng. Ví dụ:
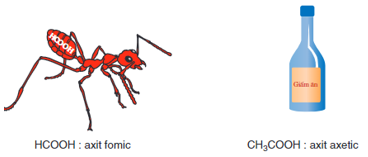
b) Tên thay thế
Tên thay thế của các axit no, đơn chức, mạch hở được xác định như sau:
+ Mạch chính của phân tử axit là mạch dài nhất, bắt đầu từ nhóm – COOH.
+ Mạch cacbon được đánh số bắt đầu từ nguyên tử cacbon của nhóm – COOH.
+ Tên thay thế =Axit + tên hiđrocacbon no tương ứng với mạch chính + oic.
Ví dụ:
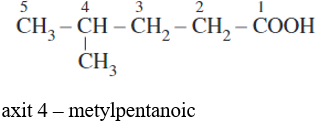
II. Đặc điểm cấu tạo
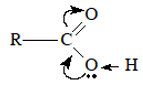
- Nhóm -COOH coi như được kết hợp bởi nhóm C = O và nhóm – OH.
- Liên kết O -H trong phân tử axit phân cực hơn liên kết O–H trong phân tử ancol, do đó nguyên tử H của nhóm COOH linh động hơn nguyên tử H của nhóm – OH ancol.
- Liên kết C- OH của nhóm cacboxyl phân cực mạnh hơn liên kết C – OH của ancol, phenol nên nhóm – OH của axit cacboxylic cũng dễ bị thay thế.
III. Tính chất vật lý
-Ở điều kiện thường các axit cacboxylic đều là những chất lỏng hoặc rắn.
- Nhiệt độ sôi tăng theo chiều tăng M và cao hơn các ancol có cùng M: nguyên nhân là do giữa các phân tử axit cacboxylic có liên kết hiđro bền hơn liên kết hidro giữa các phân tử ancol.
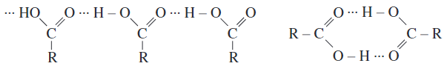
- Mỗi axit có vị riêng: axit axetic có vị giấm ăn, axit oxalic có vị chua của me …
IV. Tính chất hóa học
1.Tính axit
- Trong dung dịch, axit cacboxylic phân li thuận nghịch:
CH3COOH ⇄ H+ + CH3COO-
Dung dịch axit cacboxylic làm quỳ tím chuyển sang màu đỏ
- Tác dụng với bazơ, oxit bazơ tạo thành muối và nước. Ví dụ:
CH3COOH + NaOH → CH3COONa + H2O
2CH3COOH + ZnO → (CH3COO)2Zn + H2O
- Tác dụng với muối:
2CH3COOH + CaCO3 → (CH3COO)2Ca + H2O + CO2
- Tác dụng với kim loại trước hiđro:
2CH3COOH + Zn → (CH3COO)2Zn + H2
2. Phản ứng thế nhóm –OH
- Phản ứng giữa axit và ancol tạo thành este và nước được gọi là phản ứng este hóa.
- Tổng quát:
RCOOH + R’OH RCOOR’ + H2O
- Đặc điểm: phản ứng thuận nghịch, xúc tác H2SO4 đặc.
- Ví dụ:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
V. Điều chế
1. Phương pháp lên men giấm: (phương pháp cổ truyền sản xuất axit axetic)
C2H5OH + O2 CH3COOH + H2O
2. Oxi hóa anđehit axetic:
2CH3CHO + O2 2CH3COOH
3.Oxi hóa ankan:
2R-CH2-CH2-R’ + 5O2 2RCOOH + 2R’COOH + 2H2O
4.Từ metanol:
CH3OH + CO CH3COOH
Đây là phương pháp hiện đại để sản xuất axit axetic.
VI. Ứng dụng
Các axit hữu cơ có ứng dụng trong nhiều lĩnh vực: làm nguyên liệu cho công nghiệp mĩ phẩm, công nghiệp dệt, công nghiệp hóa học …

Trắc nghiệm Hóa học lớp 11 Bài 45: Axit cacboxylic
Bài 1: Các sản phẩm thu được khi đốt cháy hoàn toàn 3 gam axit hữu cơ X được dẫn lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 đựng dung dịch NaOH. Sau thí nghiệm thấy khối lượng bình 1 tăng 1,8 gam và khối lượng bình 2 tăng 4,4 gam. Công thức cấu tạo của X là
A. HCOOH.
B. C2H5COOH.
C. CH3COOH.
D. A hoặc B hoặc C.
Đáp án: C
Giải thích:
Khối lượng bình 1 tăng chính là khối lượng H2O, khối lượng bình 2 tăng chính là khối lượng CO2.
Theo bài ra ta lại có:
nCO2 = nH2O = 0,1 mol
BTKL:
mO = 3 – 0,1.12 – 0,1.2= 1,6 g
=> nO = 0,1 mol
Bảo toàn O có
nX =
Vậy công thức cấu tạo của X là CH3COOH.
Bài 2: Đốt cháy 14,6 gam một axit no đa chức Y ta thu được 0,6 mol CO2 và 0,5 mol nước. Biết mạch cacbon là mạch thẳng. Cho biết công thức cấu tạo của Y
A. HOOC-COOH
B. HOOC-CH2-COOH
C. HOOC-C(CH2)2-COOH
D. HOOC-(CH2)4-COOH
Đáp án: D
Giải thích:
Do axit đa chức => có 2 nhóm COOH trở lên
Mà axit mạch thằng => có không quá 2 nhóm COOH
=> Axit no, 2 chức, mạch thẳng CnH2n-2O4
=>naxit = nCO2 – nH2O = 0,1 mol
=> n = 6 => CTPT C6H10O4
=> HOOC-(CH2)4-COOH
Bài 3: Đốt cháy hết 1 thể tích hơi axit hữu cơ A được 3 thể tích hỗn hợp CO2 và hơi nước khi đo cùng điều kiện. Công thức cấu tạo của A là
A. HCOOH.
B. CH3COOH.
C. HOOC - COOH.
D. HOOC - CH2 - COOH.
Đáp án: C
Giải thích:
Ta có sơ đồ:
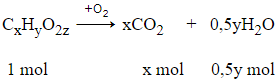
=> x + 0,5y = 3
=> x = 2 và y =2 thỏa mãn.
Vậy công thức cấu tạo của A là HOOC - COOH.
Bài 4: Cho 13,4 gam hỗn hợp X gồm hai axit no, đơn chức, mạch hở, kế tiếp nhau trong cùng dãy đồng đẳng tác dụng với Na dư, thu được 17,8 gam muối. Khối lượng của axit có số nguyên tử cacbon ít hơn có trong X là
A. 3,0 gam.
B. 4,6 gam.
C. 7,4 gam.
D. 6,0 gam.
Đáp án: D
Giải thích:
Tăng giảm khối lượng
=> n axit = mol
=> = 67
=> X chứa CH3COOH và C2H5COOH
Gọi số mol CH3COOH và C2H5COOH lần lượt là x và y
=> x + y = 0,2 và 60x + 74y = 13,4
=> x = 0,1
Bài 5: Chất X (có M = 60 và chứa C, H, O). Chất X phản ứng được với Na, NaOH, NaHCO3, tên gọi của X là
A. axit fomic.
B. metyl fomat.
C. axit axetic.
D. ancol propylic.
Đáp án: C
Giải thích:
X phản ứng được với Na, NaOH, NaHCO3 nên X là axit.
Lại có MX = 60. Vậy X là axit axetic (CH3COOH).
Bài 6: Hỗn hợp X gồm 2 axit no A1 và A2. Đốt cháy hoàn toàn 0,3 mol X thu được 11,2 lít CO2 (đkc). Để trung hòa 0,3 mol X cần 500 ml dung dịch NaOH 1M. Công thức cấu tạo của 2 axit là
A. HCOOH và C2H5COOH.
B. CH3COOH và C2H5COOH.
C. HCOOH và HOOC - COOH.
D. CH3COOH và HOOC - CH2 - COOH.
Đáp án: C
Giải thích:
0,3 mol X + 0,5 mol NaOH
=> X chứa 0,2 mol axit 2 chức và 0,1 mol axit đơn chức
Số C trung bình là = 1,67
=> Axit đơn chức là HCOOH
=> Số C của axit còn lại là
=> Axit HOOC-COOH
Bài 7: Hỗn hợp X gồm 2 axit cacboxylic no, mạch hở Y và Z (phân tử khối của Y nhỏ hơn phân tử khối của Z). Đốt cháy hoàn toàn a mol X, sau phản ứng thu được a mol H2O. Mặt khác nếu a mol X tác dụng với lượng dư dung dịch NaHCO3 thì thu được 1,6a mol CO2. Thành phần % theo khối lượng của Y trong X là:
A. 46,67%
B. 40%
C. 25,41%
D. 74,59%
Đáp án: C
Giải thích:
Đốt a mol X a mol H2
=> Cả Y và Z đều chứa 2 nguyên tử H
a mol X + Na2CO3 1,6a mol CO2
=> Y là axit đơn chức, Z là axit 2 chức
Từ đó, Y là HCOOH; Z là HOOC-COOH
Dễ thấy nHOOC-COOH = 0,6a mol ;
nHCOOH = 0,4a mol
=> % m HCOOH = %
Bài 8: Đốt cháy hết 1 thể tích hơi axit A thu được 2 thể tích CO2 đo ở cùng điều kiện, A là
A. HCOOH.
B. HOOC - COOH.
C. CH3COOH.
D. B và C đúng.
Đáp án: D
Giải thích:
1A 2CO2
=> A chứa 2 nguyên tử C
Theo các đáp án đã cho
=> A là HOOC-COOH hoặc CH3COOH.
Bài 9: Đốt cháy hoàn toàn 0,44 gam một axit hữu cơ, sản phẩm cháy cho hấp thụ hoàn toàn vào bình 1 đựng P2O5, bình 2 đựng dung dịch KOH. Sau thí nghiệm thấy khối lượng bình 1 tăng 0,36 gam và bình 2 tăng 0,88 gam. Công thức phân tử của axit là
A. C4H8O2.
B. C5H10O2.
C. C2H6O2.
D. C2H4O2.
Đáp án: A
Giải thích:
Khối lượng bình 1 tăng là khối lượng H2O; khối lượng bình 2 tăng là khối lượng CO2.
Ta có:
Vậy axit là no, đơn chức, mạch hở: CnH2nO2
BTKL:
Bảo toàn nguyên tố O có:
Vậy công thức phân tử của axit là C4H8O2.
Bài 10: Hỗn hợp X gồm axit axetic, axit fomic và axit oxalic. Khi cho m gam X tác dụng với NaHCO3 (dư) thì thu được 15,68 lít khí CO2 (đktc). Mặt khác, đốt cháy hoàn toàn m gam X cần 8,96 lit khí O2 (đktc), thu được 35,2 gam CO2 và a mol H2O. Giá trị của a là:
A. 0,3
B. 0,2
C. 0,6
D. 0,8
Đáp án: C
Giải thích:
- Xét phản ứng của hỗn hợp X với NaHCO3:
Bảo toàn nguyên tố:
n-COOH trong X = nCO2 = 0,7 mol
=> n O trong X = 1,4 mol
- Xét phản ứng đốt cháy hỗn hợp X:
BTNT:
nO trong X + 2nO2 = 2nCO2 + nH2O
=> nH2O = 1,4 + 0,4.2 - 0,8.2
= 0,6 mol.
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 11 đầy đủ, chi tiết khác:
Lý thuyết Bài 42: Luyện tập: Dẫn xuất halogen, ancol và phenol
Lý thuyết Bài 44: Anđehit – Xeton
Lý thuyết Bài 46: Luyện tập: Anđehit – Xeton – Axit cacboxylic
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
