Lý thuyết Dẫn xuất halogen của hiđrocacbon (mới 2023 + Bài Tập) - Hóa học 11
Tóm tắt lý thuyết Hóa 11 Bài 39: Dẫn xuất halogen của hiđrocacbon ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 11 Bài 39.
Lý thuyết Hóa 11 Bài 39: Dẫn xuất halogen của hiđrocacbon
Bài giảng Hóa 11 Bài 39: Dẫn xuất halogen của hiđrocacbon
I. Khái niệm, phân loại
1. Khái niệm
- Khi thay thế nguyên tử hiđro của phân tử hiđrocacbon bằng nguyên tử halogen ta được dẫn xuất halogen của hiđrocacbon.
Ví dụ:
|
Hiđro cacbon |
CH4 |
CH2 = CH2 |
C6H6 |
|
Dẫn xuất halogen |
CH3Cl; CH3Br; CH2Cl2 … |
CH2 = CH – Cl |
C6H5Br |
- Một số cách để thu dẫn xuất halogen:
+ Thay thế nhóm -OH trong phân tử ancol bằng nguyên tử halogen. Ví dụ:
C2H5OH + HBr → C2H5Br + H2O
+ Cộng hợp hiđro halogenua hoặc halogen vào phân tử hiđrocacbon không no.
Ví dụ:
CH2 = CH2 + HBr → CH3 – CH2 – Br
CH2= CH2 + Br2 → CH2Br – CH2Br
+ Thế nguyên tử H của hiđrocacbon bằng nguyên tử halogen.
CH4 + Cl2 CH3Cl + HCl
2. Phân loại
Các dẫn xuất halogen được phân loại dựa vào bản chất của halogen, số lượng của halogen và đặc điểm cấu tạo của gốc hiđrocacbon. Ví dụ:
- Dựa theo cấu tạo của gốc:
+ Dẫn xuất halogen no: CH2FCl, CH2-Cl-CH2Cl, CH3-CHBr-CH3, …
+ Dẫn xuất halogen không no: CF2=CF2, CH2=CH-Cl, CH2=CH-CH2Br, …
+ Dẫn xuất halogen thơm: C6H5F, C6H5CH2Cl, C6H5I, …
- Dựa theo bậc của cacbon: bậc của dẫn xuất halogen chính là bậc của nguyên tử C liên kết trực tiếp với nguyên tử halogen.
+ Dẫn xuất halogen bậc I: CH3CH2Cl (etyl clorua).
+ Dẫn xuất halogen bậc II: CH3CHClCH3 (isopropyl clorua).
+ Dẫn xuất halogen bậc III: (CH3)C-Br (tert - butyl bromua).
II. Tính chất vật lý
- Ở điều kiện thường các dẫn xuất monohalogen có phân tử khối nhỏ như CH3Cl, CH3Br, C2H5Cl là chất khí. Các chất khác là chất lỏng hoặc rắn.
- Không tan trong nước, dễ tan trong các dung môi hữu cơ.
- Nhiều dẫn xuất halogen có hoạt tính sinh học cao như CHCl3 có tác dụng gây mê, C6H6Cl6 (hexacloran) diệt sâu bọ…
III. Tính chất hóa học
Tính chất quan trọng của dẫn xuất halogen là phản ứng thế nguyên tử halogen và phản ứng tách hiđro halogenua.
1. Phản ứng thế nguyên tử halogen bằng nhóm –OH
Ví dụ:
CH3CH2Br + NaOH (loãng) CH3CH2OH + NaBr
Phương trình hóa học chung:
R – X + NaOH R -OH + NaX
2. Phản ứng tách hiđro halogenua
Ví dụ:
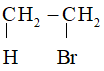 + KOH CH2 = CH2 + KBr + H2O
+ KOH CH2 = CH2 + KBr + H2O
Phản ứng tách hiđro halogenua tuân theo quy tắc tách Zai – xép: Khi tách HX khỏi dẫn xuất halogen, nguyên tử halogen X ưu tiên tách ra cùng nguyên tử H ở cacbon bậc cao hơn bên cạnh tạo sản phẩm chính.
IV. Ứng dụng
a. Làm dung môi
Metylen clorua, clorofom, cacbon tetraclorua, 1,2-đicloetan là những chất lỏng hòa tan được nhiều chất hữu cơ đồng thời chúng còn dễ bay hơi, dễ giải phóng khỏi hỗn hợp, vì thế được dùng làm dung môi để hòa tan hoặc để tinh chế các chất trong phòng thí nghiệm cũng như trong công nghiệp.
b. Làm nguyên liệu cho tổng hợp hữu cơ
- Các dẫn xuất halogen của etilen, của butađien được dùng làm monome để tổng hợp các polime quan trọng.
- Ví dụ:
CH2=CHCl tổng hợp ra PVC dùng chế tạo một số loại ống dẫn, vải giả da, ...
CF2=CF2 tổng hợp ra teflon, một polime siêu bền dùng làm những vật liệu chịu kiềm, chịu axit, chịu mài mòn, ...
Teflon bền với nhiệt tới trên 300oC nên được dùng làm lớp che phủ chống bám dính cho xoong, chảo, thùng chứa.
c. Các ứng dụng khác
- Dẫn xuất halogen thường là những hợp chất có hoạt tính sinh học rất đa dạng.
Ví dụ:
+ CHCl3,ClBrCH−CF3 được dùng làm chất gây mê trong phẫu thuật.
+ Một số dẫn xuất halogen được dùng là thuốc trừ sâu, phòng bệnh cho cây trồng.
+ CFCl3 và CF2Cl2 trước đây được dùng phổ biến trong các máy lạnh, hộp xịt ngày nay đang bị cấm sử dụng, do chúng gây tác hại cho tầng ozon.
Trắc nghiệm Hóa học lớp 11 Bài 39: Dẫn xuất halogen của hidrocacbon
Bài 1: Đun nóng 13,875 gam một ankyl clorua Y với dung dịch NaOH dư, axit hóa dung dịch thu được bằng dung dịch HNO3, nhỏ tiếp vào dung dịch AgNO3 thấy tạo thành 21,525 gam kết tủa. CTPT của Y là :
A. C2H5Cl.
B. C3H7Cl.
C. C4H9Cl.
D. C5H11Cl
Đáp án: C
Giải thích:
Đặt công thức của Y là RCl, phương trình phản ứng :
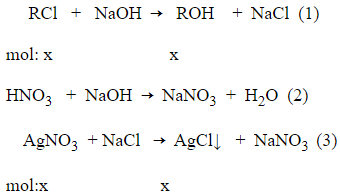
Theo giả thiết và các phản ứng ta có :
Vậy Y là C4H9Cl.
Bài 2: Đun nóng 1,91 gam hỗn hợp X gồm C3H7Cl và C6H5Cl với dung dịch NaOH loãng vừa đủ, sau đó thêm tiếp dung dịch AgNO3 đến dư vào hỗn hợp sau phản ứng, thu được 1,435 gam kết tủa. Khối lượng C6H5Cl trong hỗn hợp đầu là
A. 1,125 gam.
B. 1,570 gam.
C. 0,875 gam.
D. 2,250 gam
Đáp án: A
Giải thích:
Căn cứ vào các tính chất của các halogen ta thấy chỉ có C3H7Cl phản ứng được với dung dịch NaOH đun nóng.
Phương trình phản ứng :
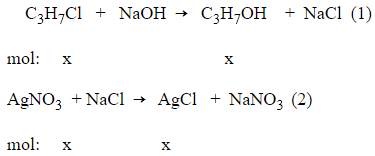
Theo (1), (2) và giả thiết ta có :
Chú ý: C6H5Cl phản ứng với NaOH ở nhiệt độ cao, áp suất cao.
Bài 3: Hỗn hợp X gồm 0,1 mol anlyl clorua; 0,3 mol benzyl bromua ; 0,1 mol hexyl clorua ; 0,15 mol phenyl bromua. Đun sôi X với nước đến khi phản ứng xảy ra hoàn toàn, chiết lấy phần nước lọc, rồi cho tác dụng với dung dịch AgNO3 dư thu được m gam kết tủa. Giá trị của m là
A. 28,7.
B. 57,4.
C. 70,75.
D. 14,35
Đáp án: C
Giải thích:
Khi đun sôi hỗn hợp X trong nước thì chỉ có anlyl clorua và benzyl bromua bị thủy phân.
Phương trình phản ứng :
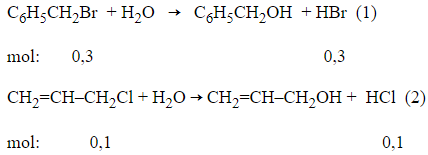

Theo các phương trình phản ứng và giả thiết ta có :
m = 0,3.188 + 0,1.143,5 = 70,75 gam.
Bài 4: Đun nóng 27,40 gam CH3CHBrCH2CH3 với KOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai olefin trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đktc)? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%
A. 4,48 lít.
B. 8,96 lít.
C. 11,20 lít.
D. 17,92 lít
Đáp án: D
Giải thích:
Khi đun nóng CH3CHBrCH2CH3 với KOH dư trong C2H5OH thì thu được hai sản phẩm hữu cơ là but-1-en và but-2-en.
Phương trình phản ứng :
C4H8 + 6O2 4CO2 + 4H2O
Theo các phương trình phản ứng và giả thiết ta thấy:
Vậy lít.
Bài 5: Đun sôi 15,7 gam C3H7Cl với hỗn hợp KOH/C2H5OH dư, sau khi loại tạp chất và dẫn khí sinh ra qua dung dịch brom dư thấy có x gam Br2 tham gia phản ứng. Tính x nếu hiệu suất phản ứng ban đầu là 80%.
A. 25,6 gam.
B. 32 gam.
C. 16 gam.
D. 12,8 gam
Đáp án: A
Giải thích:
Phương trình phản ứng :
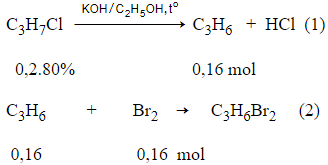
Theo các phản ứng và giả thiết ta có :
x = 0,16.160 = 25,6 gam.
Bài 6: Khi cho but-1-en tác dụng với dung dịch HBr, theo quy tắc Mac-cop-nhi-cop thì sản phẩm chính thu được là
A. CH3-CH2-CHBr-CH2Br
B. CH3-CH2-CHBr-CH3
C. CH2Br-CH2-CH2-CH2Br
D. CH3-CH2-CH2-CH2Br
Đáp án: B
Giải thích:
Phương trình hóa học:
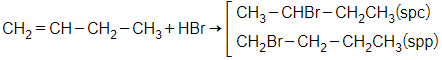
Bài 7: Số đồng phân cấu tạo anken ở thể khí (đktc) mà khi cho mỗi anken đó tác dụng với dung dịch HCl chỉ cho một sản phẩm hữu cơ duy nhất là
A. 2
B. 1
C. 3.
D. 4.
Đáp án: A
Giải thích:
Có 2 công thức thỏa mãn là:
CH2=CH2
CH3-CH=CH-CH3
Bài 8: Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ dung dịch X
Hình vẽ trên minh họa cho phản ứng
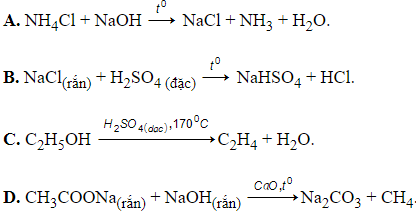
Đáp án: C
Giải thích:
Khí Y được thu bằng phương pháp dời chỗ của nước, nên khí Y không tan trong nước → loại đáp án A, B
Khí Y được điều chế từ dung dịch X → loại đáp án D
Bài 9: 0,05 mol hiđrocacbon mạch hở X làm mất màu vừa đủ dung dịch chứa 8 gam brom cho ra sản phẩm có hàm lượng brom đạt 69,56%. Công thức phân tử của X là
A. C3H6
B. C4H8
C. C5H10
D. C5H8
Đáp án: C
Giải thích:
Xét tỉ lệ
→ X là anken CnH2n (n ≥ 2)
Phương trình hóa học:
CnH2n + Br2 → CnH2nBr2
Ta có:
→ n = 5
Vậy công thức của X là C5H10
Câu 10: Cho hiđrocacbon mạch hở X phản ứng với brom (dung dịch) theo tỉ lệ mol 1:1, thu được chất hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau. Tên gọi của X là
A. but-1-en
B. but-2-en
C. propilen
D. butan
Đáp án: A
Giải thích:
X phản ứng với Br2 theo tỉ lệ mol 1:1 nên X là anken, có công thức CnH2n (n ≥ 2)
Phương trình hóa học:
CnH2n + Br2 → CnH2nBr2
Ta có:
→ n = 4
Vậy công thức của X là C4H8
Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau nên X là but-1-en
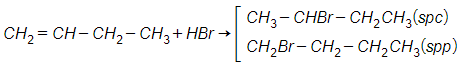
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 11 đầy đủ, chi tiết khác:
Lý thuyết Bài 42: Luyện tập: Dẫn xuất halogen, ancol và phenol
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
