Lý thuyết Axit photphoric và muối photphat (mới 2023 + Bài Tập) - Hóa học 11
Tóm tắt lý thuyết Hóa 11 Bài 11: Axit photphoric và muối photphat ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 11 Bài 11.
Lý thuyết Hóa 11 Bài 11: Axit photphoric và muối photphat
Bài giảng Hóa 11 Bài 11: Axit photphoric và muối photphat
A. Axit photphoric H3PO4
I. Cấu tạo phân tử
- Công thức cấu tạo:
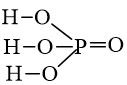
- Trong hợp chất H3PO4, photpho có số oxi hóa cao nhất là +5.
II. Tính chất vật lí
- Là chất rắn dạng tinh thể trong suốt, nóng chảy ở 42,5ºC, rất háo nước nên dễ chảy rữa và tan vô hạn trong nước.
- Axit photphoric thường dùng là dung dịch đặc, sánh, không màu, có nồng độ 85%.
III. Tính chất hóa học
Khác với axit nitric, axit photphoric không có tính oxi hóa.
1. Axit photphoric là axit ba nấc
- Trong dung dịch nước, axit photphoric phân li theo từng nấc:
Nấc 1:
Nấc 2:
Nấc 3:
- Sự phân li chủ yếu xảy ra theo nấc 1, nấc 2 kém hơn và nấc 3 rất yếu.
- Như vậy trong dung dịch axit photphoric có các ion: và các phân tử H3PO4 không phân li (không kể các ion H+ và OH- do nước phân li ra).
2. Axit photphoric có độ mạnh trung bình
- Dung dịch axit photphoric có những tính chất chung của axit như làm quỳ tím hóa đỏ, tác dụng với oxit bazơ, bazơ, muối, kim loại.
Lưu ý: Khi tác dụng với dung dịch kiềm, tùy theo lượng chất tác dụng mà axit photphoric tạo ra muối trung hòa, muối axit hoặc hỗn hợp muối.
Thí dụ:
H3PO4+NaOH→NaH2PO4+H2O
H3PO4+2NaOH→Na2HPO4+2H2O
H3PO4+3NaOH→Na3PO4+3H2O
IV. Ứng dụng và điều chế
1. Ứng dụng
- Một lượng lớn axit photphoric dùng để điều chế các muối photphat và sản xuất phân lân, thuốc trừ sâu,…

Hình 1: Phân lân nung chảy dạng viên
- Axit H3PO4 tinh khiết được dùng trong công nghiệp dược phẩm.
2. Điều chế
a) Trong phòng thí nghiệm
P+5HNO3đặcH3PO4+H2O+5NO2
b) Trong công nghiệp
+ Cho H2SO4 đặc tác dụng với quặng photphorit hoặc quặng apatit:
Ca3(PO4)2+3H2SO4đặc3CaSO4↓+2H3PO4
→ Điều chế bằng phương pháp này không tinh khiết và lượng chất thấp.
+ Để điều chế H3PO4 có độ tinh khiết và nồng độ cao hơn người ta đốt cháy P để được P2O5, rồi cho P2O5 tác dụng với nước:
4P+5O22P2O5
P2O5+3H2O→2H3PO4
B. MUỐI PHOTPHAT
Axit photphoric tác dụng với dung dịch kiềm, tạo ra 3 loại muối:
- Muối photphat trung hòa: Na3PO4, Ca3(PO4)2, …
- Muối đihiđrophotphat: NaH2PO4, Ca(H2PO4)2, …
- Muối hiđrophotphat: Na2HPO4, CaHPO4, …
1. Tính tan
Tất cả các muối đihiđrophotphat đều tan trong nước. Các muối hiđrophotphat và photphat trung hòa đều không tan hoặc ít tan trong nước (trừ muối natri, kali, amoni).
2. Nhận biết ion photphat ()
- Thuốc thử là bạc nitrat.
- Hiện tượng: Xuất hiện kết tủa màu vàng.
- Phương trình ion rút gọn:
3Ag+ + → Ag3PO4↓ (màu vàng)
Lưu ý: Kết tủa Ag3PO4 không tan trong nước, nhưng tan trong dung dịch axit nitric loãng.

Hình 2: Cho AgNO3 tác dụng với Na3PO4.
Trắc nghiệm Hóa 11 Bài 11: Axit photphoric và muối photphat
Câu 1: Trong công nghiệp, để sản xuất axit H3PO4 có độ tinh khiết và nồng độ cao, người ta làm cách nào sau đây ?
A. Cho photpho tác dụng với dung dịch HNO3 đặc, nóng.
B. Cho dung dịch H2SO4 đặc, nóng tác dụng với quặng apatit.
C. Đốt cháy photpho trong oxi dư, cho sản phẩm tác dụng với nước.
D. Cho dung dịch axit H2SO4 đặc, nóng tác dụng với quặng photphorit.
Đáp án: C
Giải thích:
Để thu được axit H3PO4 có độ tinh khiết và nồng độ cao hơn, người ta đốt cháy photpho để thu được P2O5, rồi cho P2O5 tác dụng với nước:
4P + 5O2 2P2O5.
P2O5 + 3H2O → 2H3PO4
Câu 2: Thành phần chính của quặng photphorit là
A. CaHPO4
B. Ca3(PO4)2
C. NH4H2PO4
D. Ca(H2PO4)2
Đáp án: B
Giải thích: Thành phần chính của quặng photphorit là Ca3(PO4)2.
Câu 3: Thành phần chính của quặng nào sau đây chứa muối photphat?
A. manhetit.
B. apatit.
C. cromit.
D. boxit.
Đáp án: B
Giải thích: Thành phần chính của quặng apatit là 3Ca3(PO4)2.CaF2.
Câu 4: Axit phophoric không thể được điều chế trực tiếp từ
A. photpho
B. điphotpho pentaoxit.
C. photphin.
D. canxi photphat.
Đáp án: C
Giải thích:
Các cách điều chế H3PO4 là
P + 5HNO3 → H3PO4 + 5NO2 + H2O
P2O5 + 3H2O → 2H3PO4
Ca3(PO4)2 + 3H2SO4 đặc, nóng → 3CaSO4 ↓+ 2H3PO4
Không điều chế được H3PO4 từ PH3 (photphin)
Câu 5: Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Đáp án: C
Giải thích:
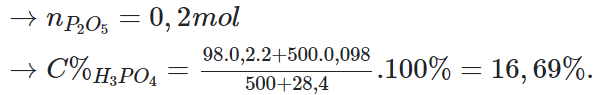
Câu 6: Đốt cháy 15,5 gam photpho rồi hoà tan sản phẩm vào 200 gam nước. C% của dung dịch axit thu được là
A. 11,36%
B. 20,8%
C. 24,5%
D. 22,7%
Đáp án: B
Giải thích:
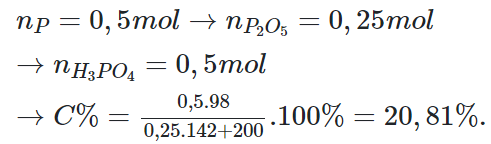
Câu 7: Cho 44 gam dung dịch NaOH 10% tác dụng với 20 gam dung dịch axit photphoric 39,2%. Muối thu được sau phản ứng là
A. NaH2PO4.
B. NaH2PO4 và Na2HPO4.
C. Na2HPO4 và Na3PO4.
D. Na3PO4.
Đáp án: B
Giải thích:
→ muối thu được sau phản ứng là NaH2PO4 và Na2HPO4
Câu 8: Đốt cháy hoàn toàn m gam photpho trong oxi dư. Cho toàn bộ sản phẩm tạo thành vào 500 ml dung dịch chứa hỗn hợp NaOH 0,1M và KOH 0,2M đến khi các phản ứng xảy ra hoàn toàn, cô cạn dung dịch sau phản ứng, làm khô các chất thu được 9,448 gam chất rắn khan. Giá trị của m là
A. 1,426.
B. 1,395.
C. 1,302.
D. 1,085.
Đáp án: C
Giải thích:
Gọi công thức chung của 2 bazơ mà MOH
Ta có:
TH1: Dung dịch sau phản ứng chỉ chứa muối
→
Bảo toàn khối lượng cho phản ứng H3PO4 + kiềm ta có :
mmuối +
→ mchất rắn + 0,15.18
→ m = 1,4389 gam
→ Không thỏa mãn.
TH2: Chất rắn có chứa MOH dư (a mol) và M3PO4 (b mol)
Ta có hệ phương trình:
Bảo toàn nguyên tố P:
Câu 9: Hòa tan 19,2 gam Cu vào 500 ml dung dịch NaNO3 1M sau đó thêm vào 500 ml dung dịch HCl 2M. Kết thúc phản ứng thu được dung dịch X và khí NO duy nhất. Phải thêm bao nhiêu ml dung dịch NaOH 1M vào X để kết tủa hết Cu2+ ?
A. 600 ml.
B. 800 ml.
C. 400 ml.
D. 120 ml.
Đáp án: B
Giải thích:
Số mol electron tối đa mà nhận là:
Số mol electron tối đa mà Cu nhường là:
→ Cu đã phản ứng hết và axit dư
Bảo toàn electron:
→
→ phản ứng =
→ dư = 0,2 mol
→ dư = 0,8 mol
lít = 800ml
Câu 10: Cho 142 gam P2O5 vào 500 gam dung dịch H3PO4 23,72% được dung dịch A. Tìm nồng độ % của dung dịch A.
A. 63%.
B. 32%.
C. 49%.
D. 56%.
Đáp án: C
Giải thích:
Ta có: → thêm = 2 mol.
mdung dịch A = 142 + 500 = 642 gam.
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 11 đầy đủ, chi tiết khác:
Lý thuyết Bài 12: Phân bón hóa học
Lý thuyết Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
