Cấu hình electron của Mg, magnesium (magie) chương trình mới
Bài viết hướng dẫn cách viết Cấu hình electron của Mg, magnesium (magie) theo chương trình sách mới của ba bộ sách Kết nối tri thức, Cánh diều, Chân trời sáng tạo giúp học sinh dễ dàng nắm vững cách viết Cấu hình electron của Mg, magnesium (magie).
Từ cấu hình electron của magnesium ta có thể suy ra được những điều gì về vị trí và tính chất của nguyên tố này? Mời các em cùng theo dõi bài viết dưới đây.
Cấu hình electron của Mg, magnesium (magie) chương trình mới
1. Cấu hình electron nguyên tử magnesium (Z = 12)
- Magnesium có kí hiệu hóa học là Mg.
- Magnesium có số hiệu nguyên tử là 12 ⇒ nguyên tử Mg có 12 electron.
- Cấu hình electron nguyên tử Mg là 1s22s22p63s2.
Viết gọn: [Ne]3s2.
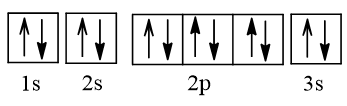
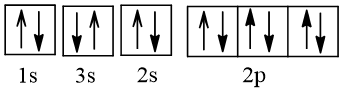
2. Cấu hình electron nguyên tử magnesium (Z = 12) theo ô orbital.
- Cấu hình electron nguyên tử magnesium (Z = 12) theo ô orbital là:
- Nguyên tử Mg không có electron độc thân.
3. Mối quan hệ giữa cấu hình electron với vị trí trong bảng tuần hoàn và tính chất nguyên tố
- Vị trí Mg trong bảng tuần hoàn:
Từ cấu hình electron của Mg là 1s22s22p63s2 ta xác định được:
+ Mg ở ô thứ 12 (do Z = 12)
+ Chu kì 3 (do có 3 lớp electron)
+ Nhóm IIA (do có 2 electron hóa trị, nguyên tố s).
+ Là nguyên tố s (do có cấu hình electron lớp ngoài cùng là 3s2).
- Tính chất nguyên tố:
+ Mg thuộc nhóm IIA (nhóm kim loại kiềm thổ) nên Mg là kim loại mạnh.
+ Mg có 2 electron lớp ngoài cùng, có xu hướng nhường 2 electron này khi hình thành liên kết hóa học để đạt được cấu hình electron bên vững giống khí hiếm Ne (8 electron lớp ngoài cùng).
Mg → Mg2+ + 2e
+ Công thức oxide: MgO (là basic oxide)
+ Công thức base tương ứng: Mg(OH)2 (là base không tan)
4. Ví dụ
Câu 1. Nguyên tố X ở chu kì 3, nhóm IIA của bảng tuần hoàn. Cấu hình electron của nguyên tử nguyên tố X là
A. 1s22s22p6
B. 1s22s22p63s23p1
C. 1s22s22p63s3
D. 1s22s22p63s2
Lời giải:
Đáp án đúng là: D
Nguyên tố X ở chu kì 3 ⇒ Có 3 lớp electron.
Nguyên tố X thuộc nhóm IIA ⇒ Lớp ngoài cùng có 2 electron.
⇒ Cấu hình electron của nguyên tố X là 1s22s22p63s2
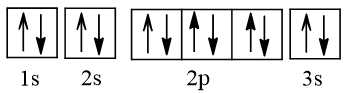
Câu 2. Cho nguyên tử X có Z = 12. Cách biểu diễn cấu hình electron theo ô orbital của X như nào sau đây là đúng?
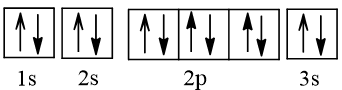
A.
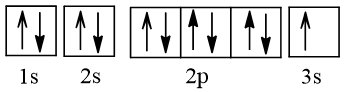
B.
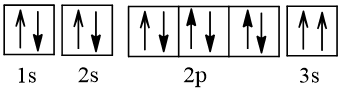
C.
D.
Lời giải:
Đáp án đúng là: A
X có số hiệu nguyên tử Z = số electron = 12
⇒ Cấu hình electron của X: 1s2 2s2 2p6 3s2
⇒ Cách biểu diễn cấu hình electron theo ô orbital của X đúng là:
Xem thêm cách viết cấu hình electron của các nguyên tố hóa học hay, chi tiết khác:
Cấu hình electron của H, hydrogen (hiđro) chương trình mới
Cấu hình electron của He, helium (heli) chương trình mới
Cấu hình electron của Li, lithium (liti) chương trình mới
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Tổng hợp các đề đọc - hiểu có đáp án chi tiết
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)