A là hỗn hợp bột gồm 2 oxit của 2 kim loại. Cho CO dư đi qua 1,965 gam A nung nóng
Vietjack.me giới thiệu bộ câu hỏi ôn tập Hóa học có đáp án được biên soạn bám sát chương trình học giúp bạn ôn luyện và bổ sung kiến thức môn Hóa học tốt hơn. Mời các bạn đón xem:
A là hỗn hợp bột gồm 2 oxit của 2 kim loại. Cho CO dư đi qua 1,965 gam A nung nóng
Đề bài: A là hỗn hợp bột gồm 2 oxit của 2 kim loại. Cho CO dư đi qua 1,965 gam A nung nóng, sau phản ứng thu được chất rắn X và khí Y. Dẫn khí Y qua dung dịch Ba(OH)2 dư thu được 2,955 gam kết tủa. Cho X vào dung dịch H2SO4 10% (vừa đủ), không tháy khí thoát ra, thu được dug dịch chỉ chứa một chất tan có nồng độ 11,243% và còn lại 0,96g một chất rắn không phản ứng. Xác định các chất trong A?
Lời giải:
Gọi CTHH của hai oxit là A2On và B2Om (1 ≤ n, m ≤ 3)
Cho X vào dung dịch H2SO4 loãng (vừa đủ), không có khí thoát ra, tạo dung dịch chỉ chứa một chất tan. Suy ra, A chứa một oxit bị khử bởi CO (tan trong H2SO4 loãng), và một oxit không bị khử bởi CO.
Giả sử oxit bị CO khử là A2On
(1)
Ca(OH)2 + CO2 → CaCO3 + H2O (2)
B2Om + mH2SO4 → B2(SO4)m + mH2O (3)
Theo PTHH (2)
Theo PTHH (1)
mà mA = 0,96 gam nên:
Vì n là hóa trị của kim loại nên 1 ≤ n ≤ 3
+ n = 1→ MA = 32 → Loại
+ n = 2 → MA = 64→ A là Cu
+ n = 3 → MA = 96→ Loại
→A chứa CuO
Giả sử có 1 mol B2Om tham gia phản ứng
Theo PTHH(3):
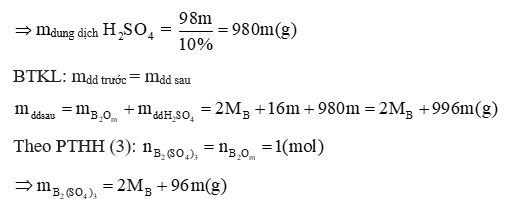
Vì dung dịch chứa muối tan có nồng độ là 11,243% nên ta có phương trình:
Vì m là hóa trị của kim loại nên 1 ≤ m ≤ 3
+ m = 1⇒ M = 9 ⇒ Loại
+ m = 2 ⇒ M = 18 ⇒ Loại
+ m = 3 ⇒ M = 27 ⇒ M là Al
→A chứa Al2O3
Vậy A gồm Al2O3 và CuO.
Xem thêm các câu hỏi Hóa học có đáp án hay, chọn lọc khác:
Phân tử M2O nặng hơn phân tử hiđro 47 lần. Nguyên tử khối của M bằng bao nhiêu
Viết PTHH của các phản ứng xảy ra (nếu có) khi lần lượt cho kim loại sắt vào
Hoà tan 1,15 gam Na vào nước dư. Viết phương trình phản ứng xảy ra
Hỗn hợp 3 kim loại Al , Fe, Cu. Hòa tan hoàn toàn a gam hỗn hợp bằng H2SO4
Cho 4,6g một kim loại nhóm IA vào nước thành dung dịch X. Để trung hòa vừa đủ
Cho 6 gam hỗn hợp hai kim loại thuộc nhóm IA và hai chu kì liên tiếp tác dụng vừa đủ
Cho 5,4 gam một kim loại thuộc nhóm IIIA tác dụng vừa đủ với m gam dung dịch HCl
Tổng số hạt cơ bản trong hợp chất RX2 là 96 hạt. Trong hạt nhân của R và X đều có
Từ một dung dịch có pH = 6 muốn tạo thành dung dịch có pH < 6 thì phải
Cho phương trình hoá học sau SO3 + H2O → H2SO4. Chất tham gia là
Hòa tan hoàn toàn 16,25g kim loại M (chưa rõ hóa trị) vào HCl dư. Khi phản ứng
Bằng phương pháp hóa học hãy phân biệt các khí CO2, N2, NH3, SO2
Trộn 100ml dung dịch HCl 1M với 400 ml dung dịch NaOH 0,375 M. Tính độ pH
Một nguyên tử R có tổng số hạt 95, trong đó số hạt không mang điện bằng 0,5833
Sục từ từ V lít khí SO2 ở đktc vào 100 ml dung dịch Ba(OH)2 1,5M, thu được 23,3
Axit tương ứng của oxit axit SO2 là
Cu có tác dụng được với NaOH không? Vì sao
Để đốt cháy hoàn toàn a gam chất X cần 10,24 gam khí oxi thu được CO2 và H2O
Cho 40 ml dung dịch H2SO4 0,375 M và 160 ml dung dịch chứa đồng thời NaOH 0,16 M
Dẫn 10 lít hỗn hợp khí A gồm CO và CO2 (đktc ) vào 100ml dung dịch Ba(OH)2 2M
Xem thêm các chương trình khác:
- Các dạng bài tập Tiếng Anh thông dụng nhất
- 3000 câu hỏi ôn tập môn Tiếng Anh có đáp án
- Toàn bộ kiến thức về cụm động từ | Định nghĩa và cách dùng
- 500 đoạn văn Tiếng Anh thông dụng nhất và cách làm
- 1000 câu hỏi ôn tập môn Công nghệ có đáp án
- 1000 câu hỏi ôn tập Giáo dục công dân
- 15000 câu hỏi ôn tập môn Toán có đáp án
- Wiki Toán | Khái niệm, định lí, tính chất, dạng bài, công thức
- Tuyển tập đề thi + chuyên đề ôn thi Toán Kangaroo các cấp độ (có đáp án 2024)
- 3000 câu hỏi ôn tập môn Vật lí có đáp án
- Tổng hợp Dạng bài - Công thức môn Vật lí
- 2000 câu hỏi ôn tập môn Tin học có đáp án
- 3000 câu hỏi ôn tập môn Lịch sử có đáp án
- 3000 câu hỏi ôn tập môn Địa lí có đáp án
- 2000 câu hỏi ôn tập môn Sinh học có đáp án
- Tổng hợp Dạng bài - Công thức môn Sinh học
- Tổng hợp về các tác giả văn học
- 3000 câu hỏi ôn tập môn Ngữ văn có đáp án
- Tổng hợp kiến thức Ngữ Văn
- Tuyển tập truyện dân gian, truyền thuyết, cổ tích,... Việt Nam
- Trò chơi Powerpoint | Game Powerpoint
- Tổng hợp bài thu hoạch BDTX Giáo viên mầm non (2025) theo Thông tư 12
- Tổng hợp bài thu hoạch BDTX Giáo viên tiểu học (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THCS (2025)
- Tổng hợp bài thu hoạch BDTX Giáo viên THPT (2025)
