Lý thuyết KHTN 8 Bài 7 (Cánh diều): Tốc độ phản ứng và chất xúc tác
Tóm tắt lý thuyết Khoa học tự nhiên lớp 8 Bài 7: Tốc độ phản ứng và chất xúc tác đầy đủ, chi tiết sách Cánh diều sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt KHTN 8.
Lý thuyết KHTN 8 Bài 7: Tốc độ phản ứng và chất xúc tác
A. Kiến thức trọng tâm KHTN 8 Bài 7: Tốc độ phản ứng và chất xúc tác
I. Tốc độ phản ứng hoá học là gì?
Phản ứng hoá học xảy ra với những tốc độ rất khác nhau, có phản ứng xảy ra rất nhanh nhưng cũng có phản ứng xảy ra rất chậm.
Ví dụ: Phản ứng đốt cháy cồn xảy ra nhanh hơn rất nhiều so với sự gỉ sắt.
|
|
|
|
Sự cháy của cồn |
Sự gỉ sắt |
Tốc độ phản ứng là đại lượng chỉ mức độ nhanh hay chậm của một phản ứng hoá học.
II. Các yếu tố ảnh hưởng đến tốc độ của một phản ứng hoá học
Tốc độ của phản ứng hoá học phụ thuộc vào nhiều yếu tố khác nhau. Các yếu tố ảnh hưởng đến tốc độ của một phản ứng hoá học có thể là: diện tích bề mặt tiếp xúc, nhiệt độ, nồng độ, sự có mặt của chất xúc tác, chất ức chế.
1. Ảnh hưởng của diện tích bề mặt tiếp xúc
Nếu chia một vật thành nhiều phần nhỏ hơn thì tổng diện tích bề mặt sẽ tăng lên. Diện tích bề mặt tiếp xúc càng lớn, tốc độ phản ứng càng nhanh.
Ví dụ:
- Nấu cháo từ bột gạo sẽ nhanh hơn nấu cháo từ hạt gạo.
- Thanh củi được chẻ nhỏ sẽ cháy nhanh hơn thanh củi to.
Kết luận: Diện tích bề mặt tiếp xúc có ảnh hưởng đến tốc độ của phản ứng hoá học. Diện tích bề mặt tiếp xúc càng lớn, tốc độ phản ứng càng nhanh.
2. Ảnh hưởng của nhiệt độ
Nhiệt độ có ảnh hưởng đến tốc độ của phản ứng hoá học. Khi tăng nhiệt độ, phản ứng diễn ra với tốc độ nhanh hơn.
Ví dụ:
Ở điều kiện nhiệt độ phòng, vi khuẩn trong sữa có thể thực hiện nhiều phản ứng hoá học khác nhau làm cho sữa nhanh chóng bị hỏng. Để giảm thiểu điều này, chúng ta thường bảo quản sữa cũng như các thực phẩm khác trong tủ lạnh để giữ chúng được lâu hơn.
3. Ảnh hưởng của nồng độ
Nồng độ có ảnh hưởng đến tốc độ của phản ứng hoá học. Nồng độ các chất phản ứng càng cao, tốc độ phản ứng càng nhanh.
4. Chất xúc tác và chất ức chế
Chất xúc tác là chất làm tăng tốc độ phản ứng nhưng không bị thay đổi cả về lượng và chất sau phản ứng.
Đôi khi việc kiểm soát để phản ứng xảy ra chậm lại cũng rất cần thiết. Chất được sử dụng để làm giảm tốc độ phản ứng được gọi là chất ức chế. Các chất bảo quản là một loại chất ức chế được sử dụng trong thực phẩm để ngăn ngừa hoặc làm chậm lại sự thối rữa, hư hỏng gây ra bởi sự phát triển của các vi sinh vật hay do các thay đổi không mong muốn về mặt hoá học.
B. Bài tập KHTN 8 Bài 7: Tốc độ phản ứng và chất xúc tác
Câu 1: Trong phòng thí nghiệm, có thể điều chế khí oxi từ muối kali clorat. Người ta sử dụng cách nào sau đây nhằm mục đích tăng tốc độ phản ứng ?
A. Nung kaliclorat ở nhiệt độ cao.
B. Nung hỗn hợp kali clorat và mangan đioxit ở nhiệt độ cao.
C. Dùng phương pháp dời nước để thu khí oxi.
D. Dùng phương pháp dời không khí để thu khí oxi.
Đáp án đúng: B
Giải thích:
- Trong phòng thí nghiệm, có thể điều chế khí oxi từ muối kali clorat. Người ta sử dụng nung hỗn hợp kali clorat và mangan đioxit ở nhiệt độ cao nhằm mục đích tăng tốc độ phản ứng.
- Ta có PTHH:
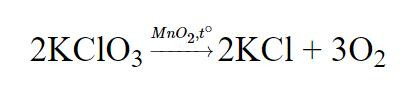
Câu 2: Trong quá trình sản xuất sulfuric acid có giai đoạn tổng hợp sulfur trioxide (SO3). Phản ứng xảy ra như sau: 2SO2 + O2 → 2SO3.
Khi có mặt vanadium(V) oxide thì phản ứng xảy ra nhanh hơn. Vanadium(V) oxide đóng vai trò gì trong phản ứng tổng hợp sulfur trioxide?
A. Chất phản ứng
B. Sản phẩm
C. Chất xúc tác
D. Không đóng vai trò gì
Đáp án đúng: C
Câu 3: Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố nào ảnh hưởng đến tốc độ của phản ứng đốt cháy than?
A. Nồng độ
B. Không khí
C. Vật liệu
D. Hóa chất
Đáp án đúng: A
Câu 4: Tốc độ phản ứng không phụ thuộc yếu tố nào sau đây.
A. Thời gian xảy ra phản ứng.
B. Bề mặt tiếp xúc giữa các chất phản ứng.
C. Nồng độ các chất tham gia phản ứng.
D. Chất xúc tác.
Đáp án đúng: A
Giải thích:
Tốc độ phản ứng phụ thuộc vào 5 yếu tố:
- Yếu tố nồng độ
- Yếu tố chất xúc tác.
- Diện tích bề mặt tiếp xúc.
- Yếu tố áp suất
- Yếu tố nhiệt độ.
Câu 5: Các yếu tố ảnh hưởng đến cân bằng hoá học là .
A. nồng độ, nhiệt độ và chất xúc tác.
B. nồng độ, áp suất và diện tích bề mặt.
C. nồng độ, nhiệt độ và áp suất.
D. áp suất, nhiệt độ và chất xúc tác.
Đáp án đúng: C
Giải thích:
- Nồng độ tăng → chất được tăng sẽ chuyển dịch theo chất tham gia phản ứng. Nồng độ giảm → chuyển dịch theo chiều sinh ra chất đó
- Nhiệt độ tăng → chuyển dịch theo chiều phản ứng thu nhiệt. Nồng độ giảm → chuyển dịch theo phản ứng tỏa nhiệt.
- Áp suất tăng → chuyển dịch theo chiều làm giảm số phân tử khí. Áp suất giảm → chuyển dịch theo chiều làm tăng số phân tử khí.
Xem thêm các bài lý thuyết KHTN 8 sách Cánh diều hay, chi tiết tại:
Xem thêm các chương trình khác:
- Soạn văn lớp 8 Cánh diều (hay nhất)
- Văn mẫu lớp 8 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 8 – Cánh diều
- Bố cục tác phẩm Ngữ văn lớp 8 – Cánh diều
- Tác giả tác phẩm Ngữ văn lớp 8 - Cánh diều
- Giải SBT Ngữ văn 8 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 8 – Cánh diều
- Soạn văn 8 Cánh diều (ngắn nhất)
- Giải sgk Toán 8 – Cánh diều
- Lý thuyết Toán 8 – Cánh diều
- Giải sbt Toán 8 – Cánh diều
- Giải sgk Tiếng Anh 8 – iLearn Smart World
- Giải sbt Tiếng Anh 8 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 8 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 8 ilearn Smart World
- Bài tập Tiếng Anh 8 iLearn Smart World theo Unit có đáp án
- Giải sgk Lịch sử 8 – Cánh diều
- Lý thuyết Lịch sử 8 - Cánh diều
- Giải sbt Lịch sử 8 – Cánh diều
- Giải sgk Địa lí 8 – Cánh diều
- Lý thuyết Địa lí 8 - Cánh diều
- Giải sbt Địa lí 8 – Cánh diều
- Giải sgk Giáo dục công dân 8 – Cánh diều
- Lý thuyết Giáo dục công dân 8 – Cánh diều
- Giải sbt Giáo dục công dân 8 – Cánh diều
- Giải sgk Công nghệ 8 – Cánh diều
- Lý thuyết Công nghệ 8 - Cánh diều
- Giải sbt Công nghệ 8 – Cánh diều
- Giải sgk Tin học 8 – Cánh diều
- Lý thuyết Tin học 8 - Cánh diều
- Giải sbt Tin học 8 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 8 – Cánh diều


