Lý thuyết Axetilen (mới 2024 + Bài Tập) - Hóa học 9
Tóm tắt lý thuyết Hóa 9 Bài 38: Axetilen ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 9 Bài 38.
Lý thuyết Hóa 9 Bài 38: Axetilen
Bài giảng Hóa 9 Bài 38: Axetilen
Công thức phân tử axetilen: C2H2
Phân tử khối: 26
I. Tính chất vật lí
Axetilen là chất khí, không màu, không mùi, nhẹ hơn không khí (), ít tan trong nước.
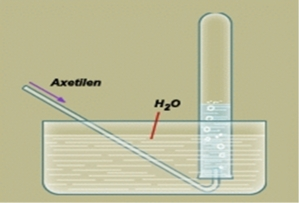
Hình 1: Thu axetilen bằng phương pháp đẩy nước
II. Cấu tạo phân tử
- Axetien có công thức cấu tạo: H – C ≡ C– H; viết gọn HC ≡ CH.
⇒Trong phân tử axetilen có một liên kết ba giữa hai nguyên tử cacbon.
- Chú ý:
Trong liên kết ba, có hai liên kết kém bền, dễ đứt lần lượt trong các phản ứng hóa học.
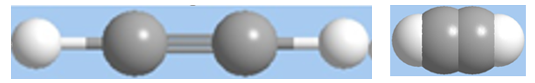
Hình 2: Mô hình phân tử axetilen dạng rỗng và dạng đặc.
III. Tính chất hóa học
1. Tác dụng với oxi
- Khí axetilen cháy tỏa nhiều nhiệt, sản phẩm sinh ra gồm CO2 và nước tương tự metan và etilen.
- Phương trình hóa học:
2C2H2 + 5O2 4CO2 + 2H2O
1 → 2 1 mol
- Nhận xét: Khi đốt cháy axetilen thu được số mol CO2 lớn hơn số mol H2O.
2. Phản ứng cộng với dung dịch brom
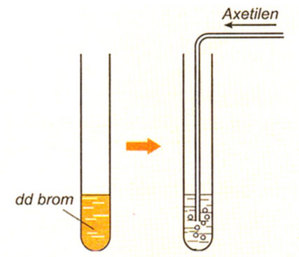
Hình 3: Axetilen tác dụng với dung dịch brom.
- Phương trình hóa học:
HC ≡ CH + Br2 → Br–CH=CH– Br
Sản phẩm mới sinh ra có liên kết đôi trong phân tử nên có thể cộng tiếp với 1 phân tử brom nữa
Br–CH=CH– Br + Br2 → Br2CH–CHBr2
- Tổng quát:
HC≡CH + 2Br2 → Br2CH–CHBr2
Sản phẩm thu được không có màu.
- Trong điều kiện thích hợp, axetilen còn tham gia phản ứng cộng với nhiều chất khác như H2, Cl2...
IV. Ứng dụng
- Khi axetilen cháy trong oxi, nhiệt độ ngọn lửa có thể lên tới 3000oC. Do đó, axetilen dùng làm nhiên liệu trong đèn xì oxi–axetilen để hàn, cắt kim loại.
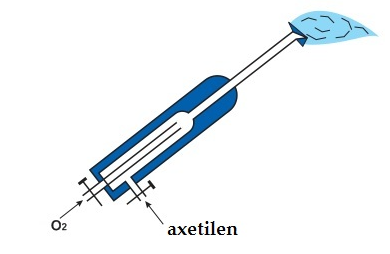
Hình 4: Mô hình đèn xì oxi - axetlen
- Trong công nghiệp axetilen là nguyên liệu để sản xuất poli (vinyl clorua) dùng sản xuất nhựa PVC và nhiều hóa chất khác.
V. Điều chế
- Trong phòng thí nghiệm axetilen được điều chế bằng cách cho canxi cacbua (thành phần chính của đất đèn) phản ứng với nước.
CaC2 + 2H2O → C2H2↑ + Ca(OH)2
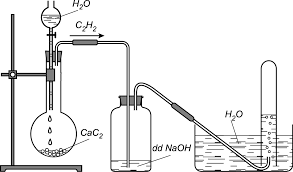
Hình 5: Điều chế và thu khí axetilen trong phòng thí nghiệm
- Phương pháp hiện đại để điều chế axetilen hiện nay là nhiệt phân metan ở nhiệt độ cao, sau đó làm lạnh nhanh.
2CH4 C2H2 + 3H2
Trắc nghiệm Hóa học 9 Bài 38: Axetilen
Câu 1: Cấu tạo phân tử axetilen gồm
A. 2 liên kết đôi và 1 liên kết ba.
B. 1 liên kết đôi và 1 liên kết ba.
C. 2 liên kết đơn và 1 liên kết đôi
D. 2 liên kết đơn và 1 liên kết ba.
Câu 2: Trong phân tử axetilen, giữa 2 nguyên tử cacbon có
A. 2 liên kết đôi.
B. 1 liên kết ba.
C. 1 liên kết đôi.
D. 1 liên kết đơn.
Câu 3: Khí X có tỉ khối đối với hiđro là 13. Khí X là
A. CH4
B. C2H4
C. C2H2
D. C2H6
Câu 4: Trong các chất sau, chất nào có liên kết 3 trong phân tử?
A. C2H4
B. CH4
C. C2H6
D. C2H2
Câu 5: Trong phòng thí nghiệm người ta thu khí axetilen bằng phương pháp nào trong các phương pháp sau?
A. Đẩy không khí
B. Đẩy nước
C. Đẩy nước brom
D. Cả A, B đều đúng
Câu 6: Đốt cháy hoàn toàn 2,24 lít khí C2H2 trong bình chứa khí oxi dư. Thể tích khí CO2 thu được ở đktc là
A. 2,24 lít
B. 4,48 lít
C. 5,60 lít
D. 6,64 lít
Câu 7: Khí axetilen không có tính chất hóa học nào sau đây?
A. Phản ứng thế với clo ngoài ánh sáng.
B. Phản ứng cộng với hiđro.
C. Phản ứng cháy với oxi.
D. Phản ứng cộng với dung dịch brom.
Câu 8: Khi đốt khí axetilen, thu được số mol của CO2 và H2O có tỉ lệ là
A. 1 : 1
B. 1 : 2
C. 1 : 4
D. 2 : 1
Câu 9: Đốt cháy hoàn toàn m gam khí C2H2 cần 3,36 lít khí oxi ở đktc, thu được khí CO2 và H2O. Giá trị của m là
A. 1,56 gam
B. 2,40 gam
C. 3,34 gam
D. 4,50 gam
Câu 10: Phương pháp hiện đại để điều chế axetilen hiện nay là
A. Nhiệt phân metan ở nhiệt độ cao
B. Nhiệt phân canxi cacbua ở nhiệt độ cao
C. Nhiệt phân benzen ở nhiệt độ cao
D. Nhiệt phân etilen ở nhiệt độ cao
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 9 đầy đủ, chi tiết khác:
Lý thuyết Bài 40: Dầu mỏ và khí thiên nhiên
Lý thuyết Bài 42: Luyện tập chương 4: hiđro cacbon. Nhiên liệu
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 9 (hay nhất) | Để học tốt Ngữ văn 9 (sách mới)
- Soạn văn 9 (ngắn nhất)
- Văn mẫu 9 (sách mới) | Để học tốt Ngữ văn 9 Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 9 (sách mới) | Giải bài tập Toán 9 Tập 1, Tập 2
- Giải sbt Toán 9
- Lý thuyết Toán 9
- Các dạng bài tập Toán lớp 9
- Giáo án Toán lớp 9 mới nhất
- Bài tập Toán lớp 9 mới nhất
- Chuyên đề Toán lớp 9 mới nhất
- Giải sgk Tiếng Anh 9 (thí điểm)
- Giải sgk Tiếng Anh 9 (sách mới) | Để học tốt Tiếng Anh 9
- Giải sbt Tiếng Anh 9
- Giải sbt Tiếng Anh 9 (thí điểm)
- Giải sgk Sinh học 9 (sách mới) | Giải bài tập Sinh học 9
- Giải vở bài tập Sinh học 9
- Lý thuyết Sinh học 9
- Giải sbt Sinh học 9
- Giải sgk Vật Lí 9 (sách mới) | Giải bài tập Vật lí 9
- Giải sbt Vật Lí 9
- Lý thuyết Vật Lí 9
- Các dạng bài tập Vật lí lớp 9
- Giải vở bài tập Vật lí 9
- Giải sgk Địa Lí 9 (sách mới) | Giải bài tập Địa lí 9
- Lý thuyết Địa Lí 9
- Giải Tập bản đồ Địa Lí 9
- Giải sgk Tin học 9 (sách mới) | Giải bài tập Tin học 9
- Lý thuyết Tin học 9
- Lý thuyết Giáo dục công dân 9
- Giải vở bài tập Lịch sử 9
- Giải Tập bản đồ Lịch sử 9
- Lý thuyết Lịch sử 9
- Lý thuyết Công nghệ 9
