Lý thuyết Benzen (mới 2024 + Bài Tập) - Hóa học 9
Tóm tắt lý thuyết Hóa 9 Bài 39: Benzen ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 9 Bài 39.
Lý thuyết Hóa 9 Bài 39: Benzen
Bài giảng Hóa 9 Bài 39: Benzen
Công thức phân tử benzen: C6H6
Phân tử khối: 78
I. Tính chất vật lí
Benzen là chất lỏng, không màu, nhẹ hơn nước, không tan trong nước, hòa tan nhiều chất như: dầu ăn, cao su, nến, iot… Benzen độc.
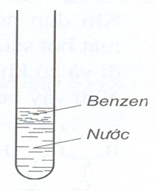
Hình 1: Benzen không tan trong nước
II. Cấu tạo phân tử
- Công thức cấu tạo của benzen:
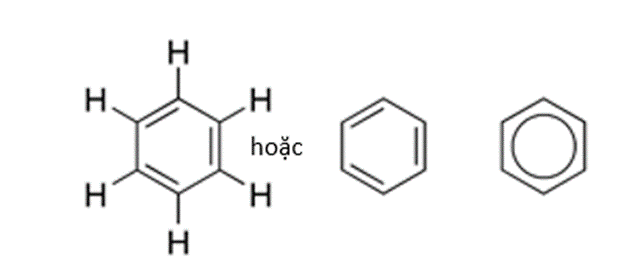
⇒ Trong phân tử benzen: Sáu nguyên tử cacbon liên kết với nhau tạo thành mạch vòng sáu cạnh đều, có ba liên kết đôi xen kẽ ba liên kết đơn.
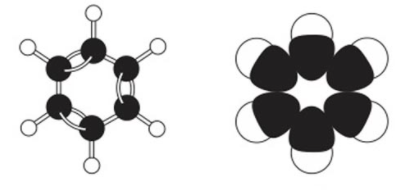
Hình 2: Mô hình phân tử benzen dạng rỗng và dạng đặc.
III. Tính chất hóa học
1. Tác dụng với oxi
- Tương tự các hiđrocacbon khác, benzen cháy trong không khí tạo ra CO2 và H2O. Tuy nhiên, khi benzen cháy trong không khí còn sinh ra muội than.
- Phương trình hóa học:
2C6H6 + 15O2 12CO2 + 6H2O
2. Phản ứng thế với với brom
- Đun nóng hỗn hợp benzen và brom có mặt bột sắt, benzen phản ứng thế với brom.
- Hiện tượng: Màu đỏ nâu của brom mất đi, có khí hidrobromua bay ra.
- Phương trình hóa học:
C6H6 (l) + Br2 (l) HBr (k) + C6H5Br (l) (brom benzen)
Như vậy, nguyên tử H trong vòng benzen được thay thế bởi nguyên tử brom.
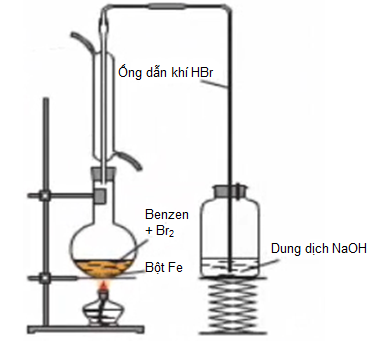
Hình 3: Thí nghiệm benzen tác dụng với brom, có mặt bột sắt.
3. Phản ứng cộng
Do phân tử có cấu tạo đặc biệt nên phản ứng cộng của benzen xảy ra khó hơn so với etilen và axetilen.
Trong điều kiện thích hợp benzen có phản ứng cộng với một số chất như H2, Cl2…
Ví dụ:
C6H6 + 3H2 C6H12
IV. ỨNG DỤNG
- Benzen là nguyên liệu quan trọng để sản xuất chất dẻo, phẩm nhuộm, dược phẩm, thuốc trừ sâu…
- Benzen được sử dụng làm dung môi trong công nghiệp và trong phòng thí nghiệm hữu cơ.
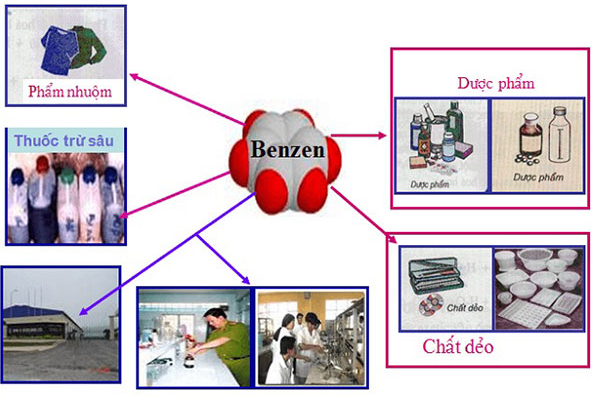
Hình 4: Một số ứng dụng của benzen
Trắc nghiệm Hóa học 9 Bài 39: Benzen
Câu 1: Tính chất vật lý của benzen là
A. Benzen là chất lỏng, không màu.
B. Benzen độc.
C. Benzen không tan trong nước.
D. Cả A, B, C đều đúng
Câu 2: Trong phân tử benzen có
A. 9 liên kết đơn, 6 liên kết đôi
B. 9 liên kết đơn, 3 liên kết đôi
C. 12 liên kết đơn, 3 liên kết đôi
D. 6 liên kết đơn, 3 liên kết đôi
Câu 3: Một hợp chất hữu cơ X có phân tử khối là 78 đvC. Vậy hợp chất hữu cơ X là
A. Benzen
B. Metan
C. Etilen
D. Axetilen
Câu 4: Tính chất hóa học của benzen là
A. Tác dụng với oxi.
B. Phản ứng thế với brom.
C. Phản ứng cộng.
D. Cả A, B, C đều đúng
Câu 5: Đốt cháy benzen trong không khí tạo ra CO2 và H2O có tỉ lệ là
A. 1 : 2
B. 1 : 3
C. 3 : 1
D. 2 : 1
Câu 6: Đun nóng brom với 3,9 gam benzen (có bột sắt), người ta thu được 4,71 gam brombenzen. Hiệu suất của phản ứng là
A. 60%
B. 70%
C. 80%
D. 90%
Câu 7: Benzen có ứng dụng nào sau đây?
A. Benzen là nguyên liệu quan trọng để sản xuất chất dẻo, phẩm nhuộm, dược phẩm, thuốc trừ sâu…
B. Benzen được sử dụng làm dung môi trong công nghiệp.
C. Benzen được sử dụng làm dung môi trong phòng thí nghiệm hữu cơ.
D. Cả A, B, C đều đúng.
Câu 8: Phản ứng đặc trưng của benzen là
A. Phản ứng cháy
B. Phản ứng trùng hợp
C. Phản ứng thế với brom (có bột sắt)
D. Phản ứng hóa hợp với brom (có bột sắt xúc tác)
Câu 9: Đốt cháy 31,2 gam benzen cần dùng bao nhiêu lít oxi ở đktc?
A. 60,8 lít
B. 58,4 lít
C. 56,6 lít
D. 67,2 lít
Câu 10: Cho benzen tác dụng với Cl2 (ánh sáng) ta thu được dẫn xuất clo X. Vậy X là
A. C6H5Cl
B. C6H4Cl2
C. C6H6Cl6
D. C6H3Cl3
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 9 đầy đủ, chi tiết khác:
Lý thuyết Bài 40: Dầu mỏ và khí thiên nhiên
Lý thuyết Bài 42: Luyện tập chương 4: hiđro cacbon. Nhiên liệu
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 9 (hay nhất) | Để học tốt Ngữ văn 9 (sách mới)
- Soạn văn 9 (ngắn nhất)
- Văn mẫu 9 (sách mới) | Để học tốt Ngữ văn 9 Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 9 (sách mới) | Giải bài tập Toán 9 Tập 1, Tập 2
- Giải sbt Toán 9
- Lý thuyết Toán 9
- Các dạng bài tập Toán lớp 9
- Giáo án Toán lớp 9 mới nhất
- Bài tập Toán lớp 9 mới nhất
- Chuyên đề Toán lớp 9 mới nhất
- Giải sgk Tiếng Anh 9 (thí điểm)
- Giải sgk Tiếng Anh 9 (sách mới) | Để học tốt Tiếng Anh 9
- Giải sbt Tiếng Anh 9
- Giải sbt Tiếng Anh 9 (thí điểm)
- Giải sgk Sinh học 9 (sách mới) | Giải bài tập Sinh học 9
- Giải vở bài tập Sinh học 9
- Lý thuyết Sinh học 9
- Giải sbt Sinh học 9
- Giải sgk Vật Lí 9 (sách mới) | Giải bài tập Vật lí 9
- Giải sbt Vật Lí 9
- Lý thuyết Vật Lí 9
- Các dạng bài tập Vật lí lớp 9
- Giải vở bài tập Vật lí 9
- Giải sgk Địa Lí 9 (sách mới) | Giải bài tập Địa lí 9
- Lý thuyết Địa Lí 9
- Giải Tập bản đồ Địa Lí 9
- Giải sgk Tin học 9 (sách mới) | Giải bài tập Tin học 9
- Lý thuyết Tin học 9
- Lý thuyết Giáo dục công dân 9
- Giải vở bài tập Lịch sử 9
- Giải Tập bản đồ Lịch sử 9
- Lý thuyết Lịch sử 9
- Lý thuyết Công nghệ 9
