Lý thuyết Một số muối quan trọng (mới 2024 + Bài Tập) - Hóa học 9
Tóm tắt lý thuyết Hóa 9 Bài 10: Một số muối quan trọng ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 9 Bài 10.
Lý thuyết Hóa 9 Bài 10: Một số muối quan trọng
Bài giảng Hóa 9 Bài 10: Một số muối quan trọng
I. Muối natri clorua (công thức hóa học NaCl)

Hình 1: Muối ăn (NaCl)
1. Trạng thái tự nhiên
Natri clorua có trong nước biển. Cho nước biển bay hơi, ta được chất rắn là hỗn hợp của nhiều muối, thành phần chính là NaCl (trong 1m3 nước biển có hòa tan chừng 27 kg NaCl, 5kg MgCl2, 1kg CaSO4 và một khối lượng nhỏ những muối khác).
Ngoài ra, trong lòng đất cũng chứa một khối lượng muối natri clorua kết tinh gọi là muối mỏ. Những mỏ muối có nguồn gốc từ những hồ nước mặn đã cạn đi từ hàng triệu năm.

Hình 2: Mỏ muối
2. Cách khai thác
* Ở những nơi có biển hoặc hồ nước mặn, người ta khai thác NaCl từ nước mặn ở trên. Cho nước mặn bay hơi từ từ, thu được muối kết tinh.

Hình 3: Ruộng muối
* Ở những nơi có mỏ muối, người ta đào hầm hoặc giếng sâu đến mỏ muối để lấy muối lên. Muối mỏ sau khi khai thác, được nghiền nhỏ và tinh chế để có muối sạch.
3. Ứng dụng
Muối NaCl có rất nhiều ứng dụng trong đời sống và sản xuất, nó được dùng để:
- Làm gia vị và bảo quản thực phẩm. Muối iot là muối ăn NaCl có trộn thêm một ít KIO3 + KI.
- Làm nguyên liệu để sản xuất: Na, NaOH, H2, Cl2, Na2CO3, nước gia – ven,…
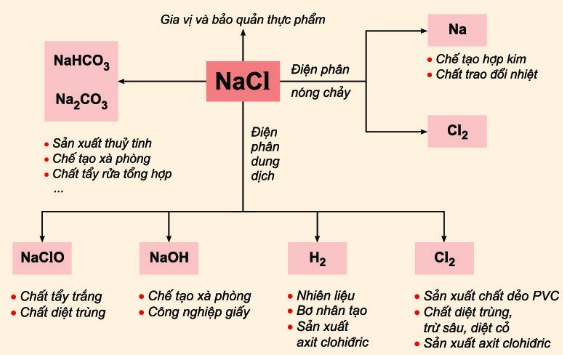
Hình 4: Ứng dụng của muối NaCl
II. Kali nitrat (công thức hóa học KNO3)
KNO3 còn có tên gọi khác là diêm tiêu.
1. Tính chất
KNO3 là chất rắn, màu trắng, tan nhiều trong nước, khi tan thu nhiệt.

Hình 5: Muối kali nitrat
KNO3 bị nhiệt phân hủy: 2KNO3 2KNO2 + O2
2. Ứng dụng
KNO3 dùng chế tạo thuốc nổ đen, làm phân bón, bảo quản thực phẩm trong công nghiệp.
Trắc nghiệm Hóa học 9 Bài 10: Một số muối quan trọng
Câu 1: Trong tự nhiên muối natri clorua có nhiều trong
A. Nước mưa
B. Nước sông
C. Nước giếng
D. Nước biển
Câu 2: Nung kali nitrat ở nhiệt độ cao, sau phản ứng thu được chất khí là
A. N2O
B. NO2
C. O2
D. NO
Câu 3: Hòa tan 14,625 gam NaCl vào nước thu được 200 ml dung dịch. Dung dịch tạo thành có nồng độ mol là
A. 0,75M
B. 1,12M
C. 0,50M
D. 1,25M
Câu 4: Cách khai thác natri clorua là
A. Ở những nơi có biển hoặc hồ nước mặn, người ta khai thác NaCl từ nước mặn trên. Cho nước mặn bay hơi từ từ, thu được muối kết tinh
B. Ở những nơi có mỏ muối, người ta đào hầm hoặc giếng sâu đến mỏ muối để lấy muối lên
C. Muối mỏ sau khi khai thác, được nghiền nhỏ và tinh chế để có muối sạch
D. A, B đều đúng
Câu 5: Hòa tan 15 gam KNO3 vào 110 gam nước, thu được dung dịch A có nồng độ phần trăm là
A. 12%
B. 13%
C. 14%
D. 15%
Câu 6: Ứng dụng của muối kali nitrat là
A. Chế tạo thuốc nổ đen
B. Làm phân bón (cung cấp nguyên tố nitơ và kali cho cây trồng)
C. Bảo quản thực phẩm trong công nghiệp
D. A, B, C đều đúng
Câu 7: Muối kali nitrat (KNO3)
A. Tan nhiều trong nước
B. Tan rất ít trong nước
C. Không tan trong nước
D. Không bị phân hủy ở nhiệt độ cao
Câu 8: Để có được dung dịch NaCl 10% thì khối lượng NaCl cần lấy hòa tan vào 108 gam nước là
A. 11 gam
B. 12 gam
C. 13 gam
D. 14 gam
Câu 9: Để loại bớt muối Na2SO4 có lẫn trong dung dịch NaCl ta dùng
A. Dung dịch AgNO3.
B. Dung dịch HCl.
C. Dung dịch BaCl2.
D. Dung dịch H2SO4
Câu 10: Hoà tan 40 gam muối ăn vào 160 gam nước thu được dung dịch có nồng độ là
A. 10%
B. 15%
C. 20%
D. 25%
Xem thêm các bài tổng hợp lý thuyết Hóa lớp 9 đầy đủ, chi tiết khác:
Lý thuyết Bài 11: Phân bón hóa học
Lý thuyết Bài 12: Mối quan hệ giữa các loại hợp chất vô cơ
Lý thuyết Bài 13: Luyện tập chương 1: Các loại hợp chất vô cơ
Lý thuyết Bài 15: Tính chất vật lý của kim loại
Lý thuyết Bài 16: Tính chất hóa học của kim loại
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 9 (hay nhất) | Để học tốt Ngữ văn 9 (sách mới)
- Soạn văn 9 (ngắn nhất)
- Văn mẫu 9 (sách mới) | Để học tốt Ngữ văn 9 Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 9 (sách mới) | Giải bài tập Toán 9 Tập 1, Tập 2
- Giải sbt Toán 9
- Lý thuyết Toán 9
- Các dạng bài tập Toán lớp 9
- Giáo án Toán lớp 9 mới nhất
- Bài tập Toán lớp 9 mới nhất
- Chuyên đề Toán lớp 9 mới nhất
- Giải sgk Tiếng Anh 9 (thí điểm)
- Giải sgk Tiếng Anh 9 (sách mới) | Để học tốt Tiếng Anh 9
- Giải sbt Tiếng Anh 9
- Giải sbt Tiếng Anh 9 (thí điểm)
- Giải sgk Sinh học 9 (sách mới) | Giải bài tập Sinh học 9
- Giải vở bài tập Sinh học 9
- Lý thuyết Sinh học 9
- Giải sbt Sinh học 9
- Giải sgk Vật Lí 9 (sách mới) | Giải bài tập Vật lí 9
- Giải sbt Vật Lí 9
- Lý thuyết Vật Lí 9
- Các dạng bài tập Vật lí lớp 9
- Giải vở bài tập Vật lí 9
- Giải sgk Địa Lí 9 (sách mới) | Giải bài tập Địa lí 9
- Lý thuyết Địa Lí 9
- Giải Tập bản đồ Địa Lí 9
- Giải sgk Tin học 9 (sách mới) | Giải bài tập Tin học 9
- Lý thuyết Tin học 9
- Lý thuyết Giáo dục công dân 9
- Giải vở bài tập Lịch sử 9
- Giải Tập bản đồ Lịch sử 9
- Lý thuyết Lịch sử 9
- Lý thuyết Công nghệ 9
