Giải Hóa 11 Bài 9: Axit nitric và muối nitrat
Lời giải bài tập Hóa học lớp 11 Bài 9: Axit nitric và muối nitrat chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa 11 Bài 9. Mời các bạn đón xem:
Mục lục Giải Hóa 11 Bài 9: Axit nitric và muối nitrat
Video giải Hóa 11 Bài 9: Axit nitric và muối nitrat
Lời giải:
- Công thức electron:
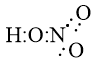
- Công thức cấu tạo:
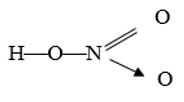
- Nguyên tố nitơ có hoá trị 4 và số oxi hoá +5
Bài 2 trang 45 Hóa 11: Lập các phương trình hoá học:
a) Ag + HNO3 (đặc) → NO2↑ + ? + ?
b) Ag + HNO3 (loãng) → NO↑ + ? + ?
e) FeO + HNO3 → NO↑ + Fe(NO3)3 + ?
f) Fe3O4 + HNO3 → NO↑ + Fe(NO3)3 + ?
Lời giải:
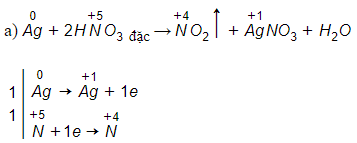
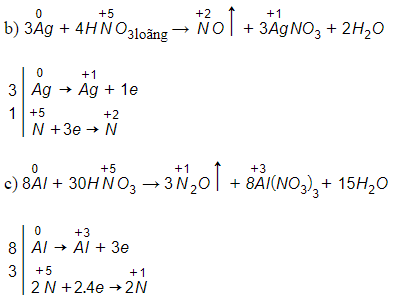
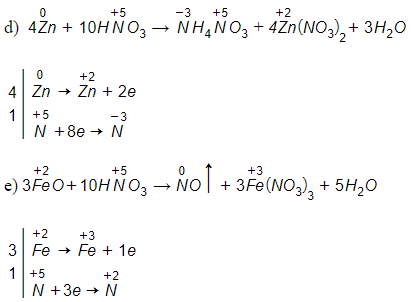
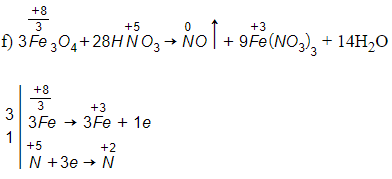
Lời giải:
- Những tính chất khác biệt:
+ Với axit H2SO4 loãng có tính axit, còn H2SO4 đặc mới có tính oxi hoá mạnh, còn axit HNO3 dù là axit đặc hay loãng đề có tính oxi hoá mạnh khi tác dụng với các chất có tính khử.
+ H2SO4 loãng không tác dụng được với các kim loại đứng sau hiđro trong dãy hoạt động hoá học như axit HNO3.
Fe + H2SO4 (loãng) → FeSO4 + H2↑
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
- Những tính chất chung:
+Với axit H2SO4 loãng và HNO3 đều có tính axit mạnh
Thí dụ:
Đổi màu chất chỉ thị: Quỳ tím chuyển thành màu đỏ
Tác dụng với bazơ, oxit bazơ không có tính khử.
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3+ 6H2O
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2↑
H2SO4 + Na2SO3 → Na2SO4 + H2O + SO2↑
+ Với axit H2SO4(đặc) và axit HNO3 đều có tính oxi hoá mạnh
Thí dụ:
Tác dụng được với hầu hết các kim loại (kể cả kim loại đứng sau hiđro trong dãy hoạt động hoá học) và đưa kim loại lên số oxi hoá cao nhất.
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Cu + 2H2SO4(đặc) → CuSO4 + SO2↑ + 2H2O
Tác dụng với một số phi kim (đưa phi kim lên số oxi hoá cao nhất)
C + 2H2SO4(đặc) → CO2↑ + 2SO2↑ + 2H2O
S + 2HNO3 → H2SO4 + 2NO↑
Tác dụng với hợp chất( có tính khử)
3FeO + 10HNO3 → 3Fe(NO3)3 + NO↑ + 5H2O
2FeO + 4H2SO4(đặc) → Fe2(SO4)3 + SO2↑ + 4H2O
Cả hai axit khi làm đặc nguội đều làm Fe và Al bị thụ động hoá (có thể dùng bình làm bằng nhôm và sắt để đựng axit nitric và axit sunfuaric đặc)
Lời giải:
a) Đáp án D
Phương trình của phản ứng nhiệt phân
4Fe(NO3)3 t°→t°→ 2Fe2O3 + 12NO2 + 3O2
Tổng các hệ số = 4 + 2 + 12 + 3 = 21
b) Đáp án A
Phương trình của phản ứng nhiệt phân
Hg(NO3)2 → Hg + 2NO2 ↑ + O2 ↑
Tổng các hệ số = 1 + 1 + 2 + 1 = 5
Lưu ý: Phản ứng nhiệt phân muối nitrat
- Các muối nitrat của kim loại hoạt động mạnh (K, Na…) bị phân hủy tạo muối nitrit
(NO2−NO2−) và O2
- Các muối nitrat của kim loại Mg, Zn, Fe, Cu, Pb…. Bị phân hủy tạo oxit kim loại tương ứng, NO2 và O2
- Muối nitrat của Ag, Au, Hg… bị phân hủy tạo thành kim loại tương ứng, NO2 và O2
Bài 5 trang 45 Hóa 11: Viết phương trình hóa học của phản ứng thực hiện dãy chuyển hóa sau:
NO2 (1)→(1)→ HNO3 (2)→(2)→Cu(NO3)2
(3)→(3)→Cu(OH)2 (4)→(4)→Cu(NO3)2
(5)→(5)→CuO (6)→(6)→ Cu (7)→(7)→ CuCl2
Lời giải:
(1) 4NO2 + O2 + 2H2O → 4HNO3
(2) 8HNO3 + 3Cu → 3Cu(NO3)2 + 2NO↑ + 4H2O
Hoặc CuO + 2HNO3 → Cu(NO3)2 + H2O
(3) Cu(NO3)2 + 2NaOH → Cu(OH)2↓ + 2NaNO3
(4) Cu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O
(5) 2Cu(NO3)2 → 2CuO + 4NO2↑ + O2↑
(6) CuO + H2 t°→t°→ Cu + H2O
(7) Cu + Cl2 t°→t°→ CuCl2
Lời giải:
nHNO3nHNO3 = 1,5. 1,00 = 1,50 (mol)
nNO = 6,72 : 22,4 = 0,3(mol)
Phương trình phản ứng:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo phương trình (1) nCu = 3232 .nNO
= 3232.0,3 = 0,45 mol
Gọi nCuO = x mol
Ta có: mhỗn hợp = mCu + mCuO
= 0,45.64 + 80x = 30,00 gam
→ x = 0,015 → nCuO = 0,015 mol
→ mCuO = 0,015. 80 = 1,2 g
%CuO = .100 = 4%
Theo phương trình (1)
nCu(NO3)2nCu(NO3)2 = nCu = 0,45 mol
Theo phương trình (2)
nCu(NO3)2nCu(NO3)2 = nCuO = 0,015 mol
Tổng nCu(NO3)2nCu(NO3)2 = 0,45 + 0,015
= 0,465 mol
→CM Cu(NO3)2CMCu(NO3)2 = 0,6451,50,6451,5 = 0,31M
Theo phương trình (1) nHNO3nHNO3 = 4. nNO
= 4. 0,3 = 1,2 mol
Theo phương trình (2) nHNO3nHNO3 = 2. nCuO
= 2. 0,015 = 0,03 mol
nHNO3nHNO3 (dư) = 1,5 - 1,2 – 0,03 = 0,27 mol
→CM HNO3=0,271,5=0,18MCMHNO3=0,271,5=0,18M
Lời giải:
Khối lượng HNO3 nguyên chất là:
5.60100=35.60100=3tấn
Sơ đồ phản ứng điều chế HNO3 từ NH3
NH3→NO→NO2→HNO31 mol1 mol17g 63gx tan 3 tan
Theo sơ đồ điều chế nHNO3=nNH3
→ mHNO3=3.1763 = 0,809524 tấn
Khối lượng NH3 hao hụt là 3,8% nghĩa là hiệu suất đạt
100 - 3,8 = 96,2%
Vậy khối lượng amoniac cần dùng là:
0,8095240,962= 0,8415 tấn
Bài giảng Hóa 11 Bài 9: Axit nitric và muối nitrat
Xem thêm lời giải bài tập Hóa học lớp 11 hay, chi tiết khác:
Bài 11: Axit photphoric và muối photphat
Bài 13: Luyện tập tính chất của nitơ, photpho và các hợp chất của chúng
Bài 14: Bài thực hành 2. Tính chất của một số hợp chất nitơ, photpho
Xem thêm tài liệu Hóa học lớp 11 hay, chi tiết khác:
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
