Hệ thống kiến thức Hóa học lớp 8 Giữa học kì 1
Hệ thống kiến thức Hóa học lớp 8 Giữa học kì 1 chi tiết giúp học sinh ôn luyện để đạt điểm cao trong bài thi Hóa học 8 Giữa học kì 1. Mời các bạn cùng đón xem:
[Năm 2023] Hệ thống kiến thức Hóa học lớp 8 Giữa học kì 1
CHƯƠNG 1: CHẤT, NGUYÊN TỬ, PHÂN TỬ
I. CHẤT
1. Vật thể và chất:
- Chất là những thứ tạo nên vật thể
- Vật thể:
+ Vật thể tự nhiên: cây, đất đá, quả chuối…
+ Vật thể nhân tạo: con dao, quyển vở…
2. Tính chất của chất:
- Mỗi chất đều có những tính chất đặc trưng( tính chất riêng).
- Tính chất của chất:
+ Tính chất vật lý: màu, mùi, vị, khối lượng riêng, tó, tonc, trạng thái
+ Tính chất hóa học: sự biến đổi chất này thành chất khác
3. Hỗn hợp:Hỗn hợp: là gồm nhiều chất trộn lẫn với nhau: không khí, nước sông…
+ Tính chất của hỗn hợp thay đổi.
+ Tính chất của mỗi chất trong hỗn hợp là không thay đổi.
+ Muốn tách riêng từng chất ra khỏi hỗn hợp phải dựa vào tính chất đặc trưng khác nhau của các chất trong hỗn hợp.
Chất tinh khiết: là chất không có lẫn chất khác: nước cất…
II. NGUYÊN TỬ:
1. Nguyên tử: Là hạt vô cùng nhỏ và trung hòa về điện.
Nguyên tử:
+ Nhân gồm có proton và notron
+ Vỏ: các hạt eclectron
|
Electron(e) |
Proton (p) |
Notron (n) |
|
me = 9,1095.10-31Kg qe = -1,602. 10-19 C qe = 1- |
mp = 1,6726.10-27 Kg = 1đvC qp = +1,602 . 10-19C qp = 1+ qp = qe 1 |
mn = 1,6748. 10-27 Kg = 1 đvC qn = 0
|
=> mp = mn = 1 đvC , => p = e
- Vì me rất nhỏ(không đáng kể) nên mnt tập trung hầu hết ở hạt nhân nguyên tử khối lượng hạt nhân nguyên tử được coi là khối lượng nguyên tử.
- p + e + n = tổng số hạt nguyên tử
2. Lớp electron trong nguyên tử:
a) Trong nguyên tử electron chuyển động rất nhanh xung quanh hạt nhân và sắp xếp thành từng lớp
b) Mô hình cấu tạo nguyên tử 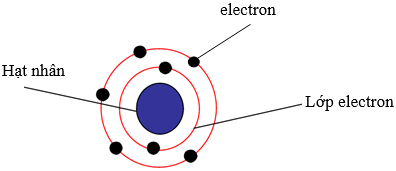
III. NGUYÊN TỐ HÓA HỌC:
1. Định nghĩa: NTHH là tập hợp những nguyên tử cùng loại, có cùng số proton trong hạt nhân.
2. Kí hiệu hóa học:
- Kí hiệu hóa học: thường lấy chữ cái đầu (in hoa) tên Latinh, trường hợp nhiều nguyên tố có chữ cái đầu giống nhau thì KHHH của chúng có thêm chữ thứ hai (viết thường).( tr.42)
- Ví dụ: Cacbon: C, Canxi: Ca, Đồng: Cu
- Ý nghĩa của KHHH: Chỉ NTHH đã cho, chỉ một nguyên tử của nguyên tố đó.
- Ví dụ: 2O: Hai nguyên tử Oxi.
3. Nguyên tử khối
- NTK: Là khối lượng của một nguyên tử tính bằng đơn vị Cacbon (đvC)
1đvC = khối lượng của một nguyên tử Cacbon
1đvC = . 1,9926.10-23 = 1,6605.10-24g = 1,6605.10-27 kg
- Ví dụ: NTK C = 12đvC, O = 16 đvC
4. Phân tử: Là hạt đại diện cho chất, gồm một số nguyên tử liên kết với nhau và thể hiện đầy đủ tính chất hóa học của chất.
5. Phân tử khối: Là khối lượng của phân tử tính bằng đơn vị cacbon, bằng tổng nguyên tử NTK của các nguyên tử trong phân tử.
VD: PTK của H2O= 1.2+16 = 18 đvC
IV. ĐƠN CHẤT – HỢP CHẤT:
1. Đơn chất:
Là những chất được tạo nên từ một NTHH.

2. Hợp chất:
Là những chất được tạo nên từ 2 hay nhiều NTHH (H2O, NaCl, H2SO4)
V. CÔNG THỨC HÓA HỌC:
1. Ý nghĩa của CTHH:
- Những nguyên tố nào tạo thành chất.
- Số nguyên tử của mỗi nguyên tố tạo thành một phân tử chất.
- Phân tử khối của chất.
2. CTHH của đơn chất:
- Kim loại(A): Al, Fe, Cu…
Phi kim:
+ X2: O2, N2, H2…
+ X: S, C, P
3. CTHH của hợp chất: gồm KHHH của những nguyên tố tạo thành phân tử hợp chất, có ghi chỉ số ở chân kí hiệu. (VD: H2O, NaCl, H2SO4) AxBy…
4. CTHH của hợp chất: gồm KHHH của những nguyên tố tạo thành phân tử hợp
chất, có ghi chỉ số ở chân kí hiệu. (VD: H2O, NaCl, H2SO4) AxBy…
VI. HÓA TRỊ:
1. Khái niệm: Hóa trị của một nguyên tố(nhóm nguyên tử) là con số biểu thị khả năng liên kết của nguyên tử nguyên tố đó với nguyên tử nguyên tố khác.( Bảng 1 tr.42).
- Hóa trị được ghi bằng chữ số La Mã và được xác định theo hóa trị của H bằng I. Hóa trị của O bằng II.
- Ví dụ: HCl thì( Cl:I ), NH3 thì( N:III ), K2O thì( K: I ), Al2O3 thì( Al: III ).
1. Quy tắc hóa trị:
Ta có: a.x = b.y hay
2. Áp dụng QTHT:
- Tính hóa trị của một nguyên tố:
+ Ví dụ: Tính hóa trị của Al trong hợp chất Al2O3
Gọi hóa trị của Al là a.
Ta có: => a.2 = II.3 => a=3. Vậy Al (III)
- Lập CTHH của hợp chất theo hóa trị:
- Lập CTHH của sắt oxit, biết Fe(III).
- Lập CTHH của hợp chất gồm Na(I) và SO4(II).
CHƯƠNG 2: PHẢN ỨNG HÓA HỌC
I. SỰ BIẾN ĐỔI CHẤT
1. Hiện tượng vật lí: là hiện tượng chất bị biến đổi về hình dạng hoặc bị biến đổi về trạng thái (rắn, lỏng, khí) nhưng bản chất của chất vẫn không thay đổi (không có sự tạo thành chất mới).
Ví dụ: chặt dây thép thành những đoạn nhỏ, tán thành đinh
2. Hiện tượng hóa học: là hiện tượng có sự biến đổi chất này thành chất khác, nghĩa là có sinh ra chất mới.
Ví dụ: đốt cháy than (cacbon) tạo ra khí cacbonic
II. PHẢN ỨNG HÓA HỌC
- Phản ứng hóa học là quá trình biến đổi chất này (chất phản ứng) thành chất khác (sản phẩm phản ứng)
- Trong phản ứng hóa học, các nguyên tử được bảo toàn, chỉ liên kết giữa các ng.tử bị thay đổi, làm phân tử chất này biến thành phân tử chất khác
Ví dụ: phản ứng xảy ra khi nung vôi: CaCO3 CaO + CO2
Trong đó: Chất pứ: CaCO3
Chất sản phẩm: CaO, CO2
- Dấu hiệu nhận biết có pứ xảy ra: có chất mới tạo thành có tính chất khác với chất pứ (màu, mùi, vị, tỏa nhiệt, phát sáng…)
III. ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG
1. ĐLBTKL: trong một phản ứng hóa học, tổng khối lượng của các chất sp bằng tổng khối lượng của các chất pứ
Áp dụng: A + B → C + D
mA + mB = mC + mD
IV. PHƯƠNG TRÌNH HÓA HỌC:
Phương trình hóa học là sự biểu diễn phản ứng hóa học bằng công thức hóa học
Ví dụ: Phản ứng sắt tác dụng với oxi:
3Fe + 2O2Fe3O4
- Các bước lập PTHH:
+ B1: Viết sơ đồ của pứ: Al + O2 -----> Al2O3
+ B2: Cân bằng số nguyên tử của mỗi nguyên tố: Al + O2-----> 2Al2O3
+ B3: Viết PTHH: 4Al + 3O2 2Al2O3
Đề thi Hoá học lớp 8 Giữa học kì 1 năm 2022-2023 có đáp án
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 8
Thời gian làm bài: 45 phút
(Đề số 1)
Phần I. Trắc nghiệm
Câu 1: Phân tử khối của hợp chất H2SO4 là:
A. 98
B. 97
C. 49
D. 100
Câu 2: Để chỉ 2 phân tử hiđro ta viết:
A. 2H
B. 2H2
C. 4H
D. 4H2
Câu 3: Hợp chất Alx(SO4)3 có phân tử khối là 342. Giá trị của x là:
A. 3
B. 1
C. 2
D. 4
Câu 4: Trong các dãy sau, dãy nào toàn là hợp chất.
A. CH4, K2SO4, Cl2, O2, NH3
B. O2, CO2, CaO, N2, H2O
C. H2O, Ca(HCO3)2, Fe(OH)3, CuSO4
D. HBr, Br2, HNO3, NH3, CO2
Câu 5: Hạt nào trong nguyên tử mang điện tích dương:
A. Nơtron
B. Proton
C. Electron
D. Electron và Nơtron
Câu 6: Cho các chất sau: nước chanh, đường, nước mắm, sữa tươi, muối tinh, nước cất, khí oxi, không khí. Số chất tinh khiết là:
A. 2
B. 3
C. 5
D. 4
Câu 7: Công thức hóa học sau đây là công thức của đơn chất:
A. N2
B. N2O5
C. NO
D. NO2.
Câu 8: Công thức hóa học của muối Kali penmanganat (biết trong phân tử có 1K, 1Mn, 4O) là:
A. K2MnO4
B. KMnO4
C. KO4Mn
D. MnKO4.
Phần II. Tự luận
Câu 1: Lập công thức hóa học tạo bởi các thành phần cấu tạo sau, rồi tính phân tử khối của các hợp chất đó:
a. Natri(I) và nhóm sunfat : SO4(II)
b. Nhôm (III) và Cl
Câu 2: Phân tử của một hợp chất gồm nguyên tử nguyên tố X liên kết với 2 nguyên tử nguyên tố Oxi nặng 44 đ.v.C.
a. Tính nguyên tử khối, cho biết tên kí hiệu của X.
b. Tính % khối lượng của nguyên tố X trong hợp chất.
Câu 3. Một oxit có công thức Mn2Ox có phân tử khối là 222. Tìm hoá trị của Mn?
(Biết Mn = 55; O = 16; C = 12; Na = 23; S = 32; O = 16; Al = 27; Cl = 35,5)
ĐÁP ÁN ĐỀ 1
Phần I. Trắc nghiệm
Câu 1: A
Phân tử khối của hợp chất H2SO4 là: 2+32+16.4=98 đv
Câu 2: B
Câu 3: C
Hợp chất Alx(SO4)3 có phân tử khối là 342
27.x + 3(32+16.4) = 342 nên x = 2
Câu 4: C
Dãy toàn là hợp chất H2O, Ca(HCO3)2, Fe(OH)3, CuSO4
Câu 5: B
Câu 6: D
Trong các chất: nước chanh, đường, nước mắm, sữa tươi, muối tinh, nước cất, khí oxi, không khí. Số chất tinh khiết là: đường, muối tinh, nước cất, khí oxi
Câu 7: A
Công thức hóa học là công thức của đơn chất:N2
Câu 8: B
Công thức hóa học của muối Kali penmanganat (biết trong phân tử có 1K, 1Mn, 4O) là: KMnO4
Phần II: Tự luận
Câu 1:
a. Nax(SO4)y: I. x= II. y nên x=2 , y =1
Ta được công thức : Na2SO4
PTK = 23.2+32+16.4= 142 đvC
b. Nhôm (III) và Cl(I) nên CTHH là AlCl3
PTK = 27+35,5.3= 133,5 đvC
Câu 2:
a. XO2 có PTK = 44 nên X + 32 = 44
X = 12 Ký hiệu của X là: C
b. % khối lượng của C trong hợp chất là:
(12:44) . 100% = 27,27 %
Câu 3:
Mn2Ox có phân tử khối là 222 nên 55.2+16.x =222
Vậy x = 7
Vậy CTHH Mn2O7 .Gọi hóa trị Mn là x, có: x.2 =II.7 nên x= VII
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Học kì 1
Năm học 2022 - 2023
Môn: Hóa học 8
Thời gian làm bài: 45 phút
(Đề số 2)
Phần I. Trắc nghiệm
Câu 1: Chọn đáp án sai
A. Khối lượng của hạt nhân được coi là khối lượng của nguyên tử
B. Số p = số e
C. Hạt nhân tạo bởi proton và notron
D. Oxi có số p khác số e
Câu 2: Khí đinito pentaoxit có công thức hoá học là N2O5, hãy cho biết trong CTHH đã cho nguyên tố nito có hóa trị mấy?
A. II
B. III
C. IV
D. V.
Câu 3: Phân tử khối của Sắt (II) sunfat FeSO4 là
A. 151 đvC
B. 152 đvC
C. 162 đvC
D. 153 đvC
Câu 4:. 7Cl có ý nghĩa gì?
A. 7 chất Clo
B. 7 nguyên tố Clo
C. 7 nguyên tử Clo
D. 7 phân tử Clo
Câu 5: Nguyên tử khối của Cu gấp mấy lần phân tử khối khí hidro
A. 4 lần
B. 2 lần
C. 32 lần
D. 62 lần
Câu 6: Từ công thức hóa học của CuSO4 có thể suy ra được những gì
A. CuSO4 do 3 nguyên tố Cu, O, S tạo nên
B. Có 3 nguyên tử oxi trong phân tử
C. Phân tử khối là 96 đvC
D. Tất cả đáp án
Câu 7: Công thức hóa học đúng
A. Kali Clorua KCl2
B. Canxi cacbua CaC4
C. Cacbon đioxit C2O2
D. Khí metan CH4
Câu 8: Cho biết CTHH hợp chất của nguyên tố X với Cl là XCl2, hợp chất của Y với O là Y2O3. Vậy CTHH của hợp chất của X và Y là:
A. X2Y3.
B. XY2.
C. X3Y2.
D. X2Y.
Phần II. Tự luận
Câu 1: Viết công thức hóa học và tính phân tử khối của các hợp chất sau:
a. Axit photphoric có phân tử gồm 3H, 1P, 4O liên kết với nhau
b. Đường sacarozo có phân tử gồm 12C, 22H và 11O liên kết với nhau.
Câu 2: Lập công thức hóa học và tính phân tử khối của các hợp chất tạo bởi một nguyên tố và nhóm nguyên tử sau: Fe (III) và nhóm (SO4).
Câu 3:
a. Tính hoá trị của Fe và N trong các hợp chất sau: Fe2O3; NH3.
b. Tính hoá trị của Cu trong hợp chất: Cu(NO3)2 biết nhóm NO3 có hoá trị I.
ĐÁP ÁN ĐỀ 2
Phần I. Trắc nghiệm
Câu 1: D
Đáp án sai Oxi có số p khác số e
Sửa : oxi có số p bằng số e
Câu 2: D
Trong CTHH N2O5 đã cho nguyên tố nito có hóa trị x, ta có
2. x = 5. II nên x = V
Câu 3: B
Phân tử khối của Sắt (II) sunfat FeSO4 là : 56+32+16.4=152 đvC
Câu 4: C
Câu 5: C
Nguyên tử khối Cu (M =64)
Phân tử khối khí H2 (M=2)
Nguyên tử khối của Cu gấp 32 lần phân tử khối khí hidro
Câu 6: A
Câu 7: D
Câu 8:C
CTHH hợp chất của nguyên tố X với Cl là XCl2 nên X hóa trị II
hợp chất của Y với O là Y2O3 nên Y háo trị III
Vậy CTHH của hợp chất của X và Y là X3Y2
Phần II. Tự luận
Câu 1:
a) H3PO4
Phân tử khối của H3PO4 = 3.1 + 31 + 16.4 = 98 đvC
b) C12H22O11
Phân tử khối của C12H22O11 = 12.12 + 22 + 16.11 = 342 đvC
Câu 2:
Công thức hóa học của hợp chất có dạng:
Ta có: x.III = y.II => x/y = II/III = 2/3 => x = 2; y = 3
Công thức hóa học của hợp chất là Fe2(SO4)3
Phân tử khối = 2.56 + 32.3 + 16.4.3 = 400 đvC
Câu 3:
a) Gọi hóa trị Fe trong Fe2O3 là x, có:
2.x= 3.II nên x=III
Gọi hóa trị của N trong các hợp chất NH3 là y, có
y.1= 3.I nên y = III
b) Gọi hoá trị của Cu trong hợp chất: Cu(NO3)2 là a, có
a. 1= I.2 nên a = II
Xem thêm các bộ đề thi Hoá học 8 chọn lọc, hay khác:
TOP 30 Đề thi Học kì 1 Hoá học lớp 8 năm 2023 có đáp án
Đề cương Học kì 1 Hoá học lớp 8 năm 2023 chi tiết nhất
Bài tập Hóa học lớp 8 Học kì 1 có đáp án
