Sách bài tập KHTN 9 Bài 19 (Chân trời sáng tạo): Sự khác nhau cơ bản giữa phi kim và kim loại
Với giải sách bài tập Khoa học tự nhiên 9 Bài 19: Sự khác nhau cơ bản giữa phi kim và kim loại sách Chân trời sáng tạo hay nhất, ngắn gọn sẽ giúp học sinh dễ dàng làm bài tập trong SBT KHTN 9 Bài 19.
Giải SBT KHTN 9 Bài 19: Sự khác nhau cơ bản giữa phi kim và kim loại
Nội dung đang được cập nhật...
Lý thuyết KHTN 9 Bài 19: Sự khác nhau cơ bản giữa phi kim và kim loại
1. Ứng dụng của một số đơn chất phi kim
a. Ứng dụng của carbon
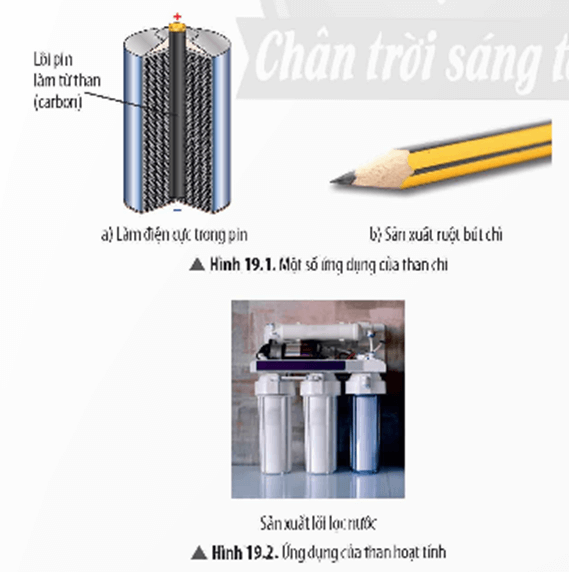
- Than (thành phần chính là carbon) là một trong những nguồn nhiên liệu cung cấp năng lượng cho hoạt động công nghiệp và đời sống của con người.
- Ngoài ra, carbon dùng làm điện cực, ruột bút chì, lõi lọc nước,…
b. Ứng dụng của lưu huỳnh (sulfur)
Lưu huỳnh dùng làm nguyên liệu sản xuất sulfuric acid, lưu hoá cao su,…
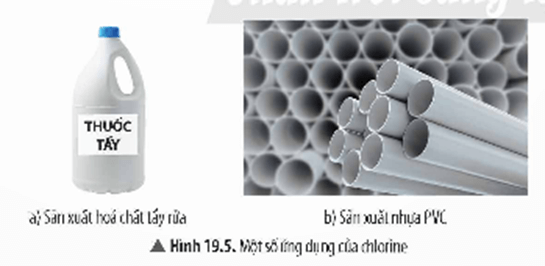
c. Ứng dụng của chlorine
Cholorine dùng để sản xuất hoá chất tẩy rửa, nhựa PVC,…
2. Sự khác nhau về một số tính chất giữa phi kim và kim loại
Các nguyên tố kim loại và phi kim có sự khác nhau ở một số tính chất (vật lí và hoá học). Dựa vào những tính chất khác biệt đó, người ta sẽ nghiên cứu, chế tạo thiết bị, vật dụng phù hợp để đáp ứng với nhu cầu cuộc sống, sản xuất.
* Sự khác nhau về tính chất vật lí
|
Kim loại |
Phi kim |
|
|
Tính dẫn điện, dẫn nhiệt |
- Dẫn điện, dẫn nhiệt tốt. |
- Thường không dẫn điện, dẫn nhiệt kém. |
|
Nhiệt độ nóng chảy, nhiệt độ sôi |
- Thường có nhiệt độ nóng chảy, nhiệt độ sôi cao. - Kim loại hầu hết ở trạng thái rắn (trừ thủy ngân ở trạng thái lỏng). |
- Thường có nhiệt độ nóng chảy, nhiệt độ sôi thấp. - Ở điều kiện thường phi kim tồn tại ở cả ba thể: rắn (C, S, …), lỏng (Br2), khí (Cl2, O2, …). |
|
Khối lượng riêng |
- Có khối lượng riêng lớn. |
- Có khối lượng riêng nhỏ. |
*Sự khác nhau về tính chất hóa học
|
Kim loại |
Phi kim |
|
|
Khả năng tạo ion |
- Có xu hướng nhường electron để tạo thành ion dương khi tham gia các phản ứng hóa học. VD: Na → Na+ + 1e Mg → Mg2+ + 2e Al → Al3+ + 3e |
- Có xu hướng nhận electron để tạo thành ion âm khi tham gia các phản ứng hóa học. VD: Cl + 1e → Cl- S + 2e → S2- N + 3e → N3- |
|
Phản ứng với oxygen |
- Kim loại phản ứng với oxygen thường tạo thành oxide base. VD: 2Mg + O2 2MgO 3Fe + 2O2 Fe3O4 |
- Phi kim phản ứng với oxygen thường tạo thành oxide acid. VD: C + O2 CO2 S + O2 SO2 |
Xem thêm các chương trình khác:
- Soạn văn 9 Chân trời sáng tạo (hay nhất)
- Văn mẫu 9 - Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn 9 – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn 9 - Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn 9 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn 9 – Chân trời sáng tạo
- Soạn văn 9 Chân trời sáng tạo (ngắn nhất)
- Giải sgk Toán 9 – Chân trời sáng tạo
- Lý thuyết Toán 9 – Chân trời sáng tạo
- Giải sbt Toán 9 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 9 - Friends plus
- Trọn bộ Từ vựng Tiếng Anh lớp 9 Friends plus đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 9 Friends plus đầy đủ nhất
- Giải sbt Tiếng Anh 9 – Friends plus
- Giải sgk Lịch sử 9 – Chân trời sáng tạo
- Giải sbt Lịch sử 9 – Chân trời sáng tạo
- Giải sgk Địa lí 9 – Chân trời sáng tạo
- Giải sbt Địa lí 9 – Chân trời sáng tạo
- Giải sgk Tin học 9 – Chân trời sáng tạo
- Giải sbt Tin học 9 – Chân trời sáng tạo
- Giải sgk Công nghệ 9 – Chân trời sáng tạo
- Giải sgk Giáo dục công dân 9 – Chân trời sáng tạo
- Giải sbt Giáo dục công dân 9 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 9 – Chân trời sáng tạo