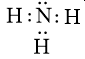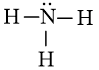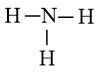Giải Hóa 10 Bài 12 (Kết nối tri thức): Liên kết cộng hóa trị
Với giải bài tập Hóa 10 Bài 12: Liên kết cộng hóa trị sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 10 Bài 12.
Giải bài tập Hóa lớp 10 Bài 12: Liên kết cộng hóa trị
Video giải bài tập Hóa lớp 10 Bài 12: Liên kết cộng hóa trị
Lời giải:
Nguyên tử hydrogen liên kết với nguyên tử chlorine bằng cách mỗi nguyên tử góp 1 electron tạo thành 1 cặp electron dùng chung trong phân tử HCl. Khi đó nguyên tử hydrogen có 2 electron (cấu hình electron bền vững của nguyên tử khí hiếm He) và nguyên tử chlorine có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

Khác với phân tử sodium chloride (NaCl) được hình thành nhờ lực hút tĩnh điện giữa các ion trái dấu Na+ và Cl-. Các ion này được tạo ra do sự nhường, nhận electron.

I. Sự tạo thành liên kết cộng hóa trị
Hoạt động trang 58 Hóa học 10: Lắp ráp mô hình một số phân tử
Chuẩn bị: Bộ lắp ráp mô hình các phân tử CH4, C2H4, C2H2, C2H5OH, CH3COOH.
- Chọn hình cầu có màu sắc khác nhau đại diện cho nguyên tử C, O, H.
- Lắp các hình cầu và que nối theo mẫu (Hình 12.8).
Quan sát mô hình và cho biết số liên kết đơn, liên kết đôi, liên kết ba trong mỗi phân tử.
Lời giải:
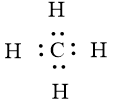
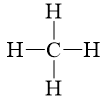
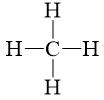
- Trong phân tử methane (CH4): có 4 liên kết đơn C-H
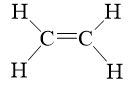
- Trong phân tử ethene (C2H4): có 4 liên kết đơn C-H và 1 liên kết đôi C=C
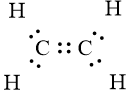
- Trong phân tử ethyne (C2H2): có 2 liên đơn C-H và 1 liên kết ba C≡C
- Trong phân tử ethanol (C2H5OH): có tất cả 8 liên kết đơn (trong đó: 5 liên kết đơn C-H, 1 liên kết đơn C-C, 1 liên kết đơn C-O và 1 liên kết đơn O-H).
- Trong phân tử ethanoic acid (CH3COOH): có 1 liên kết đôi C=O và 6 liên kết đơn (trong đó: 3 liên kết đơn C-H, 1 liên kết đơn C-C, 1 liên kết đơn C-O và 1 liên kết đơn O-H.
a) Bromine (Br2). b) Hydrogen sulfide (H2S).
c) Methane (CH4). d) Ammonia (NH3).
e) Ethene (C2H4). g) Ethyne (C2H2).
Lời giải:
|
|
Công thức electron |
Công thức Lewis |
Công thức cấu tạo |
|
a) Bromine (Br2). |
|
|
Br – Br |
|
b) Hydrogen sulfide (H2S). |
|
|
H – S – H |
|
c) Methane (CH4). |
|
|
|
|
d) Ammonia (NH3). |
|
|
|
|
e) Ethene (C2H4). |
|
|
|
|
g) Ethyne (C2H2). |
|
|
|
II. Độ âm điện và liên kết hóa học
Lời giải:
- Trong phân tử MgCl2, hiệu độ âm điện của Cl và Mg: 3,16 – 1,31 = 1,85.
⇒ Liên kết giữa Mg và Cl là liên kết ion.
- Trong phân tử AlCl3, hiệu độ âm điện của Cl và Al: 3,16 – 1,61 = 1,55.
⇒ Liên kết giữa Al và Cl là liên kết cộng hóa trị phân cực.
- Trong phân tử HBr, hiệu độ âm điện của Br và H: 2,96 – 2,2 = 0,76.
⇒ Liên kết giữa Br và H là liên kết cộng hóa trị phân cực.
- Trong phân tử O2, hiệu độ âm điện: 3,44 – 3,44 = 0.
⇒ Liên kết giữa O và O là liên kết cộng hóa trị không phân cực.
- Trong phân tử H2, hiệu độ âm điện: 2,2 – 2,2 = 0.
⇒ Liên kết giữa H và H là liên kết cộng hóa trị không phân cực.
- Trong phân tử NH3, hiệu độ âm điện của N và H: 3,04 – 2,2 = 0,84.
⇒ Liên kết giữa N và H là liên kết cộng hóa trị phân cực.
III. Mô tả liên kết cộng hóa trị bằng sự xen phủ orbital nguyên tử
Câu hỏi 3 trang 61 Hóa học 10: Sự hình thành liên kết σ và liên kết π khác nhau như thế nào?
Lời giải:
- Sự xen phủ trục, tạo ra liên kết σ. Xen phủ trục là các orbital sẽ xen phủ với nhau theo trục liên kết. Có ba loại xen phủ trục:
+ Sự xen phủ s – s
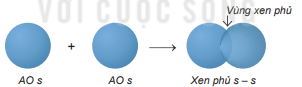
+ Sự xen phủ s – p
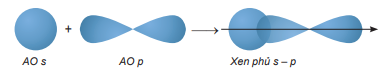
+ Sự xen phủ p – p

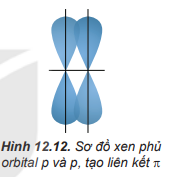
- Sự xen phủ bên tạo ra liên kết π. Sự xen phủ bên là sự xen phủ, trong đó các orbital tham gia liên kết song song với nhau và vuông góc với đường nối tâm của hai nguyên tử liên kết.
Câu hỏi 4 trang 61 Hóa học 10: Số liên kết σ và π có trong phân tử C2H4 lần lượt là
Lời giải:
Đáp án đúng là: D
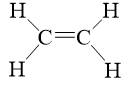
Trong phân tử C2H4 có 4 liên kết cộng hóa trị đơn (là 4 liên kết σ) và 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết π).
⇒ Trong phân tử C2H4 có 5 liên kết σ và 1 liên kết π.
IV. Năng lượng liên kết cộng hóa trị
Lời giải:
- Năng lượng liên kết (Eb) là năng lượng cần thiết để phá vỡ một liên kết hoá học trong phân tử ở thể khí thành các nguyên tử ở thể khí. Năng lượng liên kết đặc trưng cho độ bền của liên kết.
- Năng lượng liên kết của phân tử Cl2 là 243 kJ/mol cho biết: để phá vỡ 1 mol liên kết
Cl-Cl thành các nguyên tử Cl (ở thể khí) cần năng lượng là 243 kJ.
Lời giải:
Đáp án đúng là: C
Dựa vào Bảng 12.2, ta thấy:
Năng lượng liên kết Cl – Cl (243 kJ/mol) > năng lượng liên kết Br – Br (193 kJ/mol) > năng lượng liên kết I – I (151 kJ/mol).
⇒ Độ bền liên kết giảm từ Cl2 > Br2 > I2.
Lời giải:
Dựa vào hiệu độ âm điện của các nguyên tử, dự đoán loại liên kết:
0 ≤ || < 0,4: liên kết cộng hóa trị không phân cực
0,4 ≤ || < 1,7: liên kết cộng hóa trị phân cực.
|| ≥ 1,7: liên kết ion
Lý thuyết Liên kết cộng hóa trị
I. Sự tạo thành liên kết cộng hóa trị
Nguyên tử phi kim có xu hướng nhận thêm electron để đạt cấu hình electron bền vững của khí hiếm.
Khi hai nguyên tử phi kim kết hợp với nhau tạo thành phân tử, chúng sẽ góp chung một hoặc nhiều electron để tạo thành các cặp electron dùng chung. Các cặp electron dùng chung được tính cho cả hai nguyên tử trong phân tử nên mỗi nguyên tử đều đạt cấu hình bền vững theo quy tắc octet. Cặp electron dùng chung tạo ra liên kết cộng hóa trị giữa hai nguyên tử.
Cặp electron dùng chung giữa hai nguyên tử có thể được tạo thành theo hai kiểu khác nhau:
- Mỗi nguyên tử góp một hay nhiều electron để tạo thành các cặp electron dùng chung:
Ví dụ:
A× + ×B A : B hoặc A – B (liên kết A – B là liên kết cộng hóa trị).
- Cặp electron dùng chung chỉ do một nguyên tử đóng góp, liên kết giữa hai nguyên tử là liên kết cộng hóa trị kiểu cho – nhận.
Ví dụ:
Khi cặp electron dùng chung chỉ do nguyên tử B đóng góp, nguyên tử B là nguyên tử cho electron, nguyên tử A là nguyên tử nhận electron. Kí hiệu B A.
1. Sự tạo thành phân tử có liên kết đơn
- Phân tử chlorine (Cl2):
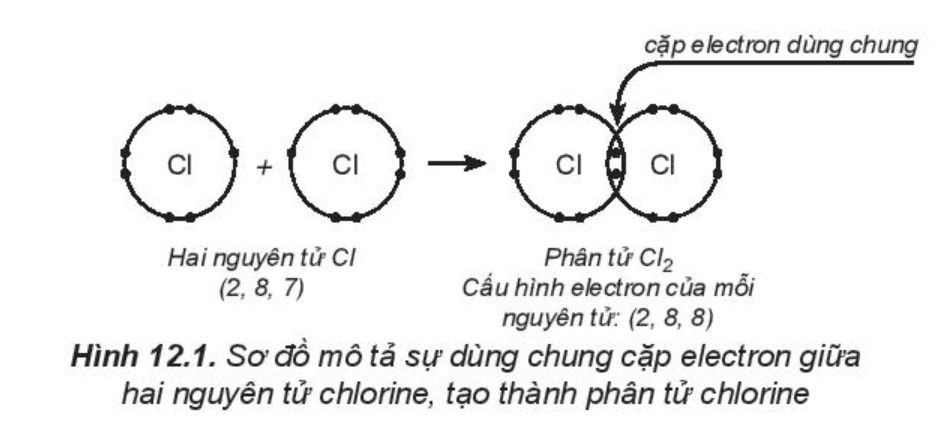
Cấu hình electron của nguyên tử Cl (Z = 17): [Ne]3s23p5 (có 7 electron hóa trị).
Hai nguyên tử chlorine liên kết với nhau bằng cách mỗi nguyên tử chlorine góp 1 electron, tạo thành 1 cặp electron dùng chung. Khi đó, trong phân tử Cl2, mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet:
Từ công thức electron, thay một cặp electron dùng chung bằng một gạch nối thì thu được công thức Lewis (Li-uýt):
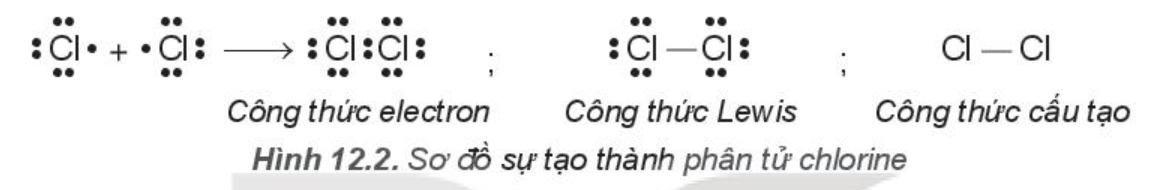
Giữa hai nguyên tử chlorine có một cặp electron dùng chung (biểu diễn bằng một gạch nối), đó là liên kết đơn.
- Phân tử hydrogen chloride (HCl):
Nguyên tử hydrogen liên kết với nguyên tử chlorine bằng cách mỗi nguyên tử góp 1 electron tạo thành 1 cặp electron dùng chung trong phân tử HCl. Khi đó nguyên tử hydrogen có 2 electron (cấu hình bền vững của nguyên tử khí hiếm helium) và nguyên tử chlorine có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

Giữa hai nguyên tử hydrogen và chlorine có một cặp electron dùng chung (biểu diễn bằng 1 gạch nối), đó là liên kết đơn.
- Phân tử hợp chất có liên kết cho – nhận:
Trong phân tử NH3, lớp ngoài cùng của nguyên tử nitrogen có 5 electron, trong đó có cặp electron chưa liên kết. Ion H+ có orbital trống, không có electron. Khi phân tử NH3 kết hợp với ion H+, nguyên tử nitrogen đóng góp cặp electron chưa liên kết để tạo liên kết với ion H+ tạo thành . Khi đó, liên kết cho – nhận được hình thành, nguyên tử nitrogen là nguyên tử cho, ion H+ là nguyên tử nhận. Trong ion , bốn liên kết N – H hoàn toàn tương đương nhau.
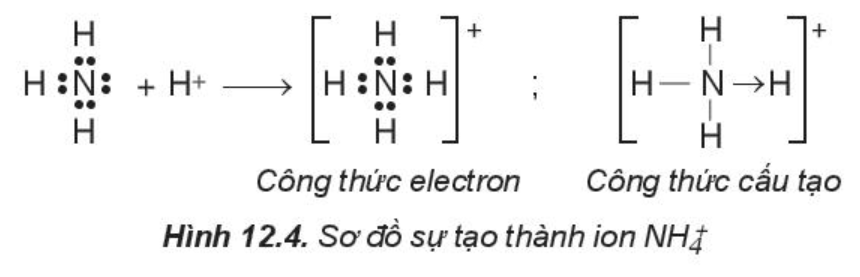 2. Sự tạo thành phân tử có liên kết đôi
2. Sự tạo thành phân tử có liên kết đôi
- Phân tử oxygen (O2):
Mỗi nguyên tử oxygen có 6 electron hóa trị, hai nguyên tử oxygen liên kết với nhau bằng cách mỗi nguyên tử đóng góp 2 electron, tạo thành 2 cặp electron dùng chung. Trong phân tử O2, mỗi nguyên tử oxygen đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

Giữa hai nguyên tử oxygen có hai cặp electron dùng chung (biểu diễn bằng hai gạch nối), đó là liên kết đôi.
- Phân tử carbon dioxide (CO2):
Nguyên tử carbon có 4 electron hóa trị, nguyên tử oxygen có 6 electron hóa trị. Hai nguyên tử oxygen liên kết với một nguyên tử carbon bằng cách mỗi nguyên tử oxygen đóng góp 2 electron và nguyên tử carbon đóng góp 4 electron tạo thành 4 cặp electron dùng chung. Khi đó, trong phân tử CO2, mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.
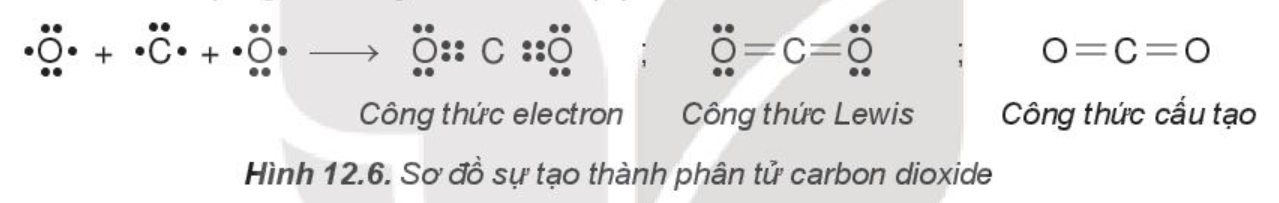 Phân tử CO2 có hai liên kết đôi.
Phân tử CO2 có hai liên kết đôi.
3. Sự tạo thành phân tử có liên kết ba
Phân tử nitrogen (N2):
Nguyên tử nitrogen có 5 electron hóa trị, hai nguyên tử nitrogen liên kết với nhau bằng cách mỗi nguyên tử nitrogen đóng góp 3 electron, tạo thành 3 cặp electron dùng chung. Khi đó, trong phân tử N2, mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

Giữa hai nguyên tử nitrogen có ba cặp electron dùng chung (biểu diễn bằng ba gạch nối), đó là liên kết ba.
Kết luận:
- Liên kết cộng hóa trị là liên kết được tạo thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung.
- Liên kết trong các phân tử Cl2, O2, N2, … có cặp electron dùng chung không bị hút lệch về phía nguyên tử nào được gọi là liên kết cộng hóa trị không phân cực.
- Liên kết trong phân tử HCl có cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn (Cl) được gọi là liên kết cộng hóa trị phân cực.
II. Độ âm điện và liên kết hóa học
Dựa vào sự khác nhau về độ âm điện giữa các nguyên tử tham gia liên kết, có thể dự đoán được loại liên kết giữa hai nguyên tử đó.

Ví dụ:
- Trong phân tử HCl, hiệu độ âm điện của Cl và H: 3,16 – 2,20 = 0,96.
Liên kết giữa H và Cl là liên kết cộng hóa trị phân cực.
- Trong phân tử CO2, hiệu độ âm điện của O và C: 3,44 – 2,55 = 0,89.
Liên kết giữa C và O là liên kết cộng hóa trị phân cực. Tuy nhiên, do phân tử CO2 có cấu tạo thẳng nên độ phân cực của hai liên kết đôi (C=O) triệt tiêu nhau, dẫn đến toàn bộ phân tử không bị phân cực.
- Trong phân tử NaCl, hiệu độ âm điện của Cl và Na: 3,16 – 0,93 = 2,23.
Liên kết giữa Na và Cl là liên kết ion.
Chú ý:
Liên kết cộng hóa trị phân cực có thể được coi là dạng trung gian giữa liên kết công hóa trị không phân cực và liên kết ion.
III. Mô tả liên kết cộng hóa trị bằng sự xen phủ các orbital nguyên tử
1. Sự xen phủ các orbital nguyên tử tạo liên kết s (sigma)
- Sự xen phủ s – s:
Phân tử H2 tạo thành từ hai nguyên tử H (1s1). Khi 2 nguyên tử H tiến lại gần nhau, hạt nhân của nguyên tử này hút đám mây electron của nguyên tử kia, hai orbital nguyên tử xen phủ vào nhau một phần. Vùng xen phủ có mật độ điện tích âm lớn, làm tăng lực hút của mỗi hạt nhân với vùng này và làm cân bằng lực đẩy giữa hai hạt nhân, để hai nguyên tử liên kết với nhau.
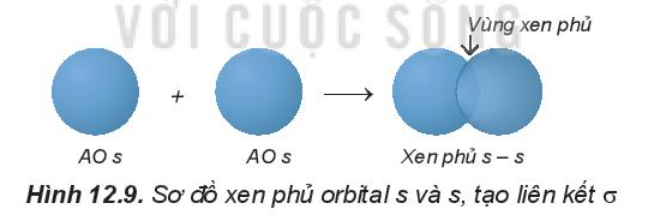
- Sự xen phủ s – p:
Phân tử HF tạo thành khi orbital 1s của nguyên tử H (1s1) xen phủ với orbital 2p của nguyên tử F (2s22p5) theo trục liên kết, tạo liên kết cộng hóa trị giữa H và F, vùng xen phủ càng lớn thì liên kết càng bền.
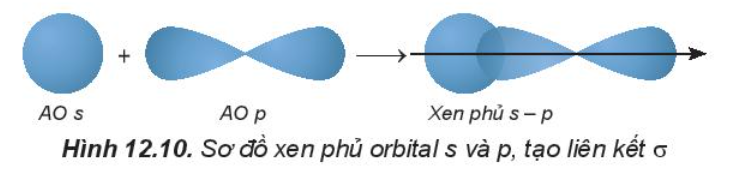 - Sự xen phủ p – p:
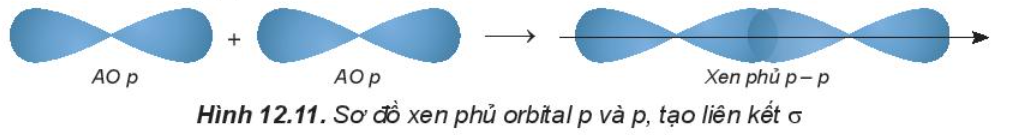
- Sự xen phủ p – p:
Phân tử Cl2 tạo thành khi hai orbital 3p của hai nguyên tử Cl (3s23p5) xen phủ theo trục liên kết của hai nguyên tử Cl.
 Nhận xét:
Nhận xét:
Các liên kết cộng hóa trị đơn đều là liên kết s. Trong liên kết s, mật độ xác suất tìm thấy electron lớn nhất dọc theo trục liên kết.
2. Sự xen phủ các orbital nguyên tử tạo liên kết p (pi)
Sự xen phủ, trong đó trục của các orbital tham gia liên kết song song với nhau và vuông góc với đường nối tâm của hai nguyên tử liên kết, được gọi là xen phủ bên. Sự xen phủ bên tạo ra liên kết p (pi).
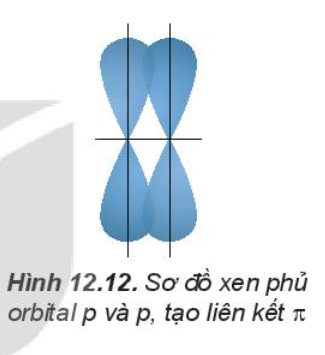 Liên kết đôi gồm một liên kết s và một liên kết p. Liên kết ba gồm một liên kết s và hai liên kết p.
Liên kết đôi gồm một liên kết s và một liên kết p. Liên kết ba gồm một liên kết s và hai liên kết p.
IV. Năng lượng liên kết cộng hóa trị
Năng lượng liên kết (Eb) là năng lượng cần thiết để phá vỡ một liên kết hóa học trong phân tử ở thể khí thành các nguyên tử ở thể khí. Năng lượng liên kết thường có đơn vị là kJ/mol.
Ví dụ: Để phá vỡ 1 mol liên kết H–Cl thành các nguyên tử H và Cl (ở thể khí) theo phương trình:
HCl(g) H(g) + Cl(g)
cần năng lượng là 432 kJ, nên năng lượng liên kết H–Cl là Eb = 432 kJ/mol.
Năng lượng liên kết đặc trưng cho độ bền của liên kết. Năng lượng liên kết càng lớn thì liên kết càng bền và phân tử càng khó bị phân hủy.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Bài 13: Liên kết hydrogen và tương tác Van der waals
Bài 15: Phản ứng oxi hóa – khử
Bài 17: Biến thiên enthalpy trong các phản ứng hóa học
Xem thêm tài liệu Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn lớp 10 – Kết nối tri thức
- Soạn văn lớp 10 (ngắn nhất) – Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn lớp 10 - KNTT
- Bố cục tác phẩm Ngữ văn lớp 10 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Kết nối tri thức
- Văn mẫu lớp 10 – Kết nối tri thức
- Giải Chuyên đề học tập Ngữ văn 10 – Kết nối tri thức
- Giải sgk Toán 10 – Kết nối tri thức
- Giải sbt Toán 10 – Kết nối tri thức
- Giải Chuyên đề Toán 10 – Kết nối tri thức
- Lý thuyết Toán 10 – Kết nối tri thức
- Chuyên đề dạy thêm Toán 10 Kết nối tri thức (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Global Success – Kết nối tri thức
- Giải sbt Tiếng Anh 10 Global Success – Kết nối tri thức
- Ngữ pháp Tiếng Anh 10 Global success
- Bài tập Tiếng Anh 10 Global success theo Unit có đáp án
- Trọn bộ Từ vựng Tiếng Anh 10 Global success đầy đủ nhất
- Giải sgk Vật lí 10 – Kết nối tri thức
- Giải sbt Vật lí 10 – Kết nối tri thức
- Giải Chuyên đề Vật lí 10 – Kết nối tri thức
- Lý thuyết Vật lí 10 – Kết nối tri thức
- Chuyên đề dạy thêm Vật lí 10 cả 3 sách (2024 có đáp án)
- Giải sgk Sinh học 10 – Kết nối tri thức
- Giải sbt Sinh học 10 – Kết nối tri thức
- Lý thuyết Sinh học 10 – Kết nối tri thức
- Giải Chuyên đề Sinh học 10 – Kết nối tri thức
- Giải sgk Lịch sử 10 – Kết nối tri thức
- Giải sbt Lịch sử 10 – Kết nối tri thức
- Giải Chuyên đề Lịch sử 10 – Kết nối tri thức
- Lý thuyết Lịch sử 10 - Kết nối tri thức
- Giải sgk Địa lí 10 – Kết nối tri thức
- Lý thuyết Địa Lí 10 – Kết nối tri thức
- Giải sbt Địa lí 10 – Kết nối tri thức
- Giải Chuyên đề Địa lí 10 – Kết nối tri thức
- Giải sgk Công nghệ 10 – Kết nối tri thức
- Lý thuyết Công nghệ 10 – Kết nối tri thức
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Kết nối tri thức
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Kết nối tri thức
- Giải Chuyên đề Kinh tế và pháp luật 10 – Kết nối tri thức
- Lý thuyết KTPL 10 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Kết nối tri thức
- Lý thuyết Giáo dục quốc phòng 10 – Kết nối tri thức
- Giải sbt Giáo dục quốc phòng 10 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 10 – Kết nối tri thức
- Giải sbt Hoạt động trải nghiệm 10 – Kết nối tri thức
- Giải sgk Tin học 10 – Kết nối tri thức
- Lý thuyết Tin học 10 – Kết nối tri thức
- Giải sbt Tin học 10 – Kết nối tri thức
- Giải Chuyên đề Tin học 10 – Kết nối tri thức
- Giải sgk Giáo dục thể chất 10 – Kết nối tri thức