Giải Hóa 10 Bài 10 (Kết nối tri thức): Quy tắc octet
Với giải bài tập Hóa 10 Bài 10: Quy tắc octet sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 10 Bài 10.
Giải bài tập Hóa lớp 10 Bài 10: Quy tắc octet
Video giải bài tập Hóa lớp 10 Bài 10: Quy tắc octet
Lời giải:
Yếu tố quyết định đến tỉ lệ số nguyên tử của mỗi nguyên tố trong phân tử đó là tỉ lệ số electron nhường, nhận hay góp chung của nguyên tử khi tham gia liên kết để hình thành phân tử.
I. Khái niệm liên kết hóa học
Lời giải:
Cấu hình electron của nguyên tử fluorine là 1s22s22p5.
Khi nguyên tử fluorine nhận thêm 1 electron thì cấu hình electron là 1s22s22p6
⇒ Giống với khí hiếm Ne.
Lời giải:
Để giảm năng lượng, các nguyên tử kết hợp lại thành phân tử theo xu hướng đạt tới cấu hình electron bền vững của khí hiếm.
II. Quy tắc octet
Lời giải:
- Sự hình thành liên kết trong phân tử F2
Khi hình thành liên kết hóa học trong phân tử F2, nguyên tử fluorine có 7 electron hóa trị, mỗi nguyên tử fluorine cần thêm 1 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử fluorine góp chung 1 electron.
Phân tử Fe được biểu diễn 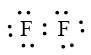
Xung quanh mỗi nguyên tử fluorine đều có 8 electron.
- Sự hình thành liên kết hóa học trong phân tử CCl4
Nguyên tử C có 4 electron hóa trị, nguyên tử Cl có 7 electron hóa trị. Mỗi nguyên tử Cl cần thêm 1 electron và nguyên tử C cần thêm 4 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử CCl4 được biểu diễn 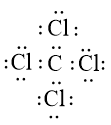
Xung quanh mỗi nguyên tử C và Cl đều có 8 electron.
- Sự hình thành liên kết hóa học trong phân tử NF3
Nguyên tử N có 5 electron hóa trị, nguyên tử F có 7 electron hóa trị. Mỗi nguyên tử F cần thêm 1 electron và nguyên tử N cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử NF3 được biểu diễn 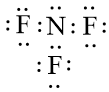
Xung quanh mỗi nguyên tử N và F đều có 8 electron.
Vận dụng quy tắc octet để giải thích sự tạo thành liên kết hoá học trong phosphine.
Lời giải:
Sự hình thành liên kết hóa học trong phosphine:
Khi hình thành liên kết hóa học trong phân tử PH3, nguyên tử H có 1 electron hóa trị, nguyên tử P có 5 electron hóa trị. Mỗi nguyên tử H cần thêm 1 electron và nguyên tử P cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet.
Phân tử PH3 được biểu diễn như sau: 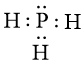
Xung quanh nguyên tử P có 8 electron.
Lời giải:
Ví dụ: Sự hình thành liên kết hóa học trong phân tử nitrogen (N2)
Khi hình thành liên kết hóa học trong phân tử N2, nguyên tử N có 5 electron hóa trị, mỗi nguyên tử N cần thêm 3 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử N góp chung 3 electron
Phân tử N2 được biểu diễn ![]()
Lý thuyết Quy tắc octet
I. Khái niệm liên kết hóa học
Liên kết hóa học là sự kết hợp giữa các nguyên tử tạo thành phân tử hay tinh thể bền vững hơn.
Trong các phản ứng hóa học, chỉ có các electron thuộc lớp ngoài cùng và phân lớp sát lớp ngoài cùng tham gia vào quá trình tạo thành liên kết.
Các electron hóa trị của nguyên tử một nguyên tố được quy ước biểu diễn bằng các dấu chấm đặt xung quanh kí hiệu nguyên tố.
Ví dụ:
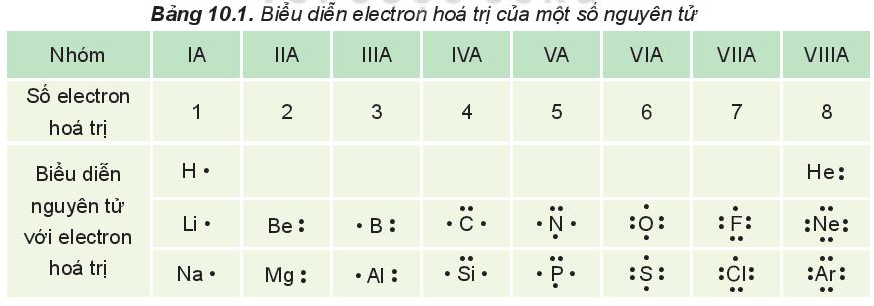
II. Quy tắc octet
Khi hình thành liên kết hóa học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm. Vì các khí hiếm (trừ helium) đều có 8 electron lớp ngoài cùng nên quy tắc này được gọi là quy tắc octet.
Ví dụ 1: Xét sự hình thành liên kết hóa học trong phân tử Cl2.
Cấu hình electron của nguyên tử Cl (Z = 17): [Ne]3s23p5.
Khi hình thành liên kết hóa học trong phân tử Cl2, nguyên tử Cl có 7 electron hóa trị, mỗi nguyên tử Cl cần thêm 1 electron để đạt cấu hình electron bão hòa theo quy tắc octet nên mỗi nguyên tử Cl góp chung 1 electron.
Phân tử Cl2 được biểu diễn:

Xung quanh mỗi nguyên tử Cl đều có 8 electron.
Ví dụ 2: Xét sự hình thành liên kết hóa học trong phân tử NaF.
Cấu hình electron của nguyên tử:
Na (Z = 11): [Ne]3s1 có 1 electron lớp ngoài cùng.
F (Z = 9): 1s22s22p5 có 7 electron lớp ngoài cùng.
Khi hình thành liên kết hóa học trong phân tử NaF, nguyên tử Na có 1 electron hóa trị, nguyên tử F có 7 electron hóa trị, nguyên tử Na nhường 1 electron hóa trị tạo thành hạt mang điện tích dương, nguyên tử F nhận 1 electron tạo thành hạt mang điện tích âm. Các hạt này đều đạt cấu hình electron bão hòa theo quy tắc octet và có điện tích trái dấu nên hút nhau.
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Bài 13: Liên kết hydrogen và tương tác Van der waals
Bài 15: Phản ứng oxi hóa – khử
Xem thêm tài liệu Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn lớp 10 – Kết nối tri thức
- Soạn văn lớp 10 (ngắn nhất) – Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn lớp 10 - KNTT
- Bố cục tác phẩm Ngữ văn lớp 10 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Kết nối tri thức
- Văn mẫu lớp 10 – Kết nối tri thức
- Giải Chuyên đề học tập Ngữ văn 10 – Kết nối tri thức
- Giải sgk Toán 10 – Kết nối tri thức
- Giải sbt Toán 10 – Kết nối tri thức
- Giải Chuyên đề Toán 10 – Kết nối tri thức
- Lý thuyết Toán 10 – Kết nối tri thức
- Chuyên đề dạy thêm Toán 10 Kết nối tri thức (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Global Success – Kết nối tri thức
- Giải sbt Tiếng Anh 10 Global Success – Kết nối tri thức
- Ngữ pháp Tiếng Anh 10 Global success
- Bài tập Tiếng Anh 10 Global success theo Unit có đáp án
- Trọn bộ Từ vựng Tiếng Anh 10 Global success đầy đủ nhất
- Giải sgk Vật lí 10 – Kết nối tri thức
- Giải sbt Vật lí 10 – Kết nối tri thức
- Giải Chuyên đề Vật lí 10 – Kết nối tri thức
- Lý thuyết Vật lí 10 – Kết nối tri thức
- Chuyên đề dạy thêm Vật lí 10 cả 3 sách (2024 có đáp án)
- Giải sgk Sinh học 10 – Kết nối tri thức
- Giải sbt Sinh học 10 – Kết nối tri thức
- Lý thuyết Sinh học 10 – Kết nối tri thức
- Giải Chuyên đề Sinh học 10 – Kết nối tri thức
- Giải sgk Lịch sử 10 – Kết nối tri thức
- Giải sbt Lịch sử 10 – Kết nối tri thức
- Giải Chuyên đề Lịch sử 10 – Kết nối tri thức
- Lý thuyết Lịch sử 10 - Kết nối tri thức
- Giải sgk Địa lí 10 – Kết nối tri thức
- Lý thuyết Địa Lí 10 – Kết nối tri thức
- Giải sbt Địa lí 10 – Kết nối tri thức
- Giải Chuyên đề Địa lí 10 – Kết nối tri thức
- Giải sgk Công nghệ 10 – Kết nối tri thức
- Lý thuyết Công nghệ 10 – Kết nối tri thức
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Kết nối tri thức
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Kết nối tri thức
- Giải Chuyên đề Kinh tế và pháp luật 10 – Kết nối tri thức
- Lý thuyết KTPL 10 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Kết nối tri thức
- Lý thuyết Giáo dục quốc phòng 10 – Kết nối tri thức
- Giải sbt Giáo dục quốc phòng 10 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 10 – Kết nối tri thức
- Giải sbt Hoạt động trải nghiệm 10 – Kết nối tri thức
- Giải sgk Tin học 10 – Kết nối tri thức
- Lý thuyết Tin học 10 – Kết nối tri thức
- Giải sbt Tin học 10 – Kết nối tri thức
- Giải Chuyên đề Tin học 10 – Kết nối tri thức
- Giải sgk Giáo dục thể chất 10 – Kết nối tri thức
